Xanthomonas campestris
En sida om mikrobiell biorealm om släktet Xanthomonas campestris
Klassificering
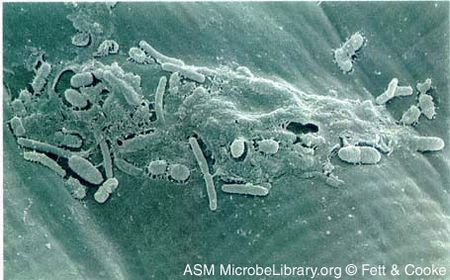
Courtesy of Fett & Cooke, ASM MicrobeLibrary
Taxa av högre ordning
Bakterier
Proteobakterier
Gammaproteobakterier
.
Xanthomonadales
Xanthomonadaceae
Xanthomonas
Xanthomonas campestris
Species
NCBI: Taxonomy
Xanthomonas campestris
Beskrivning och betydelse
Xanthomonas campestris är en aerob, gramnegativ stav som är känd för att orsaka svartröta hos korsblommor genom att göra kärlvävnaden mörkare. Över 20 olika pathovar av X. campestris har identifierats genom sin distinkta patogenitet på ett brett spektrum av växter, inklusive grödor och vilda växter. Denna bakterie är mesofil med en optimal temperatur på 25-30 grader Celsius (77-85 grader Fahrenheit) och inaktiv vid temperaturer under 10 grader Celsius (50 grader Fahrenheit) . X. campestris har överkänslig respons och patogenicitet (Hrp) pili som hjälper till att överföra effektorproteiner för att minska värdets försvar och glida genom vatten . De kan leva i jorden i över ett år och spridas genom alla vattenrörelser, inklusive regn, bevattning och ytvatten. Besprutning av friska växter med kopparfungicider kan minska spridningen av bakterierna på fältet. Men när plantan väl är infekterad kommer X. campestris så småningom att sprida sig till fröställningen och hämma tillväxten av en frisk avkomma.
Med hjälp av fermentering i renkultur kan X. campestris producera en extracellulär polysackarid som kallas xantangummi och som tillverkas kommersiellt som ett stabiliseringsmedel som används i många vardagsprodukter, bland annat salladsdressing och tandkräm . X. campestris är en modellorganism för att studera interaktioner mellan växter och bakterier. På grund av underskottet i grödor pågår ytterligare forskning om denna bakterie i hopp om att lära sig hur man kan göra växter resistenta mot denna patogen.
Genomstruktur
Genomstrukturerna hos X. campestris innehåller variationer beroende på pathovars. De olika stammarna av X. campestris uppvisar dock liknande egenskaper som cirkulära kromosomer, mobila genetiska element och proteinkodande sekvenser . År 2002 kunde den fullständiga arvsmassan av X. campestris pv campestris (Xcc) str. ATCC 33913 färdigställd och innehöll över 5 076 188 nukleotider som kodar för över 4 200 proteinkodande och 61 strukturella RNA. Med över 548 unika kodande sekvenser består X. campestris pv. vesicatoria (Xcv) av en cirkulär kromosom på 5,17 Mb, fyra plasmider och ett essentiellt typ III-proteinutsöndringssystem för patogenitet . Med hjälp av Recominbase-baserad In Vivo Expression Technology för att rikta in sig på tomat har Xcv visat sig ha 61 gener som är involverade i interaktionen mellan patogen och värd, inklusive en nödvändig virulenstransportör, citH homologgen .
Cellstruktur och ämnesomsättning
X. campestris är en stavformad gramnegativ bakterie som kännetecknas av sina två cellväggar och sitt gula pigment. Den har en filamentös struktur som kallas överkänslig respons och patogenicitet (Hrp) pili som är fäst vid typ III-proteinutsöndringssystem som genomför förmågan att överföra bakterieproteiner till växten och även motilitet i vatten .
Denna aeroba bakterie utför ett antal metaboliska vägar som är unikt beroende av pathovar. Hela sekvenseringen av Xcv:s genom uppvisar kolhydratmetabolismer som inkluderar: Glykolys/ glukoneogenes, citratcykel (TCA-cykel), pentosfosfatväg med mera. Xcv får sin energikälla genom oxidativ fosforylering, kolfixering, metan, kväve och svavelmetabolism .
X. campestris får kol från värden och omvandlar det till glukos genom glukoneogenes. Ytterligare forskning har visat att i glukoneogenesen innehåller Xcc endast malicenzym-PpsA-vägen som är nödvändig för virulens . Dessutom innehåller denna växtpatogen ett typ III-sekretionssystem (TTSS) som är nödvändigt för att angripa värden. TTSS är viktigt i patogenesen eftersom det överför effektorproteiner för att sänka värdens försvar. X. campestris skapar biofilm på växtytor och exemplifierar cell-cellkommunikation genom diffusible signal factor (DSF) .
Med sin förmåga att fermentera skapar X. campestris en extracellulär polysackarid, xantan, som produceras kommersiellt och används i en mängd olika vardagsprodukter som stabiliseringsmedel . Se Tillämpning inom bioteknik för mer information.
Ökologi
X. campestris orsakar stora förluster inom jordbruket på grund av sin livsmiljö i växter. Den kan leva i jorden i över ett år och spridas genom överbevattning och ytvatten . Denna bakterie trivs särskilt bra i vått och varmt väder med optimala temperaturer på 25-30 grader Celsius (77-85 grader Fahrenheit) . X. campestris är beroende av vatten för att överleva och förflytta sig till nästa värd. På grund av kontaminering vid odling förekommer de drabbade växterna vanligen i samma rader när de odlas . Se patologi för mer information.
Patologi

X. campestris kan upptäckas genom de svarta lesioner som utvecklas på växtytor vid kontaminering. Patogenen interagerar först med värden genom att utsöndra en rad effektorproteiner, inklusive överkänslig reaktion med hjälp av typ III-sekretionssystemet (TTSS) . Dessa effektorer kan uppträda på ett avirulent sätt genom att dölja sig för att utsöndra flera överkänslighetsreaktioner och yttre proteiner för att interaktion ska kunna ske med värdcellerna . X. campestris riktar sedan in sig på den vaskulära vävnaden och orsakar mörkfärgning och marginell bladkloros . Bakterien tränger in i bladet mot klyvöppningarna, hydathoderna och epidermalcellerna för att initiera nya skador. En allvarlig infektion inträffar i en ung fröplanta. Eftersom sjukdomen fortskrider i hela plantan kan huvudstammen inte bildas, vilket hämmar utvecklingen och gör ådrorna svarta. Så småningom sprider sig bakterien i hela kärlsystemet och till fröställningen, vilket leder till att fröet blir infekterat av framtida sjukdomar.
X. campestris uppträder mer under de våta årstiderna och har pili som möjliggör en glidande rörelse genom våta blad. När en växt väl är sjuk, kommer patogenen att sprida sig i alla former av vattenrörelser, inklusive regnstänk, till en ny värd.
Virulensfaktorer består av lytiska enzymer som angriper växtens cellvägg, utsöndring av proteaser, amylaser, cellulaser och lipaser som bidrar till att sänka växtens försvarsmekanismer. Dessutom är genklustret Rpf också avgörande för patogenesen för att X. campestris ska kunna moderera produktionen av dessa virulenta faktorer .
Användning på bioteknik
X. campestris fermenterar ett stabiliseringsmedel som kallas xantangummi och som används i många vardagsprodukter. Det producerades först kommersiellt på Kelco Company, ett stort läkemedelsföretag. Denna polysackarid är en ingrediens i produkter som Kraft French dressing, Weight Watchers-mat, Wonder Bread-produkter med mera . Xantangummi, som kommer från kolhydratjäsning av X. campestris, är pseudoplastiskt och lättblandat, vilket gör att det kan användas som förtjockningsmedel genom att öka viskositeten i en vätska. Dessutom förlänger xantangummi olje- och gaskällor även efter produktionen. Om vatten och xantangummi blandas i brunnarna, antingen genom att de pumpas in i marken eller genom sandblästring med högt tryck, bidrar det till att förtjocka vätskan för att frigöra råoljeprodukter och skära igenom stenar i gas- och oljekällor. Xantangummi kostar 7 dollar per pund jämfört med majsstärkelse som kostar 89 cent per pund.
Aktuell forskning
8.1 Biologisk bekämpning med stammar av Bacillus
Det pågår en sekvensering av arvsmassan i jakt på de viktiga gener som behövs för att utveckla resistenta växter. Ett försök gjordes med Bacillusstammar inklusive B. cereus, B. lentimorbus och B. pumilus som rival mot patogenen Xcc i kål. Bevis har visat att det finns hopp om biologisk bekämpning när Bacillus-stammen tillsattes i rötterna.
8.2 Reglerande nätverk för cell-cellkommunikation
Nyligen genomförda studier visar att X. campestris använder den diffusibla signalfaktorn (DSF) för cell-cellkommunikation. För att mikrokolonier ska kunna bilda en strukturerad biofilm krävs syntes av DSF från klustret för reglering av patogenitetsfaktorn (Rpf). Rpf-klustret innehåller nödvändiga gener för att patogenes ska inträffa. Utan den kritiska DSF-signaliseringen kommer Xcc att skapa en ostrukturerad biofilm av bakterier. Ytterligare forskning bedrivs för att förstå hur regleringsnätverket övervakas .
8.3 Genetisk variation i vilda korsblommor
Forskare har funnit genetisk mångfald i Xcc på vilda korsblommor. Med världens mest varierande och rikliga vilda korsblommiga växter gjordes studier i Kalifornien för att hitta eventuella skillnader i genetiska stammar på Xcc i infekterade vilda ogräs. Från både icke odlade och odlade områden isolerades Xcc från olika regioner i Kalifornien. Med hjälp av PCR (Amplified fragment length polymorphism PCR) (AFLP) för att identifiera den genetiska variationen i stammarna sekvenserades över 72 stammar för att visa 7 unika genotyper som var begränsade till sina respektive platser. Icke odlade vilda ogräs nära kusten hade stammar av Xcc som var specifika för regionen och skilde sig från de ogräs som odlades nära odlingsområden med producerade grödor.
Referens
Averre, Charles W. ”Black Rot of Cabbage and Related Crops” Accessed on August 16, 2007.
Ritchie David F, Averre Charles W. ”Bacterial Spot of Pepper and Tomato”. North Carolina State University College of Agriculture and Life Sciences. Tillgänglig den 20 augusti 2007.
Weber E, Ojanen-Reuhs T, Huguet E, Hause G, Romantschuk M, Korhonen TK, Bonas U, Koebnik R. ”The type III-dependent Hrp pilus is required for productive interaction of Xanthomonas campestris pv. vesicatoria with pepper host plants”. Journal of Bacteriology. 2005. Volume 187(7) s.2458-69.
Kuntz, L. ”X står för Xantangummi”. Design av livsmedelsprodukter. Tillgänglig den 26 augusti 2007.
Vorhölter FJ, Thias T, Meyer F, Bekel T, Kaiser O, Pühler A, Niehaus K. ”Comparison of two Xanthomonas campestris pv. campestris genomes revealed differences in their gene composition”. Journal Biotechnology. 2003. Volym 106(203). s.193-202.
”Xanthomonas campestris pv. campestris str. ATCC 33913, komplett genom”. Public Library of Science Biology. 2002. Tillgänglig den 25 augusti 2007.
Thieme F, Koebnik R, Bekel T, Berger C, Boch J, Büttner D, Caldana C, Gaigalat L, Goesmann A, Kay S, Kirchner O, Lanz C, Linke B, McHardy AC, Meyer F, Mittenhuber G, Nies DH, Niesbach-Klösgen U, Patschkowski T, Rückert C, Rupp O, Schneiker S, Schuster SC, Vorhölter FJ, Weber E, Pühler A, Bonas U, Bartels D, Kaiser O. ”Insights into genome plasticity and pathogenicity of the plant pathogenic bacterium Xanthomonas campestris pv. vesicatoria revleaed by the complete genome sequence”. Journal of Bacteriology. 2005. Volym 187(21). s 7254-66.
Tamir Ariel D., Navon N, Burdman S. ”Identification of Xanthomonas campestris pv. vesicatoria genes induced in its interaction with tomato”. Journal of Bacteriology. 2007. Volym 189(17). P.6359-71.
Weber E, Koebnik R. ”Domain structure of HrpE, the Hrp pilus subunit of Xanthomonas campestris pv. vesicatoria”. Journal of Bacteriology. 2005. Volym 187(17). s. 6175-86.
”Xanthomonas campestris pv. vesicatoria”. Kyoto Encyclopedia of Genes and Genomes. Tillgänglig den 24 augusti 2007.
Tang DJ, He YQ, Feng JX, He BR, Jiang BL, Lu GT, Chen B, Tang JL. ”Xanthomonas campestris pv. campestris har en enda glukoneogen väg som krävs för virulens”. Journal of Bacteriology. 2005. Volume 187(17). s 6231-7.
Torres PS, Malamud F, Rigano LA, Russo DM, Marano MR, Castagnaro AP, Zorreguieta A, Bouarab K, Dow JM, Vojnov AA. ”Kontrollerad syntes av DSF-cell-cellsignalen krävs för biofilmsbildning och virulens hos Xanthomonas campestris.” Environmental Microbiology. 2007. Volym 9(8). s. 2101-9.
Wang L, Tang X, He C. ”The bifunctional effector AvrXccC of Xanthomonas campestris pv. campestris requires plasma membrane-anchoring for host recognition”. Molekylär växtpatologi. 2007. Volym 8(4). s 491-501.
Niehaus Karsten. ”Xanthomonas campestris pv. campestris-genomprojektet”. Tillgänglig den 20 augusti 2007.
Dow JM, Crossman L, Findlay K, He YQ, Feng JX, Tang JL. ”Biofilmspridning i Xanthomonas campestris styrs av cell-cell-signalering och krävs för full virulens mot växter”. Proceedings of the National Academy of Sciences of the United States of America. 2003. Volym 100(19). s 10995-1000.
”Teknik på marknaden”. Förenta staternas jordbruksdepartement, Agricultural Research Service (ARS). Tillgänglig den 21 augusti 2007.
Massomo S, Mortensen C, Mabagala R, Newman M, Hockenhull J. ”Biological control of black rot (Xanthomonas campestris pv. campestris) of Cabbage in Tanzania with Bacillus strains”. Journal of Phytopathology. 2004. Volym 152(2). s. 98-105.
Torres PS, Malamud F, Rigano LA, Russo DM, Marano MR, Castagnaro AP, Zorreguieta A, Bouarab K, Dow JM, Vojnov AA. ”Kontrollerad syntes av DSF-cell-cellsignalen krävs för biofilmsbildning och virulens hos Xanthomonas campestris”. Miljömikrobiologi. 2007. Volym 9(8). s 2101-9.
Ignatov, A., Sechler, A.J., Schuenzel, E., Agarkova, I.V., Vidaver, A.K., Oliver, B., Schaad, N.W. 2007. ”Genetisk mångfald i populationer av Xanthomonas campestris pv. campestris i korsblommiga ogräs i Kaliforniens centrala kustregion”. Phytopathology. 2007. Volym 97. s. 803-812.
Redigerad av Tammie Chau, student till Rachel Larsen