Xanthomonas campestris
Xanthomonas campestris属の微生物バイオレームページ
分類
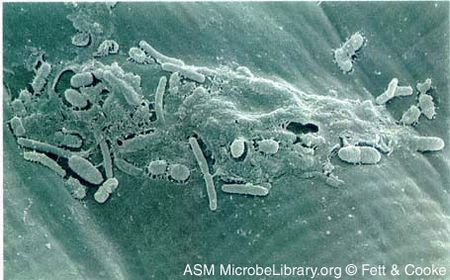
Fett & Cookeさん提供のものです。 ASM MicrobeLibrary
高次分類群
バクテリア
プロテオバクテリア
ガンマプロテオバクテリアXanthomonadales
Xanthomonas campestris
Species
NCBI.Xanthomonadales
Xanthomonas campestris
Xanthomonas group Xanthomonas family
Species
Xanthomonadales Xanthomonas group
Xanthomonas campestris
Description and significance
Xanthomonas campestrisは好気性のグラム陰性桿菌で、アブラナ科植物の血管組織を黒化させて黒腐病を引き起こすことが知られています。 X. campestrisは、農作物や野生の植物など幅広い植物に対して、その特徴的な病原性から20種類以上の病原体が同定されており、宿主に関連しています。 この細菌は好中性で、最適温度は摂氏25〜30度、摂氏10度以下では不活性である。 X. campestrisは、Hypersensitive response and pathogenicity (Hrp) piliを持ち、宿主の防御力を低下させるエフェクタータンパク質を輸送し、水中を滑るように移動することができる。 土壌中に1年以上生息し、雨水、灌漑水、地表水などあらゆる水の移動によって拡散することができる。 健康な植物に銅系殺菌剤を散布することで、圃場での菌の拡散を抑えることができる。 しかし、一度感染すると、X. campestrisは最終的に種子の茎に広がり、健康な子孫の成長を阻害する。
純粋培養発酵により、X. campestrisはキサンタンガムとして知られる細胞外多糖を生産することができ、サラダドレッシングや歯磨き粉など多くの日用品に使われる安定化剤として商業的に生産されている。 X. campestrisは、植物とバクテリアの相互作用を研究するためのモデル生物である。
ゲノム構造
X.campestrisのゲノム構造は、病原体によって様々なバリエーションがある。 しかし、X. campestrisの異なる株は、円形染色体、移動性遺伝要素、タンパク質コード配列など、類似した特徴を示す。 2002年にX. campestris pv campestris (Xcc) str.の全ゲノムが解読された。 ATCC 33913のゲノムが完成し、4200以上のタンパク質コードと61の構造RNAをコードする5,076,188塩基が含まれることが明らかになった。 X. campestris pv. vesicatoria (Xcv)は、548以上のユニークなコード配列を持ち、5.17MBの円形染色体、4つのプラスミド、病原性に必須のIII型タンパク質分泌システムから構成されている。 Xcvは、トマトを標的としたリコミンベースによるIn Vivo発現技術により、病原性に必要なトランスポーターcitH homologue遺伝子など、病原体と宿主の相互作用に関与する61の遺伝子を持つことが明らかになった
細胞構造と代謝
X. campestrisは棒状のグラム陰性菌で、2つの細胞壁と黄色の色素が特徴である。 Hrp(過敏反応病原性)と呼ばれる糸状構造を持ち、III型タンパク質分泌系に付着して、細菌タンパク質を植物に移行する能力と、水中での運動性を備えている。
この好気性細菌は、病原体に独自に依存した多くの代謝経路を実行する。 Xcvの全ゲノム配列決定により、以下のような炭水化物代謝を示す。 解糖/糖新生、クエン酸サイクル(TCAサイクル)、ペントースリン酸経路、その他。 Xcvは、酸化的リン酸化、炭素固定、メタン、窒素、硫黄代謝によってエネルギー源を獲得する。
X. campestrisは宿主から炭素を獲得し、それをグルコース生成によってグルコースに変換する。 さらに研究の結果、Xccは糖新生において、病原性に必須なリンゴ酵素-PpsA経路のみを持つことが明らかとなった。 さらに、この植物病原菌は、宿主を攻撃するために必要なIII型分泌システム(TTSS)を持っている。 TTSSは、宿主の防御力を低下させるためにエフェクタータンパク質を移送するため、病原体形成において重要である。 植物表面でバイオフィルムを形成するX. campestrisは、拡散性シグナル因子(DSF)を介した細胞間コミュニケーションを例証している。
発酵する能力を持つX. campestrisは、細胞外多糖であるキサンタンを作り、これは商業的に生産され、安定化剤として様々な日用品に使用されている. 詳しくはバイオテクノロジーへの応用をご覧ください。
生態
X. campestrisは植物に生息するため、農業に大きな損失を与えています。 この菌は土壌中に1年以上生息し、頭上灌漑や地表水を通じて拡散することができる。 この細菌は、特に湿った暖かい気候の時に繁殖し、最適温度は摂氏25~30度です。 X. campestrisは、生存と次の宿主への移動のために水に依存しています。 栽培作業中の汚染により、罹患した植物は通常、農作業時に同じ列で発生する。 詳細は病理学を参照。
病理学

X. campestrisは、汚染されると植物の表面に黒い病斑ができることで見分けることができる。 病原体はまず、III型分泌システム(TTSS)を用いて過敏反応などのエフェクタータンパク質の数々を分泌することで宿主と相互作用する。 これらのエフェクターは、宿主細胞との相互作用が起こるために、いくつかの過敏反応や外側のタンパク質を分泌するように偽装して、無害な振る舞いをすることがある。 X. campestrisはその後、血管組織を標的にし、葉の黒化および葉の縁のクロロシスを引き起こす。 細菌は葉の中に入り込み、気孔、水和器、表皮細胞へと移動し、新しい病害を引き起こす。 幼苗で重度の感染が起こる。 植物全体に病気が進行するため、主茎が形成されず、発育が阻害され、葉脈が黒くなる。 最終的には、細菌が血管系全体に増殖し、種子の茎に達し、種子が将来の病気に感染する原因となる。
雨季に多く発生するX. campestrisは、湿った葉を滑るように移動する毛管を持つ。 一旦発病すると、雨のしぶきなどあらゆる水の動きを利用して、新しい宿主へと広がっていく。
病原体は、植物の細胞壁を攻撃する溶解酵素、植物の防御機構を低下させるプロテアーゼ、アミラーゼ、セルラーゼ、リパーゼの排泄物から構成される。 さらに、X. campestrisがこれらの病原性因子の産生を穏やかにするために、Rpf遺伝子群も病原性に重要である。
バイオテクノロジーへの応用
X. campestrisは、多くの日常製品に使用されているキサンタンガムという安定剤も発酵させている。 これは、大手製薬会社のケルコ社で初めて商業生産されたものである。 この多糖類は、クラフト社のフレンチドレッシング、ウェイトウォッチャー社の食品、ワンダーブレッド社の製品などの原料となっている。 キサンタンガムは、X.campestrisによる糖質発酵から生まれたもので、擬塑性でなじみやすい性質から、液体の粘度を高めて増粘剤として使用されています。 また、キサンタンガムは、石油やガスの井戸を生産後も長持ちさせる効果がある。 ポンプで地中に注入するか、高圧サンドブラストで井戸に水とキサンタンガムを混ぜると、液体が増粘して原油の粗製品を放出したり、ガスや油井の岩盤を切開したりすることができるのだ。
Current Research
8.1 Bacillus株を用いた生物学的制御
耐性植物の開発に必要な必須遺伝子を探すために、ゲノム解読が行われている。 キャベツの病原体Xccの対抗馬として、B. cereus, B. lentimorbus, B. pumilusなどのBacillus株を使った実験が行われた。 8.2 細胞間情報伝達の制御ネットワーク
最近の研究では、X. campestrisが細胞間情報伝達に拡散性シグナル因子(DSF)を利用していることが明らかになった。 マイクロコロニーが構造化されたバイオフィルムを形成するためには、DSFの合成がregulation of pathogenicity factor (Rpf) clusterから必要であることがわかった。 Rpfクラスターには、病原性を発揮するために必要な遺伝子が含まれている。 重要なDSFシグナルがなければ、Xccは細菌の非構造化バイオフィルムを形成することになる。 調節ネットワークがどのように監視されているかを理解するために、さらなる研究が行われている。 .
8.3 野生アブラナにおける遺伝子変異
研究者は、野生アブラナのXccに遺伝子多様性を発見している。 世界で最も多様で豊富な野生のアブラナ科植物を対象に、感染した野生の雑草の Xcc の遺伝子系統に違いがあるかどうか、カリフォルニア州で調査が行われた。 その結果、カリフォルニア州の様々な地域から、非耕作地および耕作地の両方においてXccが分離された。 その結果、72株以上の菌株の塩基配列が決定され、それぞれの地域に限定された7種類の遺伝子型が確認された。 海岸付近の非栽培の野生の雑草には、その地域に特有のXccの株があり、生産作物地域の近くで栽培されている雑草とは異なることがわかった。
参考文献
Averre, Charles W. “Black Rot of Cabbage and Related Crops” Accessed on August 16, 2007.
Ritchie David F, Averre Charles W. “Bacterial Spot of Pepper and Tomato”. ノースカロライナ州立大学農学生命科学部。 2007 年 8 月 20 日にアクセス。
Weber E, Ojanen-Reuhs T, Huguet E, Hause G, Romantschuk M, Korhonen TK, Bonas U, Koebnik R. “The type III-dependent Hrp pilus is required for productive interaction of Xanthomonas campestris pv. vesicatoria with pepper host plants.”. ジャーナル・オブ・バクテリオロジー。 2005. 2005年、第187巻(7) p.2458-69。
Kuntz, L. “X is for Xanthan Gum”(Xはキサンタンガムの略)。 フードプロダクトデザイン。 2007年8月26日にアクセス。
Vorhölter FJ, Thias T, Meyer F, Bekel T, Kaiser O, Pühler A, Niehaus K. “Comparison of two Xanthomonas campestris pv. campestris genomes revealed differences in their gene composition”. ジャーナル・バイオテクノロジー。 2003. 第106巻(203)号 p.193-202.
“Xanthomonas campestris pv. campestris str. ATCC 33913, complete genome”. Public Library of Science Biology. 2002. 2007年8月25日アクセス。
Thieme F, Koebnik R, Bekel T, Berger C, Boch J, Büttner D, Caldana C, Gaigalat L, Goesmann A, Kay S, Kirchner O, Lanz C, Linke B, McHardy AC, Meyer F, Mittenhuber G, Nies DH, Niesbach-Klösgen U, Patschkowski T, Rückert C, Rupp O, Schneiker S, Schuster SC, Vorhölter FJ, Weber E, Pühler A, Bonas U, Bartels D, Kaiser O. 「植物病原細菌Xanthomonas campestris pv. vesicatoriaのゲノム可塑性と病原性に関する全ゲノム配列による洞察”. Journal of Bacteriology. 2005. 巻187(21). p 7254-66.
Tamir Ariel D., Navon N, Burdman S. “Identification of Xanthomonas campestris pv. vesicatoria genes induced in its interaction with tomato”(ザントモナス・キャンペストリス・ヴィシキャトリア・ヴィシキャトル遺伝子の特定)。 Journal of Bacteriology. 2007. 第189巻(17). P.6359-71.
Weber E, Koebnik R. “Domain structure of HrpE, the Hrp pilus subunit of Xanthomonas campestris pv. vesicatoria”. Journal of Bacteriology. 2005. 2005. 187(17). p. 6175-86.
“Xanthomonas campestris pv. vesicatoria.”. 京都大学百科事典「遺伝子とゲノム」. 2007年8月24日アクセス。
Tang DJ, He YQ, Feng JX, He BR, Jiang BL, Lu GT, Chen B, Tang JL. 「Xanthomonas campestris pv. campestrisは病原性に必要な単一のグルコネーシス経路を持つ.”. Journal of Bacteriology. 2005. Volume 187(17). p 6231-7.
Torres PS, Malamud F, Rigano LA, Russo DM, Marano MR, Castagnaro AP, Zorreguieta A, Bouarab K, Dow JM, Vojnov AA. “DSF 細胞間シグナルの制御された合成は、Xanthomonas campestris のバイオフィルム形成と病原性に必要である。” Environmental Microbiology. 2007. Volume 9(8). p. 2101-9.
Wang L, Tang X, He C. “The bifunctional effector AvrXccC of Xanthomonas campestris pv. campestris requires plasma membrane-anchoring for host recognition.”。 Molecular Plant Pathology. 2007. Volume 8(4). P 491-501.
Niehaus Karsten. “The Xanthomonas campestris pv. campestris genome project”. 2007年8月20日にアクセス。
Dow JM, Crossman L, Findlay K, He YQ, Feng JX, Tang JL. 「Xanthomonas campestris のバイオフィルム分散は、細胞間シグナルによって制御され、植物への完全な病原性に必要である”. 米国科学アカデミー紀要。 2003. Volume 100(19). p 10995-1000.
“テクノロジー・イン・ザ・マーケットプレイス”. 米国農務省農業研究事業団(ARS)。 2007年8月21日にアクセス。
Massomo S, Mortensen C, Mabagala R, Newman M, Hockenhull J. “Biological control of black rot (Xanthomonas campestris pv. campestris) of Cabbage in Tanzania with Bacillus strains”.タンザニアにおけるキャベツの黒腐病(Xanthomonas campestris pv. campestris) の生物学的防除。 を発表した。 2004. 4109>
Torres PS, Malamud F, Rigano LA, Russo DM, Marano MR, Castagnaro AP, Zorreguieta A, Bouarab K, Dow JM, Vojnov AA.「バチルス菌によるタンザニア産キャベツの黒腐病防除」. 「DSF細胞間シグナルの制御された合成は、Xanthomonas campestrisのバイオフィルム形成と毒性に必要である」。 Environmental microbiology. 2007. ボリューム 9(8). p 2101-9.
Ignatov, A., Sechler, A.J., Schuenzel, E., Agarkova, I.V., Vidaver, A.K., Oliver, B., Schaad, N.W. 2007年. 「カリフォルニア州中部沿岸のアブラナ科雑草におけるXanthomonas campestris pv. campestrisの集団における遺伝的多様性」(Genetic diversity in populations of Xanthomonas campestris pv. campestris in cruciferous weeds in central coastal California) Phytopathology. 2007. 第 97 巻 p. 803-812.
編集:Tammie Chau、Rachel Larsenの学生
。