Modyfikacja metody Winklera do oznaczania stężenia tlenu rozpuszczonego w małych objętościach próbek
First published on 27 August 2010
Metoda Winklera jest najpopularniejszą procedurą oznaczania stężenia tlenu rozpuszczonego (DO) w próbkach wody. Jednakże, metoda ta wymaga stosunkowo dużej objętości próbki 200 mL do dokładnego oznaczenia DO. Zaproponowano wiele alternatywnych metod pomiaru stężenia DO w małych objętościach próbek, ale większość z nich ma problemy związane z niską dokładnością, wysokimi kosztami, skomplikowanym oprzyrządowaniem lub długim czasem analizy. W niniejszej pracy zaproponowano prostą modyfikację metody Winklera do pomiaru stężenia DO w próbkach o objętości 1 mL. Proponowana metoda jest dokładna, tania, prosta i szybka. Stężenia DO mierzono w 33 próbkach zarówno konwencjonalną metodą Winklera (WM), jak i proponowaną metodą (PM). Dla 23 z 33 analizowanych próbek hipoteza, że średnie populacyjne pomiarów są równe (μ1 = μ2) nie mogła być odrzucona na 95-procentowym poziomie ufności, a dla 19 próbek hipoteza, że wariancje populacyjne pomiarów są równe (σ21 = σ22) nie mogła być odrzucona na 95-procentowym przedziale ufności. Stwierdzono zatem, że w większości przypadków pomiary DO za pomocą WM i PM dają porównywalne wyniki zarówno pod względem dokładności, jak i precyzji.
Wprowadzenie
Metoda Winklera (metoda nr 4500-O-C)1 została powszechnie przyjęta jako dokładna i wiarygodna metoda2 pomiaru stężenia tlenu rozpuszczonego (DO) w różnych próbkach wody. Metoda ta jest uważana za wzorcową dla oznaczania DO. Jednak główną wadą tej metody jest wymóg dużej objętości próbki wynoszącej 200 mL.3
Do pomiaru DO opracowano również wiele alternatywnych metod. Metody te należą do trzech różnych kategorii, (1) metody kolorymetryczne, (2) metody wykorzystujące chromatografię gazową i (3) metody wykorzystujące czujniki elektrochemiczne i optyczne. Metody kolorymetryczne mogą być stosowane do oznaczania DO w małych objętościach próbek. Mają one jednak wady, takie jak konieczność stosowania drogich (np. zol złota) lub toksycznych (np. cyjanek) odczynników chemicznych.4 Brak odpowiedniego uzasadnienia w doborze długości fali pomiarowej jest kolejnym czynnikiem ograniczającym te metody.5 Oznaczanie DO jest również możliwe przy użyciu chromatografii gazowej. Jednak metody chromatografii gazowej, choć dokładne i wymagające niewielkich objętości próbek, są jednak czasochłonne i kosztowne. Czujniki elektrochemiczne są szeroko stosowane do pomiaru DO, a ich zalety i wady zostały omówione w innym miejscu.6 Czujniki elektrochemiczne generalnie cierpią na nieodwracalne efekty ciśnieniowe, zanieczyszczenie siarkowodorem i wrażliwość krzyżową.7 Zużywają one również DO podczas pomiaru i dlatego mogą być nieodpowiednie dla bardzo małych objętości próbek. Ostatnio skoncentrowano się na rozwoju czujników optycznych opartych na zasadzie dynamicznego wygaszania luminescencji tlenu.8 Te czujniki optyczne są łatwe w użyciu, mają szybki czas odpowiedzi i są trwałe. Jednakże wszystkie czujniki, zarówno elektrochemiczne jak i optyczne, wymagają kalibracji metodą Winklera ze względu na wrażliwość czujników na temperaturę i ciśnienie.9,10 Są one również wrażliwe na bio-fouling i rozwój bakterii na powierzchni czujnika.8
Z uwagi na nieodłączne ograniczenia metod alternatywnych opisanych powyżej oraz ich zależność od metody Winklera w zakresie kontroli krzyżowej i kalibracji, zaproponowano również kilka modyfikacji samej metody Winklera do pomiaru stężenia DO w próbkach o objętości 1-10 mL.11,12,13 Jednakże takie metody „mikrowtryskiwaczy” nie są zbyt popularne ze względu na złożone wymagania instrumentalne i wyszukane środki ostrożności wymagane w celu uniknięcia zanieczyszczenia próbek poprzez wymianę z tlenem atmosferycznym. Metody te zostały poddane krytycznemu przeglądowi w innym miejscu.14 Grawimetryczna metoda miareczkowania Micro-Winklera została ostatnio zaproponowana15 do pomiaru DO w małych próbkach. Jednakże, procedura ta wymaga wielokrotnych i dokładnych pomiarów grawimetrycznych przy użyciu czułej wagi i stąd wydaje się być dość złożona.
Na podstawie przeglądu literatury, wydaje się, że prawie wszystkie metody opracowane dla pomiarów DO w małych próbkach są wadliwe w taki czy inny sposób. Stąd istnieje ciągła potrzeba opracowania lepszej, tj. dokładnej, precyzyjnej, taniej, prostej i szybkiej metody pomiaru DO w małych objętościach próbek.
Zarys proponowanej metody
Podstawowym wyzwaniem w pomiarze stężenia DO w małych próbkach jest zapobieganie zanieczyszczeniu próbek poprzez interakcję z atmosferą. Proponuje się wprowadzenie warstwy cieczy izolującej pomiędzy próbką wody a atmosferą. Wymagane właściwości cieczy izolującej to: nieprzepuszczalność wody, gęstość mniejsza niż wody i pomijalna zdolność rozpuszczania tlenu. Proponuje się, aby ciecz izolacyjną umieścić w fiolce, a próbkę wody, której DO ma być oznaczane (objętość 1 mL), wprowadzić bezpośrednio pod warstwę cieczy izolacyjnej. W ten sposób próbka wody zostaje skutecznie odcięta od atmosfery. DO w próbce wody może być następnie ustalone i przeliczone na równoważną ilość jodu przy użyciu tych samych odczynników, które są stosowane w metodzie Winklera. Roztwór jodu jest następnie ekstrahowany z fiolki za pomocą strzykawki i miareczkowany przy użyciu Na2S2O3 w celu oznaczenia stężenia DO w próbce.
Po kilku rundach prób, n-heksan został wybrany jako ciecz izolująca, jak opisano powyżej. n-heksan jest lżejszy od wody (ciężar właściwy = 0,7) i jest praktycznie niemieszalny z wodą. Rozpuszczalność tlenu w n-heksanie wynosi 0,002 ułamka molowego,16i.e., tlen jest praktycznie nierozpuszczalny w n-heksanie.
Materiał i metody
Wszystkie użyte odczynniki były klasy odczynnika analitycznego (>99% czystości, Loba Chemicals, Indie). Woda dejonizowana (Milli-Q, Millipore, USA) była używana do przygotowania odczynników i rozcieńczania próbek. Użyty n-heksan był klasy HPLC (>99% czystości, Merck, Indie). W badaniach użyto szkła borokrzemianowego. Roztwory MnSO4 i jodku alkaliczno-azidowego przygotowano zgodnie z metodami standardowymi (metoda nr 4500-O C).1
Procedura pomiaru DO proponowaną metodą (PM) była następująca. Początkowo 0,5 mL n-heksanu przenoszono do szklanej fiolki o pojemności 16 mL (Wheaton Science, USA). Następnie 1 mL n-heksanu pobierano do pipety o pojemności 2 mL, a pipetę dalej napełniano 1 mL próbki wody, której stężenie DO miało być oznaczone. Powyższa procedura pobierania próbek zapewniała, że próbka była pobierana bez przestrzeni nadpowierzchniowej. Ten etap zbierania próbki jest najważniejszy, ponieważ pojawienie się jakichkolwiek pęcherzyków lub szczeliny powietrznej na granicy faz heksan-woda lub w innym miejscu pipety może prowadzić do błędów. Następnie ujście pipety umieszczono poniżej warstwy heksanu w fiolce i w ten sposób próbkę wprowadzono poniżej warstwy heksanu, unikając jakiegokolwiek kontaktu próbki z atmosferą. Pobranie próbki do pipety i naniesienie jej poniżej warstwy heksanu w fiolce należy wykonać jak najszybciej, aby zminimalizować błędy. Następnie do próbki wody pod warstwą heksanu wprowadzono 5 μL MnSO4 za pomocą mikrostrzykawki 10 μL (Hamilton, USA), po czym w podobny sposób dodano 5 μL roztworu jodku alkaliczno-azidowego. Tworzenie osadu rozpoczęło się natychmiast po dodaniu i zakończyło się w ciągu 3 min. Następnie do osadu utworzonego pod warstwą heksanu dodawano mikropipetą 0,1 mL zwięzłego H2SO4. Osad rozpuścił się w ciągu 3 min i pod warstwą heksanu powstał żółty roztwór jodu. Dokładnie 1 mL roztworu jodu wyekstrahowano spod warstwy heksanu za pomocą mikrostrzykawki i przeniesiono do zlewki o pojemności 25 mL. W celu ułatwienia miareczkowania 1 mL roztworu jodu w zlewce rozcieńczono do ∼ 10 mL przez dodanie wody dejonizowanej. Dodanie wody dejonizowanej spowodowało jedynie rozcieńczenie roztworu jodu, nie wpływając na ilość jodu w zlewce. Zawartość zlewki miareczkowano 0,00625 M roztworem Na2S2O3. 1 mL tego titranta odpowiada 55,5 mg L-1 DO w oryginalnej próbce. Titrant pobierano do mikrostrzykawki o pojemności 250 μL (Hamilton, USA) i dodawano kroplami do zlewki ciągle mieszając, aż żółty kolor jodu został prawie całkowicie usunięty. Następnie dodawano 1-2 krople roztworu skrobi i kontynuowano miareczkowanie aż do zaniku niebieskiego zabarwienia spowodowanego obecnością skrobi. Na podstawie objętości titranta wymaganej w danym miareczkowaniu obliczano stężenie DO w próbce oryginalnej.
Stężenie DO oznaczano również w różnych próbkach metodą Winklera (WM). Wymagania dotyczące odczynników i inne szczegóły dotyczące obu metod przedstawiono w Tabeli 1.
| Nr próbki. | Odczynnik | Ilość | Siła | ||
|---|---|---|---|---|---|
| WM | PM | WM | PM | ||
| Próbka | 200 mL | 1 mL | – | – | |
| MnSO4 | 1 mL | 5 μL | Jak na WM | ||
| Odczynnik alkalicznyodczynnik azydkowo-jodkowy | 1 mL | 5 μL | Jak na WM | ||
| Na2S2O3 | Jak wymagany | Jak wymagany | 0.025M | 0,00625M | |
| H2SO4 | 1 mL | 0.1 mL | Jak na WM | ||
| Skrobia | 1-2 krople | 1-2 krople | Jak na WM | ||
| n-.Heksan | Nie używany | 1.5 mL | – | – | |
Wyniki i dyskusja
Stężenie DO zmierzono w 33 próbkach wody (patrz Tabela 2) uzyskanych z różnych miejsc w mieście Kanpur, Indie i jego okolicach. Z 33 próbek, 8 było próbkami wody wodociągowej, 16 było próbkami wody rzecznej, 6 było próbkami ścieków domowych rozcieńczonych wodą wodociągową, 2 były próbkami wody gruntowej i 1 była próbką wody stawowej. Próbki zostały wybrane w taki sposób, aby stężenia DO mogły być mierzone w szerokiej gamie matryc próbek. Dla każdej próbki wykonano kilka powtarzających się pomiarów DO, zarówno przez WM, jak i PM. Obliczone średnie dla próbki (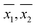 ), odchylenia standardowe dla próbki (S1, S2) oraz liczbę powtórzeń pomiarów (n1, n2) odpowiednio dla WM i PM przedstawiono w tabeli 2 dla każdej próbki.
), odchylenia standardowe dla próbki (S1, S2) oraz liczbę powtórzeń pomiarów (n1, n2) odpowiednio dla WM i PM przedstawiono w tabeli 2 dla każdej próbki.
Wszystkie wykresy normalne zestawów powtórzonych pomiarów wykonanych obiema metodami były w przybliżeniu liniowe, co wskazuje, że pomiary powtórzone miały rozkład normalny, a zatem nadawały się do dalszej analizy statystycznej na tej podstawie. Dla celów ilustracyjnych, na rys. 1A przedstawiono normalne wykresy dla pięciu pomiarów próbek wykonanych przez WM. Normalne wykresy dla tych samych pomiarów pięciu próbek wykonanych przez PM przedstawiono na Rys. 1B.
Wariancje (S21,S22) w pomiarach replikacyjnych próbki odpowiednio przez WM i PM zostały wykorzystane do porównania parami odpowiednich wariancji populacji (σ21,σ22) przy użyciu testu F. Spośród 33 próbek, dla których DO mierzono dwiema metodami (WM i PM), hipoteza, że wariancje populacji były równe (σ21 = σ22) nie mogła być odrzucona na 95-procentowym poziomie ufności dla 19 próbek. Ponadto, hipoteza, σ21 > σ22 nie mogła być odrzucona dla 4 próbek, podczas gdy hipoteza, σ21 < σ22 nie mogła być odrzucona dla pozostałych 10 próbek, wszystkie na 95 procentowym poziomie ufności. Wyniki te zostały podsumowane w tabeli 3.
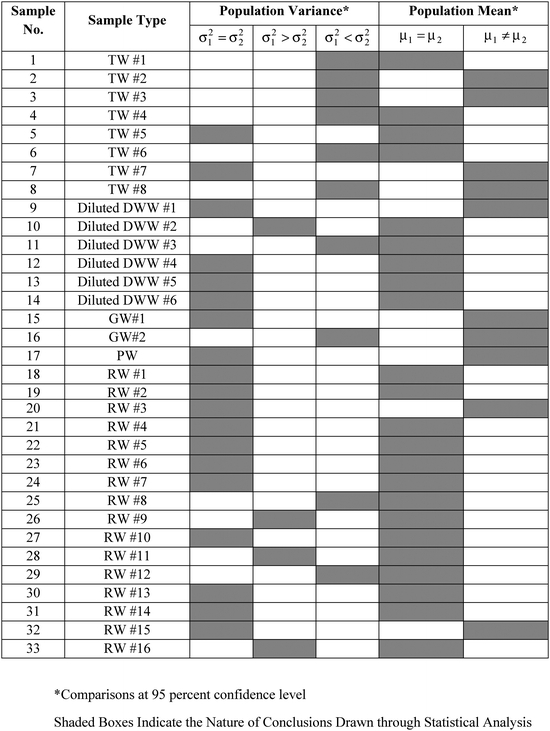
Ponadto, wariancje próbek (S21,S22) i średnie próbki (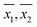 ) dla każdej próbki, uzyskane odpowiednio przez WM i PM zostały użyte do porównania parami odpowiadających im średnich populacji (μ1, μ2). W przypadku próbek o równych wariancjach (patrz tabela 3), porównania parami dokonano za pomocą testu t-Studenta. W przypadku próbek o nierównych wariancjach (patrz Tabela 3), porównania parami dokonano przy użyciu testu t-testu nierównych wariancji.17 W 23 z 33 próbek, w których pomiary DO zostały wykonane zarówno przez WM jak i PM, hipoteza, że średnie populacji były równe (μ1 = μ2) nie mogła być odrzucona na 95-procentowym poziomie ufności.
) dla każdej próbki, uzyskane odpowiednio przez WM i PM zostały użyte do porównania parami odpowiadających im średnich populacji (μ1, μ2). W przypadku próbek o równych wariancjach (patrz tabela 3), porównania parami dokonano za pomocą testu t-Studenta. W przypadku próbek o nierównych wariancjach (patrz Tabela 3), porównania parami dokonano przy użyciu testu t-testu nierównych wariancji.17 W 23 z 33 próbek, w których pomiary DO zostały wykonane zarówno przez WM jak i PM, hipoteza, że średnie populacji były równe (μ1 = μ2) nie mogła być odrzucona na 95-procentowym poziomie ufności.
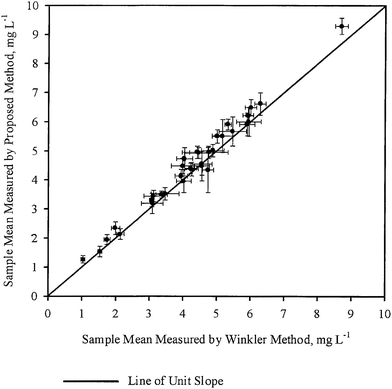
Średnie próbki (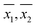 ) dla każdej próbki, uzyskane odpowiednio przez WM i PM zostały wykreślone względem siebie na Rys. 2. Słupki błędów pokazane na rysunku odpowiadają odpowiadającym im 95-procentowym przedziałom ufności. Linia o jednostkowym nachyleniu przechodząca przez początek została również narysowana na tym samym rysunku. Zaobserwowano, że wszystkie punkty leżą bardzo blisko linii o jednostkowym nachyleniu, co jest zgodne z ogólnymi wnioskami wyciągniętymi w tabeli 3, tj. dla większości próbek średnie stężenie DO uzyskane za pomocą obu metod nie różni się statystycznie. Tak więc w większości przypadków pomiar DO metodą PM był równie dokładny jak pomiar DO metodą WM.
) dla każdej próbki, uzyskane odpowiednio przez WM i PM zostały wykreślone względem siebie na Rys. 2. Słupki błędów pokazane na rysunku odpowiadają odpowiadającym im 95-procentowym przedziałom ufności. Linia o jednostkowym nachyleniu przechodząca przez początek została również narysowana na tym samym rysunku. Zaobserwowano, że wszystkie punkty leżą bardzo blisko linii o jednostkowym nachyleniu, co jest zgodne z ogólnymi wnioskami wyciągniętymi w tabeli 3, tj. dla większości próbek średnie stężenie DO uzyskane za pomocą obu metod nie różni się statystycznie. Tak więc w większości przypadków pomiar DO metodą PM był równie dokładny jak pomiar DO metodą WM.
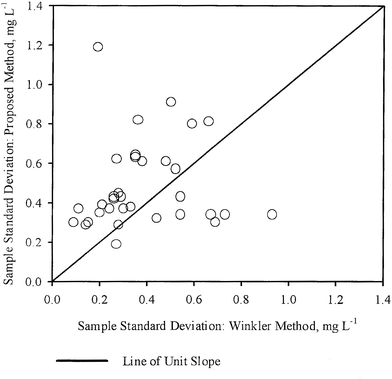
Odchylenia standardowe próbek (S1,S2) dla każdej próbki, uzyskane odpowiednio przez WM i PM, zostały wykreślone względem siebie na Rys. 3. Na tym samym rysunku narysowano również linię o jednostkowym nachyleniu przechodzącą przez początek. W tym przypadku punkty wydają się być rozproszone dość równomiernie w stosunku do linii o jednostkowym nachyleniu, przy czym niektóre punkty znajdują się blisko linii, podczas gdy inne są od niej bardziej oddalone. Obserwacje te są również ogólnie zgodne z wnioskami wyciągniętymi z tabeli 3, tj. w przypadku większości próbek zmiany stężenia DO mierzonego dwiema metodami nie różnią się statystycznie. Tak więc w większości przypadków pomiar DO metodą PM był równie dokładny jak pomiar DO metodą WM.
Stwierdzono, że przy starannym postępowaniu z próbką i miareczkowaniu, proponowana metoda (PM) może dawać wyniki porównywalne z metodą Winklera (WM) zarówno pod względem dokładności jak i precyzji. Niemniej jednak, dokładność oznaczania DO metodą PM może być prawdopodobnie zwiększona poprzez zastosowanie mikrostrzykawki o mniejszej liczbie najmniejszych cząstek do końcowego miareczkowania. Mikrostrzykawka użyta w tym badaniu miała najmniejszą liczbę 5 μL, co odpowiada niepewności na poziomie ∼0.25 mg L-1 DO w warunkach tego badania. Niepewność ta może być obniżona przez użycie mikrostrzykawki z niższą liczbą najmniejszych zliczeń.
Wnioski
Celem tego badania było opracowanie dokładnej, taniej, prostej i szybkiej metody pomiaru DO w małych objętościach próbek. Na podstawie przedstawionych wyników i analiz można stwierdzić, że zaproponowana metoda rozwiązuje większość z powyższych problemów. Główne wnioski z przeprowadzonych badań są następujące:
➢ Wprowadzenie izolacyjnej warstwy n-heksanu w celu zapobiegania przenoszeniu tlenu pomiędzy próbką wodną a atmosferą skutkuje spójnym i dokładnym oznaczaniem DO w małych objętościach próbek. Jest to główna innowacja wprowadzona do proponowanej metody.
➢ Wykazano również, że przy zastosowaniu odpowiednich środków ostrożności, proponowana metoda (PM) może generalnie dawać wyniki, które są statystycznie porównywalne z wynikami uzyskanymi metodą Winklera (WM), zarówno w odniesieniu do średniego stężenia DO, jak również w odniesieniu do wariancji stężenia DO wokół średniej.
➢ Wymagania dotyczące odczynników i szkła w przypadku proponowanej metody są mniejsze niż w przypadku metody Winklera, głównie ze względu na mniejszą objętość wykorzystywanej próbki. n-heksan jest jedynym dodatkowym wykorzystywanym odczynnikiem, ale niewielka ilość (∼1,5 mL na próbkę) wymaganego n-heksanu ma nieistotny wpływ na ogólny koszt analizy próbki.
W związku z tym proponowana metoda (PM) może być wykorzystywana do pomiarów DO we wszystkich okolicznościach, w których obecnie stosowana jest metoda Winklera. Proponowana metoda jest szczególnie przydatna w okolicznościach, w których metoda Winklera nie może być stosowana ze względu na ograniczenia w dostępnej objętości próbki.
.