Bilateral whole lung lavage in pulmonary alveolar proteinosis – A retrospective study
Introduction
Pulmonary Alveolar Proteinosis (PAP) is a rare diffuse lung disease with three clinical forms, congenital, nabytą (idiopatyczną) i wtórną, charakteryzującą się nagromadzeniem dużych ilości materiału fosfolipoproteinowego w pęcherzykach płucnych w wyniku niedoboru aktywności czynnika stymulującego tworzenie kolonii granulocytów-makrofagów (GM-CSF)1-14 (ryc. 1). 1). Wiąże się to z nieprawidłową funkcją makrofagów i upośledzeniem klirensu surfaktantu z płuc. Częstość występowania PAP wynosi 3,7 przypadków na milion, przeważają mężczyźni (stosunek 4:1 między mężczyznami a kobietami), a 80% przypadków odnotowuje się w trzeciej i czwartej dekadzie życia.6
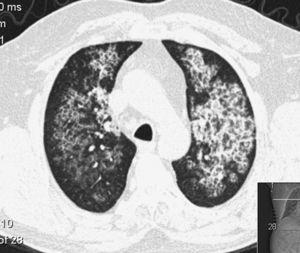
CT Scan of a patient with Pulmonary Alveolar Proteinosis. Zwracają uwagę pogrubiałe przegrody międzypęcherzykowe w obrębie zmętniałego miąższu, tworzące wzór „szalonego bruku”.
Whole Lung Lavage (WLL), wprowadzone w latach 60-tych,3,4,7,10,15 jest nadal złotym standardem leczenia.6 Najczęściej wykonuje się jednostronny WLL, polegający na płukaniu każdego płuca w różnych sesjach, oddzielonych od siebie dniami/tygodniami. Jednak obustronne sekwencyjne WLL w tej samej sesji leczenia jest atrakcyjną alternatywą, ponieważ jest znacznie mniej czasochłonne, wiąże się z mniejszym dyskomfortem pacjenta i jest bardziej opłacalne.
Jego skuteczność przypisuje się nie tylko usuwaniu materiału lipoproteinowego z przestrzeni pęcherzykowych, ale także usuwaniu przeciwciał anty GM-CSF, makrofagów pęcherzykowych i komórek nabłonka typu II. Takie postępowanie terapeutyczne rozważa się w przypadku zgłaszanego przez chorego znacznego ograniczenia w codziennej aktywności i/lub stwierdzenia hipoksemii z pO2
60mmHg, P(A-a) O2 ≥40mmHg i frakcją shunt ≥10%.12
W naszym szpitalu pierwszą WWL wykonaliśmy w 2010 roku, a po pięciu jednostronnych WLL przeszliśmy do programu sekwencyjnych obustronnych WWL.
Celem niniejszego doniesienia jest opisanie techniki obustronnej WLL oraz omówienie jej bezpieczeństwa i skuteczności.
Metody
W tym retrospektywnym badaniu zebraliśmy dane demograficzne i kliniczne z raportów medycznych trzech dorosłych pacjentów. Zastosowaną standardową techniką była zmodyfikowana wersja protokołu techniki Royal Brompton Hospital (Londyn).6,10
Przez cały czas trwania procedury stale monitorowano elektrokardiografię, pulsoksymetrię (SatO2), inwazyjne ciśnienie tętnicze, ośrodkowe ciśnienie żylne (CVP), wydalanie moczu, kapnografię, objętość oddechową, indeks bispektralny (BIS) i temperaturę centralną, a co godzinę wykonywano badanie gazów krwi tętniczej (ABG). Wykonywano całkowite znieczulenie dożylne (TIVA), aby umożliwić kontrolę głębokości znieczulenia, niezależnie od zmian wentylacyjnych nieodłącznie związanych z zabiegiem. Kuraryzacja była utrzymywana przez cały czas trwania zabiegu. Wprowadzono lewą rurkę o podwójnym świetle (DLT), wybierając możliwie największy rozmiar, aby zapewnić izolację płuc i zwiększyć skuteczność wentylacji i WLL. Jej prawidłowe położenie potwierdzono w bronchoskopii fiberoskopowej, a ciśnienie w mankiecie mierzono, aby zapobiec kontralateralnemu przeciekowi z płynu płuczącego.11
Przez 5 min prowadzono wstępną oksygenację przy FiO2 równym 100%, aby zapewnić prawidłową denitrogenizację pęcherzyków płucnych i wyeliminować występowanie pęcherzyków powietrza, które mogłyby upośledzać usuwanie materiału lipoproteinowego z pęcherzyków. Rozpoczynano wentylację jednopłucną i sprawdzano izolację płuc. Chorzy byli wentylowani metodą ciśnieniowo-kontrolną, przy wartości ciśnienia poniżej 30cmH2O. Objętość soli fizjologicznej do podania obliczano na podstawie przedoperacyjnych pomiarów czynnościowej pojemności zalegającej (functional residual capacity – FRC). Objętość płuca prawego obliczano na podstawie 3/5 FRC, a płuca lewego na podstawie 2/5 FRC (w pierwszym cyklu podawano mniejszą objętość). Sól fizjologiczną należy wstrzykiwać pod wpływem siły grawitacji z wysokości nieprzekraczającej 40 cm powyżej linii środkowo-osiowej, aby zapobiec barotraumie i przeciekowi do wentylowanego płuca.10 Chociaż w niektórych doniesieniach opisywano ułożenie w pozycji leżącej na boku pod kątem 30° w celu zachowania stosunku wentylacji do perfuzji zależnego wentylowanego płuca, zwiększa to prawdopodobieństwo zalania płuca kontralateralnego, dlatego preferowaliśmy ułożenie w pozycji leżącej na grzbiecie, z odwróconym trendelenburga, jak również w pozycji trendelenburga w celu ułatwienia grawitacyjnego podawania i usuwania ciepłej soli fizjologicznej z płuc.6,11 Pozycję tę przyjęto w przypadku wykonywania obustronnej WLL (ryc. 2).
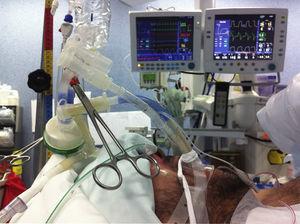
Techniczne przedstawienie WLL.
Gdy wypływ, początkowo mleczny, stał się mniej gęsty, drenaż przerwano w połowie objętości, a kilka cykli wentylacji ręcznej przy użyciu zastawki CPAP z ograniczeniem ciśnienia do 5-10 mmHg („modyfikacja Bingissera”) pozwoliło na ręczne udrażnianie pęcherzyków płucnych. Ten manewr znacznie zwiększa klirens lipoproteinowy.12,14 Cykl płukania powtarzano do momentu, aż wypływ płynu stanie się klarowny (ryc. 3). Ponieważ podczas zabiegu objętość wypłukiwanego płynu jest duża, istnieje duże ryzyko hipotermii. Zachowanie temperatury ciała jest kluczowe i powinno być utrzymywane przy użyciu podgrzewanego płynu do płukania o temperaturze 37°C i koca ogrzewającego.

Ewolucja mlecznego płynu w trakcie zabiegu.
Po skutecznym wypłukaniu pierwszego płuca, starannie je odessano i wykonano jego ponowną ekspansję, początkowo wentylację obustronną, a następnie jednostronną. Po 1 h wentylacji sprawdzano podatność płuc i dane z analizy gazowej krwi. Jeśli płukane płuco mogło zabezpieczyć potrzeby wymiany gazowej pacjenta, rozpoczynano kontralateralną WLL, powtarzając opisane powyżej procedury.8
Po zakończeniu zabiegu resztki soli fizjologicznej aspirowano przez bronchoskopię fibroskopową i wznawiano wentylację obustronną. Następnie rurkę o podwójnym świetle zastąpiono rurką dotchawiczą, a pacjenta przeniesiono na oddział wybudzeniowy w celu całonocnego monitorowania.
Wyniki
Obustronną WWL wykonano u trzech dorosłych pacjentów, 2 mężczyzn i 1 kobiety, w średnim wieku 43,6 lat (zakres 39 – 47 lat) (Tabela 1), u wszystkich z hipoksją w spoczynku poniżej 60 mmHg.
Ilość roztworu soli wstrzykniętego i zatrzymanego w obustronnej WWL.
| Płuca | Objętość (L) płuca prawego | Objętość (L) płuca lewego | ||
| Wstrzyknięta volume (L) | Positive balance (mL) | Instilled volume (L) | Positive balance (mL) | |
| 1st | 9.2 | 470 | 11.8 | 510 |
| 2nd | 15.3 | 530 | 10.7 | 450 |
| 3rd | 14.0 | 600 | 10,8 | 550 |
| 4. | 13,5 | 500 | 10,6 | 350 |
| 5. | 15.5 | 930 | 11.1 | 480 |
| 6-ta | 15.5 | 820 | 15.3 | 900 |
Pierwszym pacjentem był mężczyzna, lat 39, palacz tytoniu, piekarz, u którego rozpoznano PAP miesiąc przed pierwszą WLL na podstawie obrazu klinicznego, radiologicznego i BAL oraz obecności przeciwciał GM-CSF w surowicy. W chwili rozpoznania choroby u chorego występowała niewydolność oddechowa połączona z rozległym obustronnym zajęciem płuc obserwowanym w badaniu HRCT. Wykonano obustronną WLL, podając 9,2 i 11,8 l roztworu soli fizjologicznej odpowiednio do prawego i lewego płuca. Po krótkim okresie poprawy klinicznej, czynnościowej i radiologicznej nastąpiło pogorszenie stanu chorego z rozprzestrzenieniem się radiologicznych zmian w płucach i niewydolnością oddechową. To pogorszenie kliniczne zbiegło się w czasie z jego powrotem do pracy. W rzeczywistości mąkę piekarską opisywano jako potencjalny czynnik wyzwalający.16 Trzy miesiące później wykonano drugą obustronną WLL, a następnie podano 15,3 i 10,7 l roztworu soli fizjologicznej. Po tym zabiegu i zaprzestaniu pracy w poprzednim środowisku chory utrzymywał stabilność kliniczną.
Drugi pacjent poddany WLL to kobieta w wieku 47 lat, rolnik, niepaląca, bez chorób współistniejących, u której miesiąc przed pierwszą WLL rozpoznano PAP na podstawie obrazu klinicznego, radiologicznego i BAL oraz obecności przeciwciał GM-CSF w surowicy. Obraz kliniczny był bardzo podobny jak u pierwszego pacjenta, z dusznością przy wysiłku i suchym kaszlem związanym z niewydolnością oddechową oraz szerokimi, obustronnymi, szalonymi ogniskami brukowymi w badaniu HRCT. Po postawieniu diagnozy wykonano WLL z podaniem 14 i 10,8 l soli fizjologicznej odpowiednio do prawego i lewego płuca. Po krótkotrwałej początkowej poprawie klinicznej pacjentka została poddana kolejnej WLL 1,5 miesiąca później, ponieważ nasiliły się objawy i wzrosło paO2
60mmHg. Podczas tej procedury do prawego i lewego płuca podano łącznie 13,5L i 10,6L. Cztery miesiące później z powodu pogorszenia stanu klinicznego wykonano trzeci zabieg WLL, podczas którego do prawego i lewego płuca podano 15,5L i 11,1L (ryc. 4). Po tym zabiegu chory osiągnął stabilność kliniczną, czynnościową i radiologiczną.

Sequential samples of bilateral WLLs.
Trzecim włączonym pacjentem był mężczyzna, lat 45, były palacz, pracownik fabryki opon, z rozpoznaniem PAP podczas oceny i leczenia ropnia mózgu wywołanego przez nocardię. Podobnie jak w przypadku dwóch pozostałych pacjentów, rozpoznanie ustalono na podstawie typowych cech radiologicznych i BAL związanych z obecnością przeciwciał GM-CSF w surowicy. Jednak dwa lata wcześniej u pacjenta wykonano badanie HRCT klatki piersiowej z obustronnym obrazem szalonego brukowania. Po roku od rozpoznania nasiliły się objawy, wystąpiła duszność wysiłkowa i niewydolność oddechowa (paO2-57 mmHg), w związku z czym poddano go WLL z podaniem 15,5 i 15,3 soli fizjologicznej odpowiednio do prawego i lewego płuca. Po tym zabiegu uzyskano znaczną poprawę kliniczną, czynnościową i radiologiczną.
Wszystkie sześć zabiegów WLL przeprowadzono zgodnie z ustalonym protokołem i bez większych powikłań.
Godzinne monitorowanie gazometryczne koncentrowało się na zapewnieniu prawidłowej oksygenacji i wentylacji. Wartości gazometryczne pacjentów były łatwo utrzymywane podczas całego zabiegu, z pCO2 poniżej 55 mmHg i SpO2 utrzymywanym powyżej aktualnych wartości własnych pacjentów, mimo że znajdowali się oni w pozycji leżącej (tab. 2) (ryc. 5). Istotnie, u wszystkich obustronnie poddanych WWL pacjentów obserwowaliśmy postępującą instalację kwasicy metabolicznej podczas zabiegu. Ta kwasica metaboliczna została odwrócona w pierwszych godzinach pooperacyjnych i nie zidentyfikowano po tym żadnych chorób współistniejących.
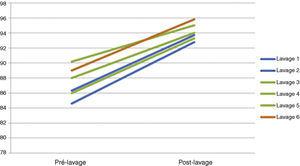
Ewolucja pomiaru SatO2 w trakcie wykonywania Whole Lung Lavages.
Przy zastosowaniu manewru Bingissera obserwowaliśmy przejściowe trudności w odzyskaniu objętości płukania (przyczyniające się do dodatniego bilansu płynów), ale wyraźny wzrost gęstości płukania.
W każdym przypadku obserwowaliśmy epizod kontralateralnego wynaczynienia płukania. Podczas wszystkich zabiegów temperatura ciała utrzymywana była w granicach 36-37°C. Średni czas zabiegu wynosił 8 godzin (zakres 7h32-9h41).
Czas do ekstubacji zmieniał się w zależności od rozwoju sytuacji klinicznej i analizy gazometrycznej krwi, a wszyscy pacjenci zostali skutecznie ekstubowani po 18 godzinach.
Po tych zabiegach zdolność funkcjonalna i codzienna aktywność wszystkich pacjentów uległy znacznej poprawie, udokumentowanej objawami klinicznymi, jak również testami czynności oddechowej i danymi gazometrycznymi.
Dyskusja
W tym krótkim komunikacie opisaliśmy sześć obustronnych sekwencyjnych zabiegów WLL, wykonanych u trzech pacjentów z PAP, potwierdzając ich skuteczność kliniczną i bezpieczeństwo.
Pomimo znacznej inwazyjności, WLL pozostaje zalecaną metodą leczenia PAP i jak dotąd jest jedyną terapią o ustalonej skuteczności. W rzeczywistości, gdy pacjent z PAP zgłasza się z niewydolnością oddechową i rozległymi zmianami w obrazie HRCT, procedura ta jest obowiązkowa. WLL jest techniką kosztowną i czasochłonną, wymagającą wielodyscyplinarnego podejścia, co w połączeniu z rzadkością występowania PAP wyjaśnia, dlaczego procedura ta jest wykonywana tylko w nielicznych ośrodkach. Wybór obustronnej WLL oznacza lepszy komfort pacjenta, redukcję kosztów i czasu oraz utrzymanie skuteczności klinicznej.
Trzy włączone do badania pacjentki można uznać za typowe przypadki PAP, choć istniały pewne różnice. Dwóch z nich miało ostrą postać choroby i wymagało WLL po postawieniu diagnozy, podczas gdy drugi został poddany tej procedurze w trakcie trwania choroby. Podczas gdy ten trzeci pacjent musiał być poddany tylko jednemu WLL, pozostali dwaj musieli mieć wielokrotne WLL, a dokładnie dwie i trzy procedury.
Kluczowym czynnikiem umożliwiającym przystąpienie do drugiego płukania płuca jest to, czy wentylacja pierwszego płukanego płuca odzyskała wystarczającą pojemność, aby zapewnić potrzeby pacjenta. Z tego powodu, jeśli nie ma przewagi bocznej, do pierwszego płukania wybieramy większe płuco – prawe. Aby zapobiec barotraumie, maksymalne ciśnienie wdechowe ograniczano do 30cmH2O. We wszystkich procedurach, po 1 godzinie wentylacji, podatność płuc i wartości gazometryczne w jednopłucnej wentylacji płukanego płuca były zgodne z początkiem płukania drugiego płuca.
Wybór wentylacji kontrolowanej ciśnieniem pozwolił nam na ciągłe monitorowanie zmian podatności płuc podczas płukania i zapobiegł ewentualnemu przemieszczeniu się rurki lub innym zakłóceniom. Ponadto, w ten sam sposób, pozwoliło to na obserwację powrotu podatności płuc po płukaniu.
Ułożenie pacjenta w pozycji leżącej nie utrudniało utlenowania, dzięki czemu nie musieliśmy uciekać się do pozycji bocznej odleżynowej z wentylacją płuca zależnego, która jest mniej stabilna i wiąże się z większym ryzykiem w przypadku długiej procedury (średnio 8 godzin).
Manewr Bingissera wybraliśmy ze względu na fakt, że ciśnienie wywierane na drogi oddechowe jest mierzone, w przeciwieństwie do manewrów kinezyterapii, gdzie taka kwantyfikacja jest niemożliwa, co zmniejsza ryzyko nadmiernego ciśnienia przy wstrząsach, unikając i zapobiegając ewentualnej kontralateralnej inundacji.8
Próbując odwrócić kwasicę metaboliczną obserwowaną podczas zabiegów, surowica podtrzymująca stosowana w okresie okołooperacyjnym – chlorek sodu 0,9% – została zastąpiona mleczanem Ringera w trzeciej procedurze obustronnej i później, z jedynie skromną poprawą. W piśmiennictwie nie ma wzmianki o stosowaniu tego rozpuszczalnika jako płynu do płukania płuc, dlatego chlorek sodu pozostaje w użyciu.
Podsumowując, biorąc pod uwagę skuteczność kliniczną obustronnej WLL, jej zalety w postaci oszczędności czasu i kosztów oraz zmniejszenia dyskomfortu pacjenta, czynią tę technikę odpowiednim pierwszym wyborem w płukaniu terapeutycznym u pacjentów z PAP.
Ujawnienia etyczneOchrona ludzi i zwierząt
Autorzy oświadczają, że zastosowane procedury były zgodne z przepisami odpowiedniej komisji etyki badań klinicznych oraz z przepisami Kodeksu Etycznego Światowego Stowarzyszenia Medycznego (Deklaracja Helsińska).
Poufność danych
Autorzy oświadczają, że postępowali zgodnie z protokołami swojego ośrodka pracy dotyczącymi publikacji danych pacjentów.
Prawo do prywatności i świadoma zgoda
Autorzy oświadczają, że w tym artykule nie pojawiają się dane pacjentów.
Konflikt interesów
Autorzy nie mają konfliktu interesów do zgłoszenia.
.