Pain in Motion
Giovedì 18 gennaio, stavo guardando il giornale e la testata dell’ultima notizia sportiva leggeva: “La carriera di calciatrice finisce dopo una commozione cerebrale: mancava una ‘buona guida’”. Una giocatrice di calcio olandese ha ricevuto una palla contro la sua testa e poco sapeva che la palla contro la sua testa avrebbe cambiato la sua vita per sempre. Nel 2008 ha subito sia una commozione cerebrale che un colpo di frusta. Tuttavia, ha continuato a giocare, ma dopo qualche giorno i suoi disturbi sono rimasti. Al club ha allarmato il suo allenatore e lo staff medico. Troppo tardi, a quanto pare. Non ha recuperato secondo le aspettative, costringendola a seppellire i suoi sogni e a porre fine alla sua carriera.
Sia la commozione cerebrale che il colpo di frusta sono una causa significativa di morbilità, con molti sopravvissuti che affrontano difficoltà persistenti per anni dopo l’infortunio. Nella maggior parte dei casi, il recupero completo è previsto entro 3 mesi dopo la commozione cerebrale/il colpo di frusta. Tuttavia, non tutti i pazienti sperimentano un recupero così rapido. Fino al 15% dei pazienti con diagnosi di commozione cerebrale e fino al 50% dei pazienti con diagnosi di colpo di frusta continuano a sperimentare sintomi disabilitanti persistenti (Marshall et al, 2015; De Kooning et al, 2015). Un certo numero di fattori influenzano il tasso e la portata del recupero è come il meccanismo e l’impostazione per la lesione iniziale. Sterling 2014 ha presentato fattori prognostici che mostrano prove coerenti per il recupero povero dopo il colpo di frusta. In entrambe le lesioni, una diagnosi corretta è un passo critico nella gestione di successo che porta a risultati migliori e un ritardo potenziale diminuito nel recupero. Tuttavia, la diagnosi di queste lesioni è spesso difficile per il professionista e frustrante per il paziente.
In questo blogpost, ho fatto un confronto tra la sindrome post-concussiva (PCS) e il disturbo associato al colpo di frusta (WAD), nel tentativo di rispondere alla domanda che mi è venuta in mente: “È chiaro per il medico come fare una diagnosi corretta di PCS e WAD?”

Prima ancora di cercare una risposta a questa domanda, mi sono posto un’altra domanda. Esiste già una definizione chiara di PCS e WAD?
All’intorno della definizione di PCS c’è molta confusione. L’Ontario Neurotrauma Foundation Guideline for Concussion/Mild Traumatic Brain Injury & Persistent Symptoms (2nd edition, 2008) afferma: “Proprio come c’è confusione intorno alla definizione di lesione cerebrale traumatica lieve, questo è anche il caso della definizione di PCS”. Mentre Voormolen et al, 2018 hanno dichiarato che: “È impegnativo definire la PCS perché non c’è consenso per quanto riguarda i criteri di diagnosi. I criteri più utilizzati per la diagnosi sono quelli specificati nella Classificazione internazionale delle malattie (ICD-10) e nel Manuale diagnostico e statistico dei disturbi mentali (DSM-IV).”
La PCS è meglio definita come: la persistenza di tre o più sintomi per 4 settimane (ICD-10), o 3 mesi (Manuale Diagnostico e Statistico dei Disturbi Mentali – DSM IV), dopo una commozione cerebrale – una forma lieve di lesione cerebrale traumatica.
Criteri diagnostici della PCS come offerti dall’ICD-10:
- Storia di trauma cranico con perdita di coscienza che precede la comparsa dei sintomi di un massimo di 4 settimane.
- Sintomi in 3 o più delle seguenti categorie di sintomi
- Mal di testa, vertigini, malessere, affaticamento, intolleranza al rumore
- Irritabilità, depressione, ansia, labilità emotiva
- Concentrazione soggettiva, memoria, o difficoltà intellettuali senza prove neuropsicologiche di una compromissione marcata
- Insonnia
- Ridotta intolleranza all’alcool
- Preoccupazione per i sintomi di cui sopra e paura di danni cerebrali con preoccupazione ipocondriaca e adozione del ruolo di malato
La definizione di WAD è più chiara della definizione di PCS?
La Task Force del Quebec ha sviluppato delle raccomandazioni riguardanti la classificazione e il trattamento del WAD, che sono state utilizzate per sviluppare una guida per la gestione del colpo di frusta 1995. In questa guida Spitzer e colleghi, 1995 hanno definito il colpo di frusta come: lesioni ossee o dei tessuti molli derivanti da un impatto posteriore o laterale, principalmente negli incidenti automobilistici, e da altri incidenti come risultato di un meccanismo di accelerazione-decelerazione di trasferimento di energia al collo. L’impatto può portare a una varietà di manifestazioni cliniche chiamate WAD. In questo caso, credo si possa dire che manca ancora una definizione univoca per la WAD.
Diagnosi di PCS vs WAD
Il fatto che sia difficile definire la PCS e la WAD, rende difficile anche la diagnosi. Inoltre, molte controversie riguardanti la diagnosi di PCS e WAD esistono a causa di 1) la grande varietà nel numero di pazienti che riportano lesioni, 2) l’incapacità in molti casi di trovare prove diagnostiche certe di lesioni e 3) gli studi che esaminano PCS e WAD, che hanno riportato segni significativi e sovrapposizione dei sintomi con altre diagnosi che possono risultare come conseguenza di un’esperienza traumatica, per esempio, disturbo da stress post-traumatico e cefalea post-traumatica. I pazienti con WAD hanno riportato segni e sintomi che appaiono sorprendentemente simili a quelli sperimentati nella PCS, con l’eccezione di alcune differenze chiave (cioè i sintomi radicolari) (Tabella 1).
Ecco dove la scarpa si blocca. Sia la diagnosi di PCS che quella di WAD sono cambiate poco negli ultimi tempi e rimangono piuttosto cliniche (Sterling 2014). La diagnosi di WAD è fatta sul meccanismo della lesione e sui sintomi riportati dal paziente – dolore al collo e sintomi correlati a seguito di un evento traumatico, di solito un incidente stradale. La diagnosi di PCS si basa su una costellazione di sintomi comunemente sperimentati a seguito di una lieve lesione cerebrale traumatica. Non ci sono test neuropsicologici specifici che possono diagnosticare PCS o WAD (Marshall et al, 2015; Rodriquez et al, 2004). Inoltre, nel caso del WAD, le attuali linee guida cliniche raccomandano che l’imaging radiologico dovrebbe essere intrapreso solo per rilevare il WAD di grado IV (cioè, frattura o dislocazione) e che i clinici dovrebbero aderire alla regola canadese C-Spine o alla regola di Nexus quando prendono la decisione di riferire il paziente per un esame radiografico (Nikles et al, 2017).
Quindi, è molto difficile per gli operatori differenziare tra PCS e WAD ed eseguire una diagnosi corretta. Devono fare molto affidamento sui segni e sintomi riferiti dal paziente, che, come menzionato in precedenza, mostrano una significativa sovrapposizione (Tabella 1) e sono anche comuni nelle popolazioni normali (Iverson & Lange, 2003). Inoltre, le indagini dei medici di base in Canada (Ferrari et al, 2004) e in Australia (Brijnath et al, 2016) hanno dimostrato che i medici di base spesso mancano di conoscenze sulla WAD e di fiducia nella diagnosi e nella gestione delle lesioni. Formare ed educare i medici generici ha il potenziale per ridurre l’imaging non necessario per la WAD e ottimizzare la diagnosi e il rinvio precoce dei pazienti a rischio di recupero ritardato.
A prescindere dalla diagnosi formale (ad esempio, PCS contro WAD), i sintomi dopo la commozione cerebrale/il colpo di frusta hanno il potenziale per causare limitazioni e devono essere affrontati in modo coordinato e diretto al fine di assistere il recupero. È obbligatorio misurare il dolore e la disabilità come primo passo della valutazione clinica a causa della loro consistente capacità prognostica. Per le lesioni da colpo di frusta, le misure di dolore raccomandate dalle linee guida includono la scala analogica visiva a 11 punti o la scala di valutazione numerica, e la misura di disabilità raccomandata è il Neck Disability Index per le sue proprietà clinimetriche (Nikles et al, 2017). Tuttavia, anche altre misure sono accettabili, e alcune includono il Whiplash Disability Questionnaire e la Patient Specific Functional Scale (Nikles et al, 2017). Un valido strumento di valutazione per la commozione cerebrale è il Rivermead Concussion Symptoms Questionnaire
È anche importante notare che c’è spesso un’interazione di sintomi, circostanze sociali e successivo sviluppo di complicazioni (ad esempio, ansia, stress) che possono complicare e influenzare negativamente il recupero. Il particolare gruppo di sintomi varierà tra i pazienti, rendendo necessario un approccio individualizzato alla gestione.
Dite la vostra:
“I fisioterapisti devono assumere un ruolo maggiore nel piano di cura generale del paziente con disturbo associato al colpo di frusta o sindrome post-concussiva? Questo significherebbe avere esperienza nella valutazione dei fattori di rischio e una comprensione di quando sono necessari trattamenti aggiuntivi come farmaci e interventi psicologici.”
Votate: https://goo.gl/X5NpQr
Risultati: https://goo.gl/3KVK3K
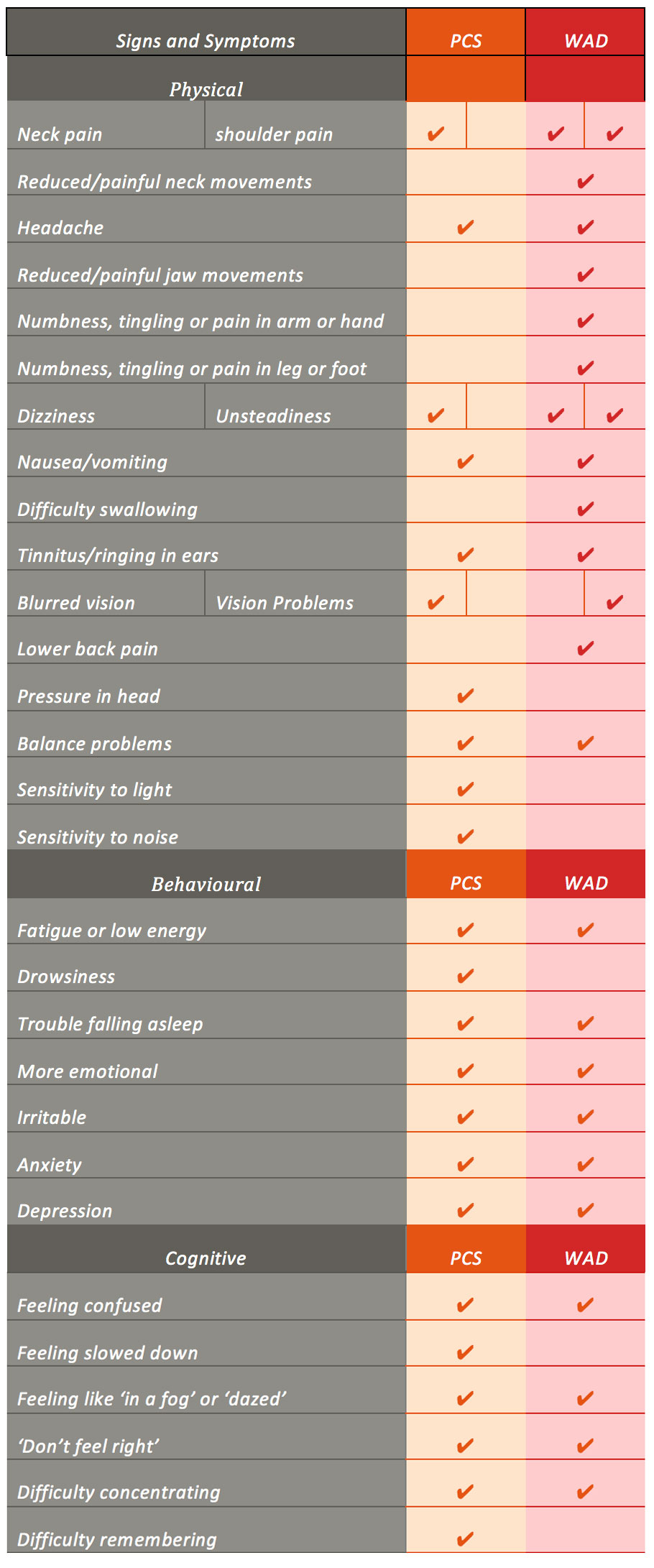
Tabella 1. Un confronto tra segni e sintomi di PCS e WAD. dal punteggio dei sintomi post-concussivi del Sideline Concussion Assessment Tool versione 3 (SCAT-3), il WAD Form C della Quebec Task Force for Whiplash Associated Disorder (Spitzer et al, 1995) e i risultati delle revisioni sistematiche su PCS e WAD.
Ward Willaert
Ward Willaert è un ricercatore di dottorato alla Vrije Universiteit Brussel (Bruxelles, Belgio) e all’università di Ghent (Ghent, Belgio). Fa parte del gruppo di ricerca Pain in Motion e il suo interesse clinico e di ricerca si estende al dolore cronico “inspiegabile”, ai disturbi associati, alla diagnosi e al trattamento del dolore (cronico). Ha un interesse speciale per i disturbi associati al colpo di frusta e il sistema nervoso centrale.
2018 Pain in Motion
Riferimenti e ulteriori letture:
Marshall, S. et al. Linee guida aggiornate di pratica clinica per la concussione/lesione cerebrale traumatica lieve e sintomi persistenti. Brain Inj. 29, 688-700 (2015).
https://www.ncbi.nlm.nih.gov/pubmed/25871303
Kooning, M. De et al. L’inibizione endogena del dolore non è correlata alle risposte autonomiche nei disturbi acuti associati al colpo di frusta. 52, 431-440 (2015).
https://www.ncbi.nlm.nih.gov/pubmed/26348457
Sterling, M. Gestione fisioterapica dei disturbi associati al colpo di frusta (WAD). J. Physiother. 60, 5-12 (2014).
https://www.ncbi.nlm.nih.gov/pubmed/24856935
Voormolen, D. C. et al. Divergent Classification Methods of Post-Concussion Syndrome after Mild Traumatic Brain Injury: Tassi di prevalenza, fattori di rischio e risultati funzionali. J. Neurotrauma neu.2017.5257 (2018). doi:10.1089/neu. 2017 .5257
https://www.ncbi.nlm.nih.gov/pubmed/29350085
Bigler ED. Neuropsicologia e neuroscienze cliniche della sindrome post-concussiva persistente. 14, 1-22 (2008)
https://www.ncbi.nlm.nih.gov/pubmed/18078527
Spitzer, W. O. et al. Monografia scientifica della Quebec Task Force on Whiplash-Associated Disorders: ridefinire il “colpo di frusta” e la sua gestione. Spine (Phila. Pa. 1976). 20, 1S-73S (1995)
https://www.ncbi.nlm.nih.gov/pubmed/7604354
Rodriquez, A. A., Barr, K. P. & Burns, S. P. Whiplash: Pathophysiology, diagnosis, treatment, and prognosis. Muscle Nerve 29, 768-781 (2004).
https://www.ncbi.nlm.nih.gov/pubmed/15170609
Nikles, J., Yelland, M., Bayram, C., Miller, G. & Sterling, M. Management of Whiplash Associated Disorders in Australian general practice. BMC Musculoskelet. Disord. 18, 551 (2017)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5747169/
Iverson, G. L. & Lange, R. T. Examination of “Postconcussion-Like” Symptoms in a Healthy Sample. Appl. Neuropsychol. 10, 137-144 (2003)
https://www.ncbi.nlm.nih.gov/pubmed/12890639
Ferrari, R. & Russell, A. S. Survey of general practitioner, family physician, and chiropractor’s beliefs regarding the management of acute whiplash patients. Spine (Phila. Pa. 1976). 29, 2173-7 (2004).
https://www.ncbi.nlm.nih.gov/pubmed/15454712
Brijnath, B. et al. General practitioners knowledge and management of whiplash associated disorders and post-traumatic stress disorder : implications for patient care. BMC Fam. Pract. 1-11 (2016).
https://bmcfampract.biomedcentral.com/articles/10.1186/s12875-016-0491-2