Modifica del metodo di Winkler per la determinazione della concentrazione di ossigeno disciolto in piccoli volumi di campione
Pubblicato il 27 agosto 2010
Il metodo di Winkler è la procedura più popolare per la determinazione della concentrazione di ossigeno disciolto (DO) in campioni di acqua. Tuttavia, questo metodo richiede un volume di campione relativamente grande di 200 mL per una determinazione accurata del DO. Molti metodi alternativi sono stati proposti per misurare le concentrazioni di DO in piccoli volumi di campione, ma la maggior parte di questi metodi hanno problemi di bassa precisione, costi elevati, strumentazione complicata o tempi di analisi lunghi. In questo articolo, viene proposta una semplice modifica al metodo di Winkler per la misurazione delle concentrazioni di DO in campioni di 1 mL di volume. Il metodo proposto è accurato, a basso costo, semplice e veloce. Le concentrazioni di DO sono state misurate in 33 campioni sia con il metodo convenzionale di Winkler (WM) che con il metodo proposto (PM). Per 23 dei 33 campioni analizzati, l’ipotesi che le medie della popolazione delle misurazioni siano uguali (μ1 = μ2) non potrebbe essere rifiutata al livello di confidenza del 95% e per 19 campioni, l’ipotesi che le varianze della popolazione delle misurazioni siano uguali (σ21 = σ22) non potrebbe essere rifiutata all’intervallo di confidenza del 95%. Si è quindi concluso che, nella maggior parte dei casi, le misurazioni di DO tramite WM e PM danno risultati comparabili sia in termini di accuratezza che di precisione.
Introduzione
Il metodo di Winkler (metodo n. 4500-O-C)1 è stato universalmente accettato come un metodo accurato e affidabile2 per la misurazione della concentrazione di ossigeno disciolto (DO) in una varietà di campioni d’acqua. Questo metodo è considerato il punto di riferimento per la determinazione del DO. Tuttavia, lo svantaggio principale di questo metodo è il requisito di un grande volume di campione di 200 mL.3
Sono stati sviluppati anche numerosi metodi alternativi per la misurazione del DO. Questi metodi rientrano in tre categorie distinte: (1) metodi colorimetrici, (2) metodi che utilizzano la gascromatografia e (3) metodi che utilizzano sensori elettrochimici e ottici. I metodi colorimetrici possono essere usati per la determinazione del DO in piccoli volumi di campione. Tuttavia, soffrono di svantaggi come il requisito di reagenti chimici costosi (ad esempio, sol d’oro) o tossici (ad esempio, cianuro).4 La mancanza di un’adeguata giustificazione nella scelta della lunghezza d’onda di misurazione è un altro fattore limitante per tali metodi.5 La determinazione del DO è possibile anche utilizzando la gascromatografia. Tuttavia i metodi gascromatografici, anche se accurati e che richiedono piccoli volumi di campione, sono comunque lunghi e costosi. I sensori elettrochimici sono stati ampiamente utilizzati per la misurazione del DO e i loro vantaggi e svantaggi sono stati esaminati altrove.6 I sensori elettrochimici generalmente soffrono di effetti irreversibili della pressione, contaminazione da solfuro di idrogeno e sensibilità incrociata.7 Inoltre consumano DO durante la misurazione e quindi possono essere inadatti per volumi di campione molto piccoli. Recentemente ci si è concentrati sullo sviluppo di sensori ottici basati sul principio del quenching dinamico della luminescenza dell’ossigeno.8 Questi sensori ottici sono facili da usare, hanno tempi di risposta rapidi e sono durevoli. Tuttavia, tutti i sensori, sia elettrochimici che ottici, richiedono una calibrazione rispetto al metodo di Winkler a causa della sensibilità dei sensori alla temperatura e alla pressione.9,10 Sono anche sensibili al bio-fouling e alla crescita batterica sulla superficie del sensore.8
A causa delle limitazioni intrinseche dei metodi alternativi descritti sopra e della loro dipendenza dal metodo di Winkler per il controllo incrociato e la calibrazione, sono state proposte diverse modifiche al metodo di Winkler stesso per la misurazione delle concentrazioni di DO in volumi di campione di 1-10 mL.11,12,13 Tuttavia, tali metodi ‘Micro-Winkler’ non sono molto popolari a causa dei complessi requisiti strumentali e delle elaborate precauzioni richieste per evitare la contaminazione dei campioni attraverso scambi con ossigeno atmosferico. Questi metodi sono stati criticamente rivisti altrove.14 Un metodo di titolazione gravimetrica Micro-Winkler è stato recentemente proposto15 per la misura DO in piccoli campioni. Tuttavia, questa procedura richiede misure gravimetriche multiple e accurate utilizzando una bilancia sensibile e quindi sembra essere abbastanza complessa.
Sulla base della revisione della letteratura, sembra che quasi tutti i metodi sviluppati per le misure di DO in piccoli campioni siano carenti in un modo o nell’altro. Quindi c’è un continuo bisogno di sviluppare un metodo migliore, cioè accurato, preciso, a basso costo, semplice e veloce per la misurazione del DO in piccoli volumi di campione.
Sintesi del metodo proposto
La sfida principale nella misurazione delle concentrazioni di DO in piccoli campioni è la prevenzione della contaminazione dei campioni attraverso l’interazione con l’atmosfera. Si propone di introdurre uno strato di liquido isolante tra il campione d’acqua e l’atmosfera. Le proprietà richieste del liquido isolante sono: immiscibilità dell’acqua, densità inferiore a quella dell’acqua e capacità di dissoluzione dell’ossigeno trascurabile. Si propone che il liquido isolante sia preso in una fiala e che il campione d’acqua il cui DO deve essere determinato (1 mL di volume) sia introdotto direttamente sotto lo strato di liquido isolante. Il campione d’acqua è efficacemente sigillato dall’atmosfera attraverso questo passaggio. Il DO nel campione d’acqua può quindi essere fissato e convertito in una quantità equivalente di iodio utilizzando gli stessi reagenti usati nel metodo di Winkler. La soluzione di iodio viene poi estratta dalla fiala con una siringa e titolata con Na2S2O3 per la determinazione della concentrazione di DO nel campione.
Dopo diverse serie di prove, l’n-esano è stato scelto come liquido isolante come descritto sopra. L’n-esano è più leggero dell’acqua (peso specifico = 0,7) ed è praticamente immiscibile in acqua. La solubilità dell’ossigeno in n-esano è di 0,002 frazione molare,16 cioè, l’ossigeno è praticamente insolubile in n-esano.
Materiale e metodi
Tutti i reagenti usati erano di grado analitico reagente (>purezza 99%, Loba Chemicals, India). L’acqua deionizzata (Milli-Q, Millipore, USA) è stata usata per la preparazione dei reagenti e la diluizione dei campioni. L’n-esano utilizzato era di grado HPLC (>99% purezza, Merck, India). La vetreria in borosilicato è stata utilizzata in questo studio. MnSO4 e alcali-azide-ioduro soluzioni sono state preparate secondo i metodi standard (Metodo No. 4500-O C).1
La procedura di misurazione DO dal metodo proposto (PM) è stato il seguente. Inizialmente, 0,5 mL di n-esano sono stati trasferiti in una fiala di vetro da 16 mL (Wheaton Science, USA). Poi, 1 mL di n-esano è stato preso in una pipetta da 2 mL, e la pipetta è stata ulteriormente riempita con 1 mL del campione di acqua la cui concentrazione DO doveva essere determinata. La procedura di raccolta del campione di cui sopra assicurava che il campione fosse raccolto senza spazio di testa. Questa fase di raccolta del campione è la più cruciale, poiché la comparsa di qualsiasi bolla o spazio d’aria nell’interfaccia esano-acqua o altrove nella pipetta può portare a errori. La bocca della pipetta è stata quindi posizionata sotto lo strato di esano nella fiala e quindi il campione è stato introdotto sotto lo strato di esano, evitando qualsiasi contatto tra il campione e l’atmosfera. La raccolta del campione nella pipetta e l’applicazione del campione sotto lo strato di esano nella fiala deve essere fatta il più rapidamente possibile in modo da minimizzare gli errori. Successivamente, 5 μL di MnSO4 è stato introdotto nel campione di acqua sotto lo strato di esano utilizzando una micro siringa da 10 μL (Hamilton, USA), seguita da una simile aggiunta di 5 μL di soluzione di alcali-azide-ioduro. La formazione del precipitato è iniziata immediatamente dopo le aggiunte ed è stata completa entro 3 minuti. Successivamente, 0,1 mL di conc. H2SO4 è stato aggiunto utilizzando una micropipetta al precipitato formato sotto lo strato di esano. Il precipitato è stato dissolto entro 3 minuti e la soluzione di iodio giallo si è formata sotto lo strato di esano. Esattamente 1 mL della soluzione di iodio è stato estratto da sotto lo strato di esano utilizzando micro siringa e trasferito in un becher da 25 mL. La soluzione di iodio da 1 mL nel becher è stata diluita a ∼10 mL aggiungendo acqua deionizzata per facilitare la titolazione. L’aggiunta di acqua deionizzata diluisce semplicemente la soluzione di iodio, senza influenzare la quantità di iodio nel becher. Il contenuto del becher è stato titolato con una soluzione di Na2S2O3 0,00625 M. 1 mL di questo titolante corrisponde a 55,5 mg L-1 di DO nel campione originale. Il titolante è stato preso in una microsiringa da 250 μL (Hamilton, USA) e aggiunto goccia a goccia al becher con agitazione costante fino a quando il colore giallo dello iodio è stato quasi scaricato. Poi, sono state aggiunte 1-2 gocce di soluzione di amido e la titolazione è continuata fino a quando il colore blu dovuto all’amido è stato scaricato. In base al volume di titolante richiesto in una particolare titolazione, è stata calcolata la concentrazione di DO nel campione originale.
La concentrazione di DO è stata anche determinata in vari campioni usando il metodo di Winkler (WM). I requisiti dei reagenti e altri dettagli di entrambi i metodi sono presentati nella Tabella 1.
| Campione No. | Reagente | Quantità | Forte | ||
|---|---|---|---|---|---|
| WM | PM | WM | PM | ||
| Campione | 200 mL | 1 mL | – | – | |
| MnSO4 | 1 mL | 5 μL | Come per WM | ||
| Alkali-reagente azide-ioduro | 1 mL | 5 μL | Come per WM | ||
| Na2S2O3 | Come richiesto | Come richiesto | 0.025M | 0.00625M | |
| H2SO4 | 1 mL | 0.1 mL | Come per WM | ||
| Amido | 1-2 gocce | 1-2 gocce | Come per WM | ||
| n-Esano | Non usato | 1.5 mL | – | – | |
Risultati e discussione
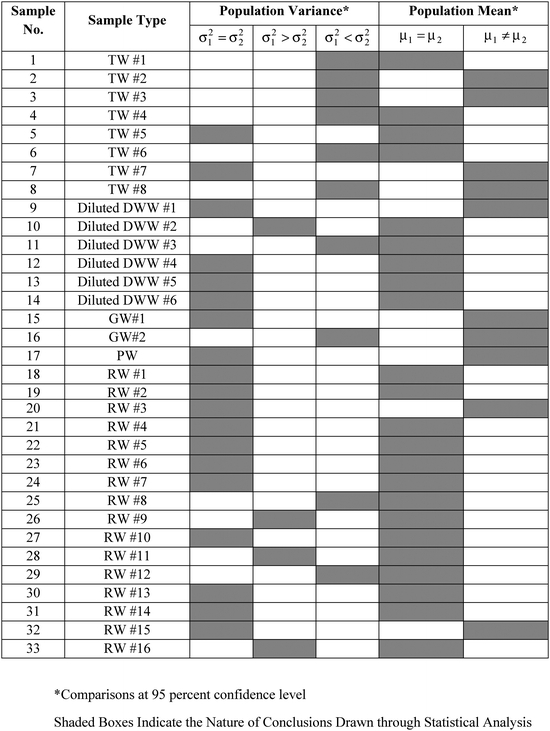
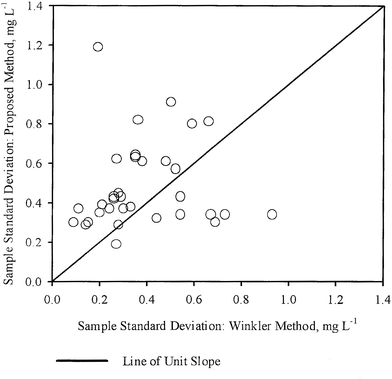
La concentrazione di DO è stata misurata in 33 campioni di acqua (vedi tabella 2) ottenuti da vari luoghi nella città di Kanpur, India e dintorni. Dei 33 campioni, 8 erano campioni di acqua di rubinetto, 16 erano campioni di acqua di fiume, 6 erano campioni di acque reflue domestiche diluite con acqua di rubinetto, 2 erano campioni di acqua freatica e 1 era un campione di acqua di stagno. I campioni sono stati scelti in modo che le concentrazioni di DO potessero essere misurate in un’ampia varietà di matrici di campioni. Per ogni campione, sono state effettuate diverse misurazioni DO in replica, sia dal WM che dal PM. Le medie del campione calcolate (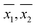 ), le deviazioni standard del campione (S1, S2) e il numero di misurazioni replicate (n1, n2) rispettivamente per il WM e il PM sono presentati nella tabella 2 per ogni campione.
), le deviazioni standard del campione (S1, S2) e il numero di misurazioni replicate (n1, n2) rispettivamente per il WM e il PM sono presentati nella tabella 2 per ogni campione.
I tracciati normali delle serie di misurazioni replicate con entrambi i metodi erano tutti approssimativamente lineari, indicando che le misurazioni replicate erano distribuite normalmente e quindi erano suscettibili di ulteriori analisi statistiche su tale base. A scopo illustrativo, i grafici normali per cinque misurazioni del campione eseguite dal WM sono presentati in Fig. 1A. I grafici normali per le stesse misurazioni di cinque campioni eseguite dal PM sono presentati in Fig. 1B.
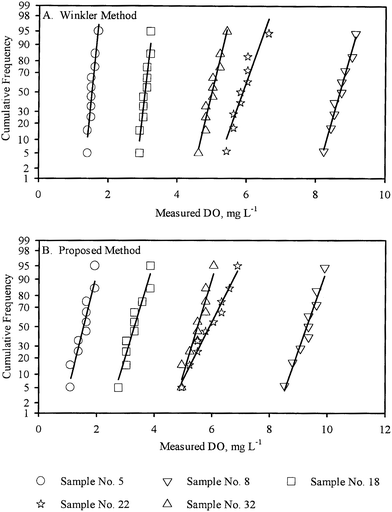
Le varianze (S21,S22) nelle misurazioni replicate di un campione rispettivamente da WM e PM sono state utilizzate per il confronto a coppie delle corrispondenti varianze di popolazione (σ21,σ22) utilizzando il test F. Dei 33 campioni per i quali il DO è stato misurato con i due metodi (WM e PM), l’ipotesi che le varianze di popolazione fossero uguali (σ21 = σ22) non ha potuto essere rifiutata al livello di confidenza del 95% per 19 campioni. Inoltre, l’ipotesi σ21 > σ22 non poteva essere rifiutata per 4 campioni, mentre l’ipotesi σ21 < σ22 non poteva essere rifiutata per i restanti 10 campioni, tutti a livello di confidenza del 95 per cento. Questi risultati sono stati riassunti nella tabella 3.
Inoltre, le varianze dei campioni (S21,S22) e le medie dei campioni (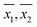 ) per ogni campione, come ottenuto da WM e PM rispettivamente sono state utilizzate per il confronto a coppie delle corrispondenti medie della popolazione (μ1, μ2). Per i campioni con varianze uguali (vedi tabella 3), il confronto a coppie è stato fatto usando il test t di Student. Per i campioni con varianze disuguali (vedi Tabella 3), il confronto a coppie è stato fatto utilizzando il t-test della varianza disuguale.17 In 23 dei 33 campioni in cui le misurazioni DO sono state effettuate sia da WM che da PM, l’ipotesi che le medie della popolazione fossero uguali (μ1 = μ2) non poteva essere rifiutata al livello di confidenza del 95%.
) per ogni campione, come ottenuto da WM e PM rispettivamente sono state utilizzate per il confronto a coppie delle corrispondenti medie della popolazione (μ1, μ2). Per i campioni con varianze uguali (vedi tabella 3), il confronto a coppie è stato fatto usando il test t di Student. Per i campioni con varianze disuguali (vedi Tabella 3), il confronto a coppie è stato fatto utilizzando il t-test della varianza disuguale.17 In 23 dei 33 campioni in cui le misurazioni DO sono state effettuate sia da WM che da PM, l’ipotesi che le medie della popolazione fossero uguali (μ1 = μ2) non poteva essere rifiutata al livello di confidenza del 95%.
Le medie dei campioni (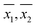 ) per ogni campione, come ottenuto da WM e PM rispettivamente sono state tracciate tra loro in Fig. 2. Le barre di errore mostrate nella figura corrispondono ai corrispondenti intervalli di confidenza al 95%. Nella stessa figura è stata tracciata anche una linea di pendenza unitaria passante per l’origine. Tutti i punti sono stati osservati come molto vicini alla linea di pendenza unitaria, che è in accordo con le conclusioni generali tratte nella tabella 3, cioè, per la maggior parte dei campioni, la concentrazione media di DO ottenuta con i due metodi non è statisticamente diversa. Quindi, nella maggior parte dei casi, la misurazione del DO tramite PM è stata accurata quanto la misurazione del DO tramite WM.
) per ogni campione, come ottenuto da WM e PM rispettivamente sono state tracciate tra loro in Fig. 2. Le barre di errore mostrate nella figura corrispondono ai corrispondenti intervalli di confidenza al 95%. Nella stessa figura è stata tracciata anche una linea di pendenza unitaria passante per l’origine. Tutti i punti sono stati osservati come molto vicini alla linea di pendenza unitaria, che è in accordo con le conclusioni generali tratte nella tabella 3, cioè, per la maggior parte dei campioni, la concentrazione media di DO ottenuta con i due metodi non è statisticamente diversa. Quindi, nella maggior parte dei casi, la misurazione del DO tramite PM è stata accurata quanto la misurazione del DO tramite WM.
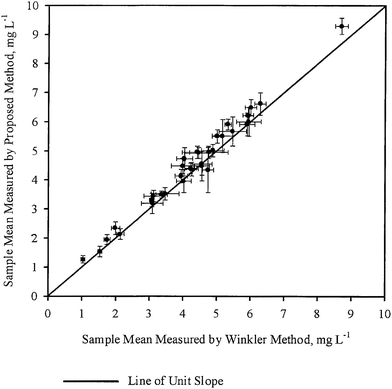
Le deviazioni standard dei campioni (S1,S2) per ogni campione, come ottenuto da WM e PM rispettivamente sono state tracciate l’una contro l’altra in Fig. 3. Nella stessa figura è stata tracciata anche una linea di pendenza unitaria passante per l’origine. In questo caso, i punti sembrano essere dispersi abbastanza uniformemente rispetto alla linea di pendenza unitaria, con alcuni punti vicini alla linea, mentre gli altri sono più lontani. Queste osservazioni sono anche in accordo generale con le conclusioni tratte dalla tabella 3, cioè, per la maggior parte dei campioni, la variazione della concentrazione di DO misurata dai due metodi non è statisticamente diversa. Quindi, nella maggior parte dei casi, la misurazione del DO con il PM è stata precisa quanto la misurazione del DO con il WM.
Si è concluso che con un’attenta manipolazione e titolazione del campione, il metodo proposto (PM) può produrre risultati comparabili al metodo di Winkler (WM) sia in termini di accuratezza che di precisione. Tuttavia, l’accuratezza della determinazione del DO con il metodo PM può probabilmente essere aumentata utilizzando una microsiringa con un numero inferiore per la titolazione finale. La microsiringa usata in questo studio aveva un conteggio minimo di 5 μL, che corrisponde a un’incertezza di ∼0,25 mg L-1 DO nelle condizioni del presente studio. Questa incertezza può essere abbassata usando una microsiringa con un conteggio minimo più basso.
Conclusioni
L’obiettivo di questo studio era di sviluppare un metodo accurato, a basso costo, semplice e veloce per la misurazione del DO in piccoli volumi di campione. Sulla base dei risultati e delle analisi presentate, si può concludere che il metodo proposto affronta la maggior parte dei problemi sopra citati. Le principali conclusioni dello studio sono state le seguenti:
➢ L’introduzione di uno strato isolante di n-esano per la prevenzione del trasferimento di ossigeno tra il campione acquoso e l’atmosfera permette una determinazione coerente e accurata del DO in piccoli volumi di campione. Questa è la principale innovazione incorporata nel metodo proposto.
➢ È stato anche dimostrato che, prendendo le precauzioni adeguate, il metodo proposto (PM) può generalmente produrre risultati che sono statisticamente comparabili con i risultati ottenuti dal metodo di Winkler (WM), sia per quanto riguarda la concentrazione media di DO che per quanto riguarda la varianza della concentrazione di DO intorno alla media.
➢ I requisiti dei reagenti e della vetreria per il metodo proposto sono inferiori a quelli del metodo di Winkler, principalmente a causa del minor volume di campione utilizzato. L’n-esano è l’unico reagente aggiuntivo utilizzato, ma la piccola quantità (∼1,5 mL per campione) di n-esano richiesta ha un impatto trascurabile sul costo complessivo dell’analisi del campione.
Il metodo proposto (PM) può quindi essere utilizzato per la misurazione del DO in tutte le circostanze in cui il metodo di Winkler è attualmente utilizzato. Il metodo proposto è particolarmente utile nelle circostanze in cui il metodo di Winkler non può essere utilizzato a causa delle limitazioni del volume di campione disponibile.