Lavaggio polmonare intero bilaterale nella proteinosi alveolare polmonare – Uno studio retrospettivo
Introduzione
La proteinosi alveolare polmonare (PAP) è una rara malattia polmonare diffusa con tre forme cliniche, congenita, acquisita (idiopatica) e secondaria, caratterizzata da un accumulo di grandi quantità di materiale fosfolipoproteico negli alveoli a causa di una carenza di attività del fattore stimolante la colonia dei granulociti-macrofagi (GM-CSF)1-14 (Fig. 1). Questo è associato a una funzione anormale dei macrofagi e a un’alterata eliminazione del surfattante dai polmoni. La PAP ha una prevalenza di 3,7 casi per milione, una preponderanza maschile (rapporto maschio/femmina 4:1) e l’80% dei casi sono riportati durante la terza e quarta decade di vita.6
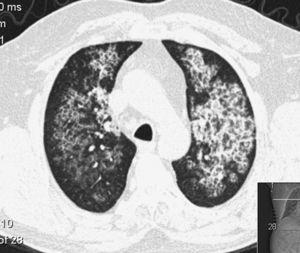
Scansione TAC di un paziente con proteinosi alveolare polmonare. Si noti l’ispessimento dei setti interlobari all’interno del parenchima opacizzato che produce un modello di “pavimentazione folle”.
Il lavaggio polmonare completo (WLL), introdotto negli anni 60,3,4,7,10,15 è ancora il trattamento gold standard.6 Il WLL unilaterale, con il lavaggio eseguito in ciascun polmone in diverse sessioni separate da giorni/settimane, è la procedura più frequente. Tuttavia, il WLL bilaterale sequenziale nella stessa sessione di trattamento è un’alternativa attraente, poiché richiede molto meno tempo, con un minore disagio per il paziente ed è più conveniente.
La sua efficacia è stata attribuita non solo alla rimozione di materiale lipoproteico dagli spazi alveolari, ma anche alla rimozione di anticorpi anti GM-CSF, macrofagi alveolari e cellule epiteliali di tipo II. Questa procedura terapeutica viene presa in considerazione quando il paziente riferisce una significativa limitazione delle attività quotidiane e/o viene rilevata un’ipossiemia con una pO2
60mmHg, una P(A-a) O2 ≥40mmHg e una frazione di shunt ≥10%.12
Nel nostro ospedale, abbiamo eseguito la prima WWL nel 2010 e dopo cinque WLL unilaterali, siamo passati a un programma di WWL bilaterale sequenziale.
Lo scopo di questa relazione è di descrivere la tecnica WLL bilaterale e di discutere la sua sicurezza ed efficacia.
Metodi
In questo studio retrospettivo, abbiamo raccolto dati demografici e clinici dai referti medici di tre pazienti adulti. La tecnica standard applicata era una versione modificata del protocollo della tecnica del Royal Brompton Hospital (Londra).6,10
Durante la procedura, l’elettrocardiografia, la pulsossimetria (SatO2), la pressione sanguigna invasiva, la pressione venosa centrale (CVP), la produzione di urina, la capnografia, i volumi correnti dell’indice bispettrale (BIS) e la temperatura centrale sono stati monitorati continuamente e i gas sanguigni arteriosi (ABG) sono stati fatti ogni ora. Un’anestesia totale endovenosa (TIVA) è stata eseguita per consentire la profondità dell’anestesia da gestire, indipendentemente dalle variazioni ventilatorie inerenti alla procedura. La curarizzazione è stata mantenuta durante l’intera procedura. È stato introdotto un tubo a doppio lume (DLT) sinistro, selezionando la dimensione più grande possibile, per garantire l’isolamento polmonare e promuovere la ventilazione e l’efficacia del WLL. La sua posizione corretta è stata confermata dalla broncoscopia a fibre ottiche e insufflazione pressione bracciale misurata al fine di evitare perdite controlaterali dal liquido di lavaggio.11
Una pre-ossigenazione con una FiO2 del 100% è stato effettuato durante 5 minuti per garantire una corretta denitrogenazione alveolare e la comparsa di bolle d’aria, che potrebbe compromettere la rimozione del materiale lipoproteinaceo dagli alveoli. La ventilazione unipolmonare è stata avviata e l’isolamento polmonare è stato verificato. I pazienti sono stati ventilati con una ventilazione a pressione controllata, con un valore di pressione inferiore a 30cmH2O. Il volume di soluzione salina da instillare è stato calcolato in base alle misurazioni preoperatorie della capacità funzionale residua (FRC). Il volume del polmone destro fu calcolato da 3/5 della FRC e il polmone sinistro da 2/5 della FRC (nel primo ciclo fu instillato un volume minore). La soluzione salina dovrebbe essere instillata sotto l’effetto gravitazionale da un’altezza non superiore a 40 cm sopra la linea medio-ascellare, al fine di prevenire il barotrauma e la perdita nel polmone ventilato.10 Anche se alcuni rapporti descrivono un posizionamento di decubito laterale a 30° per preservare il rapporto di ventilazione/perfusione del polmone ventilato dipendente, questo aumenta la probabilità di inondazione del polmone controlaterale, quindi abbiamo preferito un posizionamento di decubito dorsale, con un trendelenburg inverso così come il posizionamento trendelenburg per facilitare l’instillazione gravitazionale e la rimozione della soluzione salina calda dai polmoni.6,11 Questo posizionamento è stato adottato quando è stato eseguito un WLL bilaterale (Fig. 2).
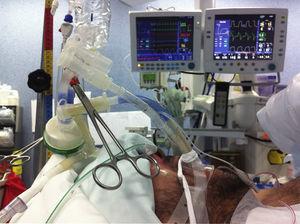
Rappresentazione tecnica di un WLL.
Quando il deflusso, inizialmente lattiginoso, è diventato meno denso, il drenaggio è stato interrotto a metà del volume, e diversi cicli di ventilazione manuale utilizzando una valvola CPAP con limite di pressione di 5-10mmHg (la “modifica Bingisser”) hanno permesso una percussione manuale degli alveoli. Questa manovra migliora notevolmente la clearance lipoproteinacea.12,14 Il ciclo di lavaggio è stato ripetuto fino a quando il flusso di lavaggio è diventato limpido (Fig. 3). Poiché il volume di lavaggio del fluido è elevato durante la procedura, c’è un alto rischio di ipotermia. La conservazione della temperatura corporea è cruciale e dovrebbe essere mantenuta usando il fluido di lavaggio riscaldato a 37°C e una coperta riscaldante.

Evoluzione del fluido lattiginoso attraverso la procedura.
Dopo che il primo polmone è stato lavato con successo, è stato accuratamente aspirato e la sua riespansione è stata eseguita, inizialmente con ventilazione bilaterale seguita da ventilazione unilaterale. Dopo 1 ora di ventilazione, sono stati verificati i dati di compliance polmonare e di analisi dei gas sanguigni. Se il polmone lavato era in grado di assicurare le esigenze di scambio gassoso del paziente, allora si iniziava il WLL controlaterale, ripetendo le procedure descritte sopra.8
Al termine della procedura la soluzione salina residua veniva aspirata attraverso la broncoscopia a fibre ottiche e la ventilazione bilaterale veniva ripresa. Il tubo a doppio lume è stato poi sostituito da un tubo endotracheale e il paziente è stato trasferito in un’unità di recupero per il monitoraggio notturno.
Risultati
La WWL bilaterale è stata eseguita in tre pazienti adulti, 2 maschi e 1 femmina, età media di 43,6 (range 39 – 47 anni) (Tabella 1) tutti con ipossia a riposo inferiore a 60mmHg.
Quantità di soluzione salina instillata e trattenuta nella WWL bilaterale.
| Lavaggi | Volume (L) Polmone destro | Volume (L) Polmone sinistro | ||
| Instillato (L) | Bilancio positivo (mL) | Volume versato (L) | Bilancio positivo (mL) | |
| 1° | 9.2 | 470 | 11.8 | 510 |
| 2° | 15.3 | 530 | 10.7 | 450 |
| 3° | 14.0 | 600 | 10.8 | 550 |
| 4° | 13.5 | 500 | 10.6 | 350 |
| 5° | 15.5 | 930 | 11.1 | 480 |
| 6° | 15.5 | 820 | 15.3 | 900 |
Il primo paziente era maschio, 39 anni, fumatore, panettiere, con diagnosi di PAP un mese prima del primo WLL, sulla base delle caratteristiche cliniche, radiologiche e BAL e la presenza di anticorpi sierici GM-CSF. Alla presentazione della malattia aveva insufficienza respiratoria associata a un esteso coinvolgimento polmonare bilaterale osservato in HRCT-scan e un WLL bilaterale è stato eseguito con 9.2 e 11.8L di soluzione salina instillata nel polmone destro e sinistro rispettivamente. Dopo un breve periodo di miglioramento clinico, funzionale e radiologico, le condizioni del paziente sono peggiorate con la diffusione delle opacità polmonari radiologiche e l’insufficienza respiratoria. Questo deterioramento clinico ha coinciso con il suo ritorno al posto di lavoro. Infatti, la farina da forno era stata descritta come un potenziale fattore scatenante.16 Un secondo WLL bilaterale è stato eseguito tre mesi dopo, e sono stati instillati 15,3 e 10,7 L di soluzione salina. Dopo questa procedura e la cessazione del suo precedente ambiente di lavoro, il paziente ha mantenuto la stabilità clinica.
Il secondo paziente sottoposto a WLL era una donna, 47 anni, contadina, non fumatrice, senza comorbidità, con la diagnosi di PAP un mese prima del primo WLL sulla base delle caratteristiche cliniche, radiologiche e BAL e la presenza di anticorpi sierici GM-CSF. La presentazione clinica era molto simile a quella del primo paziente, con dispnea da sforzo e una tosse secca associata a insufficienza respiratoria e ampie opacità bilaterali a matrice paonazza nella scansione HRCT. Dopo la diagnosi, è stato eseguito un WLL con l’instillazione di 14 e 10.8L di soluzione salina nel polmone destro e sinistro rispettivamente. Dopo un breve miglioramento clinico iniziale, è stata sottoposta a un altro WLL 1,5 mesi dopo, poiché era diventata più sintomatica e con paO2
60mmHg. Con questa procedura, un totale di 13,5 e 10,6L furono instillati rispettivamente nel polmone destro e sinistro. Quattro mesi dopo è stato eseguito un terzo WLL a causa del deterioramento clinico e in questa occasione sono stati instillati 15,5 e 11,1 litri rispettivamente nel polmone destro e sinistro (Fig. 4). Dopo questa procedura, il paziente ha raggiunto la stabilità clinica, funzionale e radiologica.

Campioni sequenziali di WLLs bilaterali.
Il terzo paziente incluso era un maschio, 45 anni, ex-fumatore, operaio della fabbrica di pneumatici, con la diagnosi di PAP durante una valutazione e trattamento dell’ascesso cerebrale indotto da nocardia. Come per gli altri due pazienti, la diagnosi è stata stabilita dalle caratteristiche radiologiche e BAL tipiche associate agli anticorpi GM-CSF del siero. Tuttavia, aveva avuto una precedente scansione HRCT toracica con un modello di pavimentazione folle bilaterale due anni prima. Un anno dopo la diagnosi, è diventato più sintomatico, con dispnea da sforzo e insufficienza respiratoria (paO2-57mmHg) e quindi è stato sottoposto a un WLL con instillazione di 15,5 e 15,3 di soluzione salina rispettivamente nel polmone destro e sinistro. Dopo questa procedura, ha ottenuto un significativo miglioramento clinico, funzionale e radiologico.
Tutte le sei procedure WLL sono state eseguite secondo il protocollo stabilito e senza complicazioni importanti.
Il monitoraggio gasometrico giornaliero si è concentrato sull’assicurazione di una corretta ossigenazione e ventilazione. I valori gasometrici del paziente sono stati facilmente mantenuti durante tutta la procedura, con una pCO2 sotto i 55 mmHg e una SpO2 sostenuta al di sopra dei valori attuali del paziente stesso, nonostante fossero in posizione supina (Tabella 2) (Fig. 5). Infatti, in tutti i pazienti sottoposti a WWL bilaterale abbiamo osservato una progressiva installazione di acidosi metabolica durante la procedura. Questa acidosi metabolica è stata invertita nelle prime ore post-operatorie e nessuna comorbidità è stata identificata in seguito.
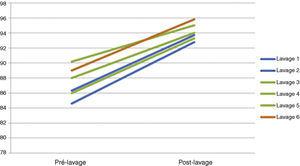
Evoluzione delle misure di SatO2 durante i lavaggi polmonari integrali.
Con la manovra di Bingisser abbiamo osservato una transitoria difficoltà a recuperare il volume del lavaggio (contribuendo ad un bilancio fluido positivo) ma un evidente aumento della densità del lavaggio.
In ogni caso abbiamo osservato un episodio di stravaso di lavaggio controlaterale. In tutte le procedure la temperatura corporea è stata mantenuta tra 36 e 37°C. Il tempo medio della procedura è stato di 8 ore (range 7h32-9h41).
Il tempo di estubazione variava secondo l’evoluzione clinica e dell’emogasanalisi e tutti i pazienti sono stati estubati con successo dopo 18 ore.
Dopo queste procedure la capacità funzionale e le attività quotidiane di tutti i pazienti erano significativamente migliorate, documentate da segni/sintomi clinici, nonché dai test di funzionalità respiratoria e dai dati gasometrici.
Discussione
In questa breve comunicazione abbiamo descritto sei procedure bilaterali sequenziali di WLL, eseguite in tre pazienti con PAP, corroborando la sua efficacia clinica e la sua sicurezza.
Nonostante la sua significativa invasività, la WLL rimane il trattamento raccomandato nella PAP, ed è stata finora l’unica terapia con efficacia stabilita. Infatti, quando un paziente con PAP si presenta con insufficienza respiratoria e opacità estese alla scansione HRCT, questa procedura è obbligatoria. Il WLL è una tecnica costosa e dispendiosa in termini di tempo, richiede la competenza di un approccio multidisciplinare e questo, insieme alla rarità della PAP, spiega perché questa procedura viene eseguita solo in un piccolo numero di centri. La scelta di un WLL bilaterale significa un migliore comfort del paziente, riduzioni di costi e tempi e mantenimento dell’efficacia clinica.
I tre pazienti inclusi potrebbero essere considerati casi tipici di PAP, anche se c’erano alcune differenze. Due di loro avevano una presentazione acuta della malattia, avendo bisogno di WLL dopo la diagnosi, mentre l’altro è stato sottoposto a questa procedura durante il corso della malattia. Mentre questo terzo paziente ha dovuto essere sottoposto a un solo WLL, gli altri due hanno dovuto avere WLL multipli, per essere precisi a due e tre procedure.
Il fattore cruciale per poter procedere al secondo lavaggio polmonare è se la prima ventilazione polmonare lavata ha recuperato una capacità sufficiente per assicurare le necessità del paziente. Per questo motivo, se non c’è predominanza laterale, abbiamo scelto il polmone più grande, il polmone destro, da lavare per primo. Per prevenire il barotrauma, la pressione inspiratoria massima è stata limitata a 30cmH2O. In tutte le procedure, dopo 1 ora di ventilazione, la compliance polmonare e i valori gasometrici nella ventilazione monopolmonare del polmone lavato erano compatibili con l’inizio del lavaggio del secondo polmone.
La scelta della ventilazione controllata dalla pressione ci ha permesso di monitorare continuamente i cambiamenti nella compliance polmonare durante il lavaggio e ha impedito la possibile dislocazione del tubo o qualsiasi altra interferenza. Inoltre, allo stesso modo, ha permesso di osservare il recupero della compliance polmonare lavata.
La posizione supina del paziente non ha ostacolato l’ossigenazione, e quindi non abbiamo dovuto ricorrere alla posizione di decubito laterale con ventilazione del polmone dipendente, posizionamento che è meno stabile e comporta maggiori rischi in una procedura lunga (media 8h).
Abbiamo scelto la percussione della manovra di Bingisser per il fatto che la pressione esercitata sulle vie aeree viene misurata, a differenza delle manovre di chinesiterapia, dove tale quantificazione è impossibile, riducendo così il rischio di un’eccessiva pressione di percussione, evitando e prevenendo una possibile inondazione controlaterale.8
Nel tentativo di invertire l’acidosi metabolica osservata durante le procedure, il siero di mantenimento utilizzato nel periodo perioperatorio – cloruro di sodio 0,9% – è stato sostituito dal lattato di ringer nella terza procedura bilaterale e successivamente, con solo modesti miglioramenti. In letteratura non c’è alcun riferimento all’uso di questo soluto come liquido di lavaggio polmonare, quindi il cloruro di sodio rimane in uso.
In conclusione, considerando l’efficacia clinica del WLL bilaterale, i suoi vantaggi nel risparmio di tempo e costi e la riduzione del disagio del paziente rendono questa tecnica una prima scelta adatta nel lavaggio terapeutico nei pazienti PAP.
Discrezioni eticheProtezione dei soggetti umani e animali
Gli autori dichiarano che le procedure seguite sono state conformi alle norme del comitato etico di ricerca clinica pertinente e a quelle del codice etico dell’associazione medica mondiale (Dichiarazione di Helsinki).
Confidenzialità dei dati
Gli autori dichiarano di aver seguito i protocolli del loro centro di lavoro sulla pubblicazione dei dati dei pazienti.
Diritto alla privacy e al consenso informato
Gli autori dichiarano che nessun dato dei pazienti appare in questo articolo.
Conflitti di interesse
Gli autori non hanno conflitti di interesse da dichiarare.
Gli autori non hanno conflitti di interesse.