Diagnostisk avbildning av avvikelser i den vita substansen | Medfödd cerebral hypomyelinisering; nätverk för Pelizaeus-Merzbachers sjukdom och relaterade sjukdomar
Diagnostic Imaging of White Matter Abnormalities
Junichi TAKANASHI, Department of Pediatrics, Tokyo Women’s Medical University, Yachiyo Medical Center
Introduktion
I den här artikeln redogör jag för det tillvägagångssätt som används för diagnostik av sjukdomar som uppträder som onormala signaler i hjärnans vita substans vid magnetresonanstomografi (MRT), från avbildning till diagnos. Störningar som huvudsakligen påverkar den vita substansen kallas allmänt för ”leukoencefalopati” eller ”white matter disorders” på engelska.1, 2) 3) En annan term, leukodystrofi, förväxlas ibland med degeneration av vit substans, men detta avser egentligen ett smalare spektrum av sjukdomar med en genetisk komponent (nedärvda demyeliniserande sjukdomar).
Bilddiagnostikbaserad klassificering av sjukdomar i den vita substansen
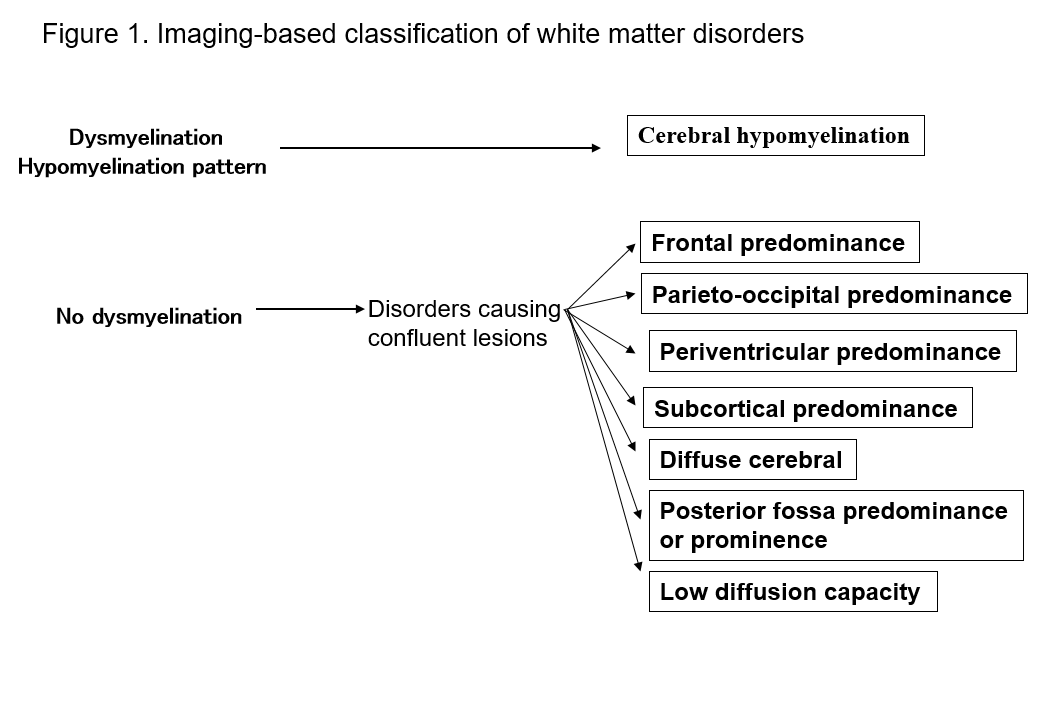
Med framväxten av MRT har vår förmåga att upptäcka lesioner i den vita substansen i det centrala nervsystemet förbättrats dramatiskt. Många kända former av sjukdomar i den vita substansen uppvisar specifika tecken på MRT, vilket är användbart för deras diagnostik. Att identifiera mönster av avvikelser i den vita substansen som ses på MRT (T1-viktad, T2-viktad eller FLAIR-avbildning) gör det lätt att begränsa möjligheterna vid flera differentialdiagnoser. Schiffmann och van der Kamps klassificering av sjukdomar i den vita substansen enligt MRT-fynd är av praktiskt värde2, 4) (figur 1, tabell 1). Även om detta inte leder till en slutgiltig diagnos kan klassificeringen av bilddiagnostiska fynd leda till att man senare upptäcker en ny sjukdom. Här beskriver jag sjukdomar i den vita substansen utifrån ovanstående MRT-klassificeringar och förklarar de viktigaste typerna av sjukdomar.
Tabell 1. Förteckning över sjukdomar efter MRI-mönster
- Frontal dominans
Alexanders sjukdom, frontal variant av X-bunden adrenoleukodystrofi (ALD), metakromatisk leukodystrofi (MLD), neuroaxonal leukodystrofi med sfärer. - Parieto-occipital predominans
X-bunden adrenoleukodystrofi (ALD), Krabbes sjukdom, peroxisomala sjukdomar med tidig debut, neonatal hypoglykemi. - Periventrikulär dominans
Metachromatisk leukodystrofi (MLD), Krabbes sjukdom, Sjögren-Larssons syndrom, vuxen polyglukosankroppssjukdom, leukoencefalopati med hjärnstam- och ryggmärgsinblandning och laktatförhöjning (LBSL), periventrikulär leukodystrofi (PVL), hiv-encefalopati, senare insjuknande i neuronala ceroid lipofuscinoser. - Subkortikal predominans
L-2-hydroxyglutarsyrauri, galaktosemi, Kearns-Sayers syndrom, propionakemi, störningar i ureacykeln, Canavans sjukdom. - Diffus cerebral
Megalencefalisk leukoencefalopati med subkortikala cystor (MLC), leukoencefalopati med försvinnande vit substans (VWM), medfödd muskeldystrofi med merosinbrist, mitokondriell sjukdom, molybdenkofaktorbrist, sulfitoxidasbrist, avancerade fall av sjukdomar i vit substans. - Dominans eller framhävning i den bakre fossa
Lesioner i cerebellum och cerebellar peduncles: cerebrotendinös xanthomatos (CTX), peroxisomala sjukdomar, Alexanders sjukdom, leukoencefalopati med hjärnstams- och ryggmärgsinblandning och laktatförhöjning (LBSL), lönnsirapurinsjukdom, histiocytos, vuxen autosomal dominant leukodystrofi relaterad till en lamin B1-duplikation, heroin- och kokaintoxicitet.
Hjärnstamslesioner: Alexanders sjukdom, LSBL, peroxisomala sjukdomar, Wilsons sjukdom, vuxen polyglukosansjukdom, Leighs syndrom, dentatorubropallidoluysian atrofi (DRPLA), vuxen polyglukosankroppssjukdom, vuxen autosomal dominant leukodystrofi relaterad till en lamin B1 duplikation. - Multifokala lesioner
TORCH-syndrom (medfödd cytomegalovirusinfektion), brucellos, akut disseminerad encefalomyelit (ADEM), multipel skleros (MS), neuromyelitis optica (NMO), cerebral autosomalt dominant arteriopati med subkortikala infarkter och leukoencefalopati (CADASIL), ateroskleros, amyloid angiopati, COL4A1-associerad cerebral småkärlssjukdom, Fabrys sjukdom, Susacs syndrom, mitokondriell sjukdom, L-2-hydroxyglutarsyrauri, mukopolysackaridos (MPS), kromosomala avvikelser (såsom 6p-syndrom). - Lesioner med låg spridningskapacitet
Maple syrup urine disease, methionin adenosyltransferase I/III deficiency, fenylketonuri, icke-ketotisk hyperglycinemi, Canavans sjukdom, aktiva lesioner vid Krabbes sjukdom och metakromatisk leukodystrofi.
1. Hypomyelinisering av cerebral vit substans
Detta avser en grupp sjukdomar där bildandet av myelinskidan är nedsatt eller fördröjd, och dess bilder liknar dem hos nyfödda barn med omogen myelinisering. På T2-viktade bilder framträder den vita substansen karakteristiskt som en utbredd hyperintensitet som är svag jämfört med cortex. Mer information finns på webbplatsen för medfödd cerebral hypomyelinatio.
Om vitämneslesioner inte stämmer överens med hypomyelinisering av den vita substansen i hjärnan måste man avgöra om de är konfluenta eller multipla. 2) Konfluenta vitämneslesioner beror vanligen på ärftlig degeneration av den vita substansen (leukodystrofi) och är i de flesta fall bilateralt symmetriska. Multipla vita substanslesioner är vanligen asymmetriska och förvärvade. Konfluenta lesioner i vit substans delas vidare in i kategorierna 2-7 nedan.
2. Frontal predominans
I denna grupp av sjukdomar förekommer omfattande lesioner i vit substans främst i frontalloben. De omfattar Alexanders sjukdom, den frontala varianten av X-bunden adrenoleukodystrofi (ALD), metakromatisk leukodystrofi (MLD) och neuroaxonal leukodystrofi med sfärer.
(a) Alexanders sjukdom.
Alexanders sjukdom är en autosomal dominant ärftlig sjukdom som orsakas av en mutation i GFAP-genen på kromosom 17q21. Den resulterar i ackumulering av Rosenthalfibrer i de stellata gliacellerna. Dessa fibrer består av GFAP och stressproteiner (αB-kristallin och HSP27. Alexanders sjukdom uppträder huvudsakligen i spädbarnsåldern, mellan 3 månaders och 2 års ålder, med förekomst av megalencefali, utvecklingsstörning, spastisk paralys och epilepsi. På MRT kan den uppvisa i) utbredda lesioner i den vita substansen, främst i frontalloben, ii) T1 hyperintensiv och T2 hypointensiv marginalisering runt de laterala ventriklarna, iii) lesioner i basalganglierna och thalamus, iv) lesioner i hjärnstammen och v) kontrastförstärkning av aktiva lesioner (figur 2). I de tidiga stadierna ses tillsammans med lesioner i vit substans och putamen en svullnad som gradvis kan orsaka atrofi eller cystbildning.
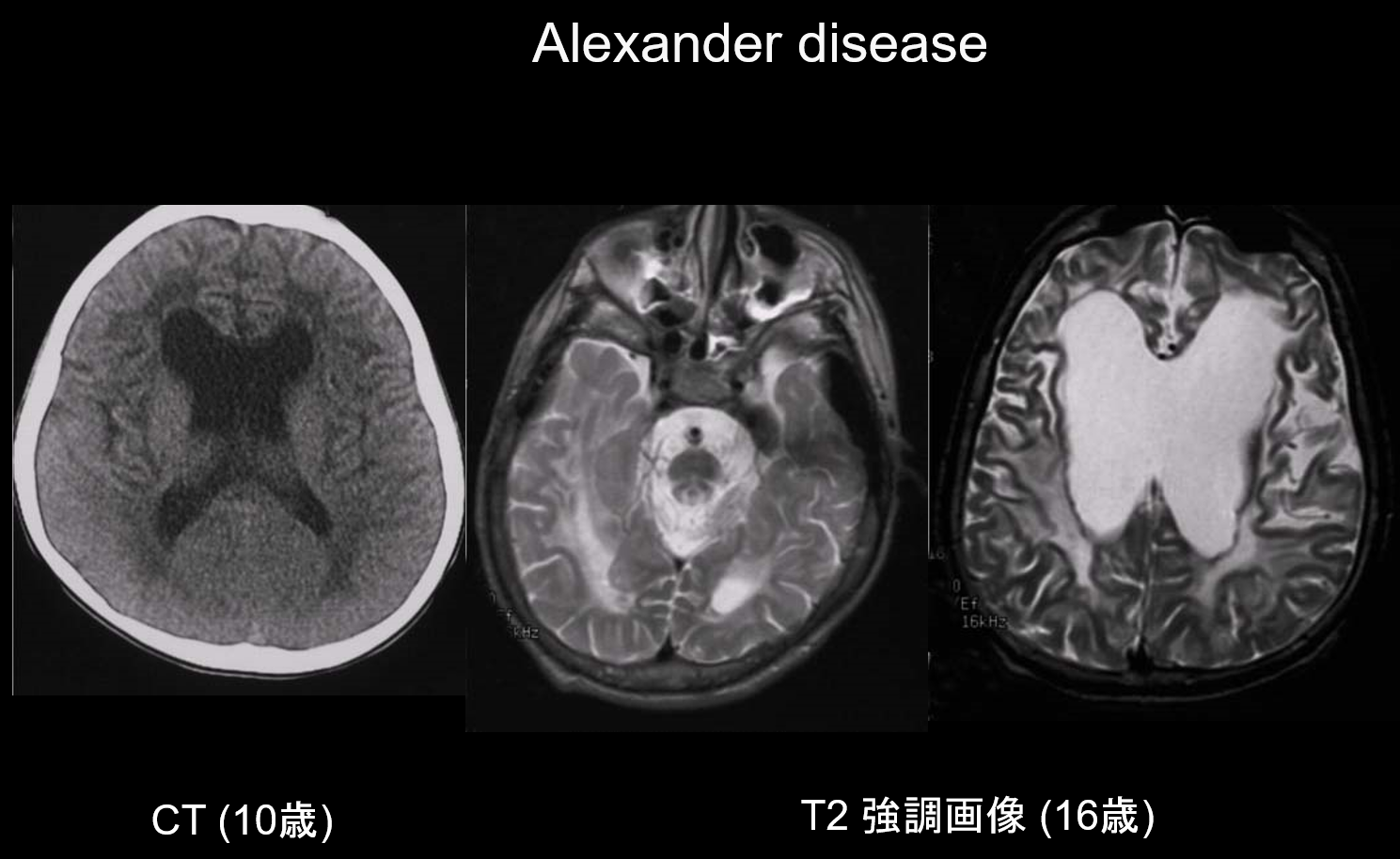
3. Parieto-occipital predominans
Det viktigaste kännetecknet för denna grupp av sjukdomar är parieto-occipitala lesioner av den vita substansen. De omfattar X-bunden adrenoleukodystrofi (ALD), Krabbes sjukdom, tidiga peroxisomala störningar och neonatal hypoglykemi.
(a) Krabbes sjukdom.
Krabbes sjukdom är en autosomalt recessivt nedärvd sjukdom (lysosomal lagringssjukdom) som orsakas av galaktosylceramidasbrist (kromosom 14q31), där ackumulationen av starkt cytotoxiskt psykosin tros orsaka utbredd demyelinisering. Stora, flerkärniga celler som kallas ”globoidceller” förekommer också. Beroende på den ålder då sjukdomen uppträder klassificeras den som infantil, sen infantil, juvenil eller vuxen. De flesta fall är infantila och börjar med feber, irritabilitet, matningssvårigheter, utvecklingsstörning, perifer neuropati, spasticitet och optisk nervatrofi vid 3-6 månaders ålder. Under de tidiga stadierna visar datortomografi (CT) karakteristisk hyperdensitet i thalamus och corona radiata. Detta tros återspegla globoida celler med hög densitet och glial proliferation. MRT kan också visa T1-hyperintensitet och T2-hypointensitet runt ventriklarna samt linjära strukturer som liknar dem som ses vid MLD (figur 3). Den cerebellära dentatkärnan, cerebellära vita substansen och hjärnstammens pyramidala trakter uppvisar T2-hyperintensitet från ett tidigt stadium.
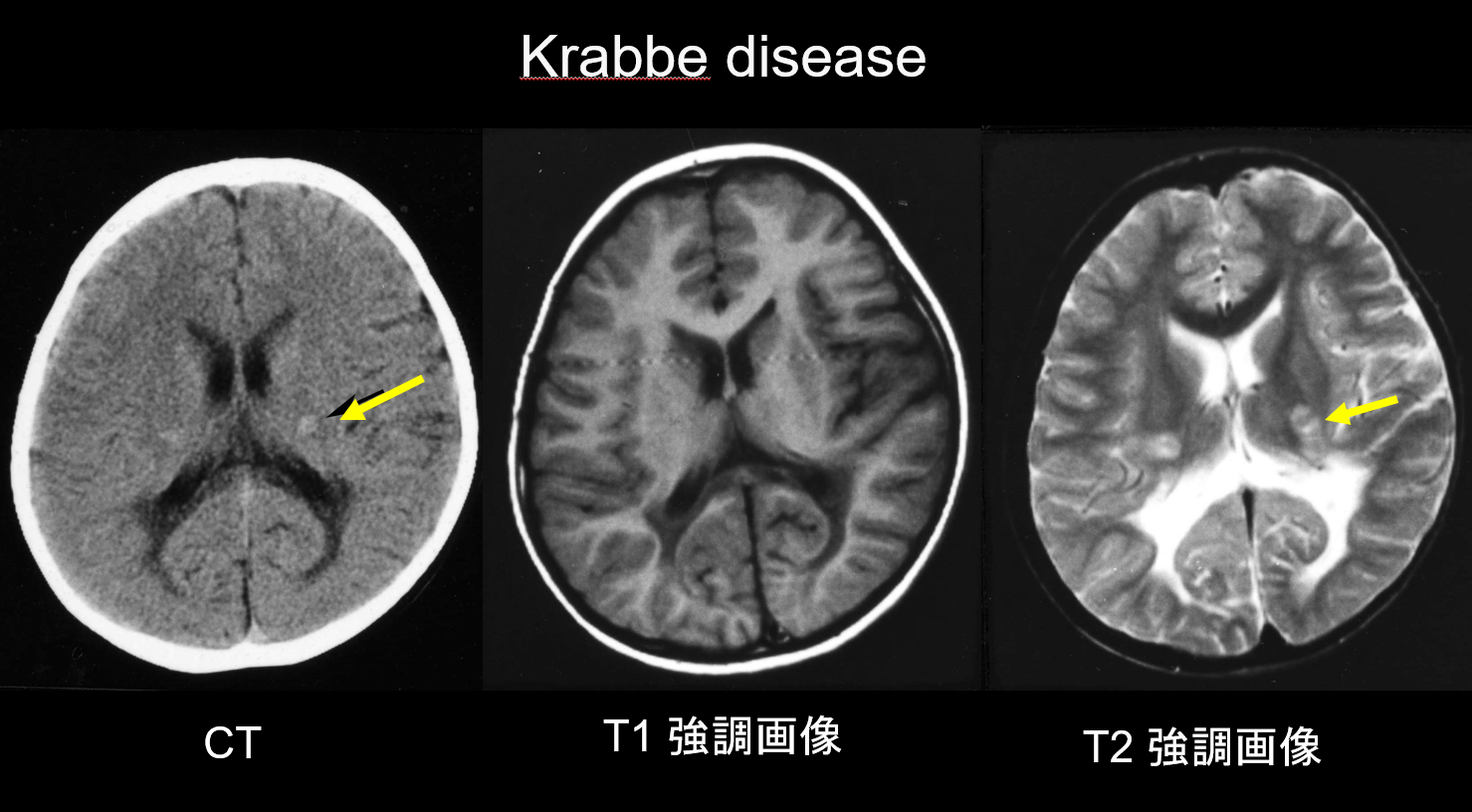
(b) X-bunden adrenoleukodystrofi
X-bunden adrenoleukodystrofi (ALD) är en X-bunden recessiv ärftlig sjukdom (peroxisomal sjukdom) som orsakas av en abnormitet i ABCD1-genen (kromosom Xq28). Försämrad β-oxidation resulterar i ackumulering av mycket långkedjiga fettsyror i hjärnans vita substans och i binjurarna, vilket orsakar demyelinisering och binjureinsufficiens. ALD kategoriseras i barndoms-, ungdoms- och vuxna cerebrala former, adrenomyeloneuropati (AMN) och enbart Addisons sjukdom. Den cerebrala barndomsformen utvecklas vid 5-8 års ålder, med uppkomsten av symtom som intellektuell försämring, spastisk gång och nedsatt syn och hörsel. Patologiskt sett fortskrider demyeliniseringen från den vita substansen som omger trigonen i den laterala ventrikeln till splenium i corpus callosum och utvidgas gradvis anterolateralt. Som en återspegling av sjukdomspatologin kan man på MRT se symmetriska T2-hyperintensiviteter och T1-hypointensiviteter som sträcker sig anterolateralt från den vita substansen som omger trigonen i den laterala ventrikeln, med kontrastförstärkning vid marginalerna (figur 4). Läsioner i kortikospinalbanan är också uppenbara.
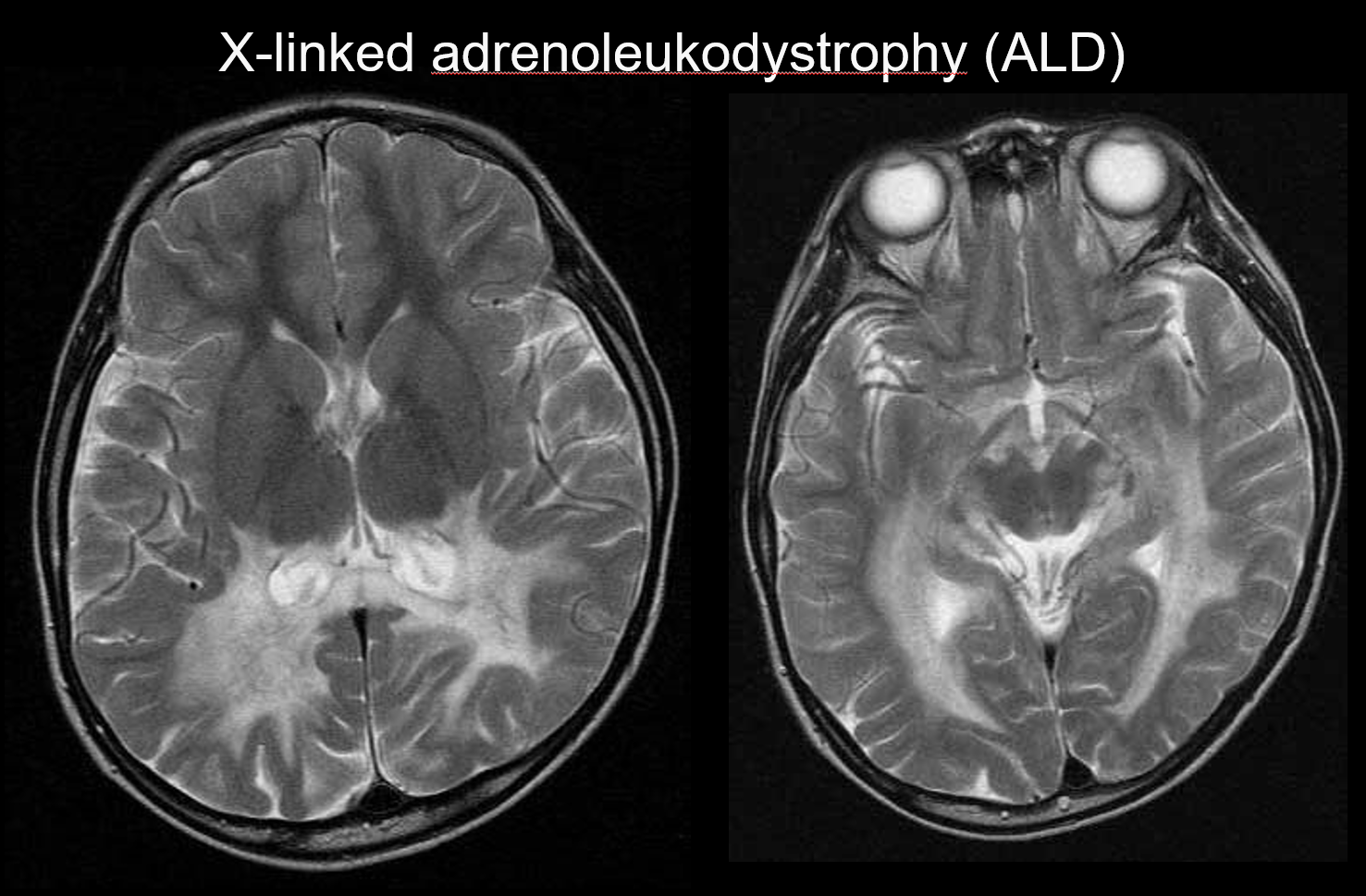
4. Periventrikulär predominans
Dessa sjukdomar kännetecknas främst av lesioner i den vita substansen som omger de laterala ventriklarna, där den subkortikala vita substansen (U-fibrerna) är bevarad. Detta mönster ses vid många sjukdomar, inklusive MLD, och är därför jämförelsevis ospecifikt. Mildt onormala signaler runt de laterala ventriklarna ses också vid kortikaldegeneration, särskilt neuronala ceroid lipofuscinoser som utvecklas efter barndomen.
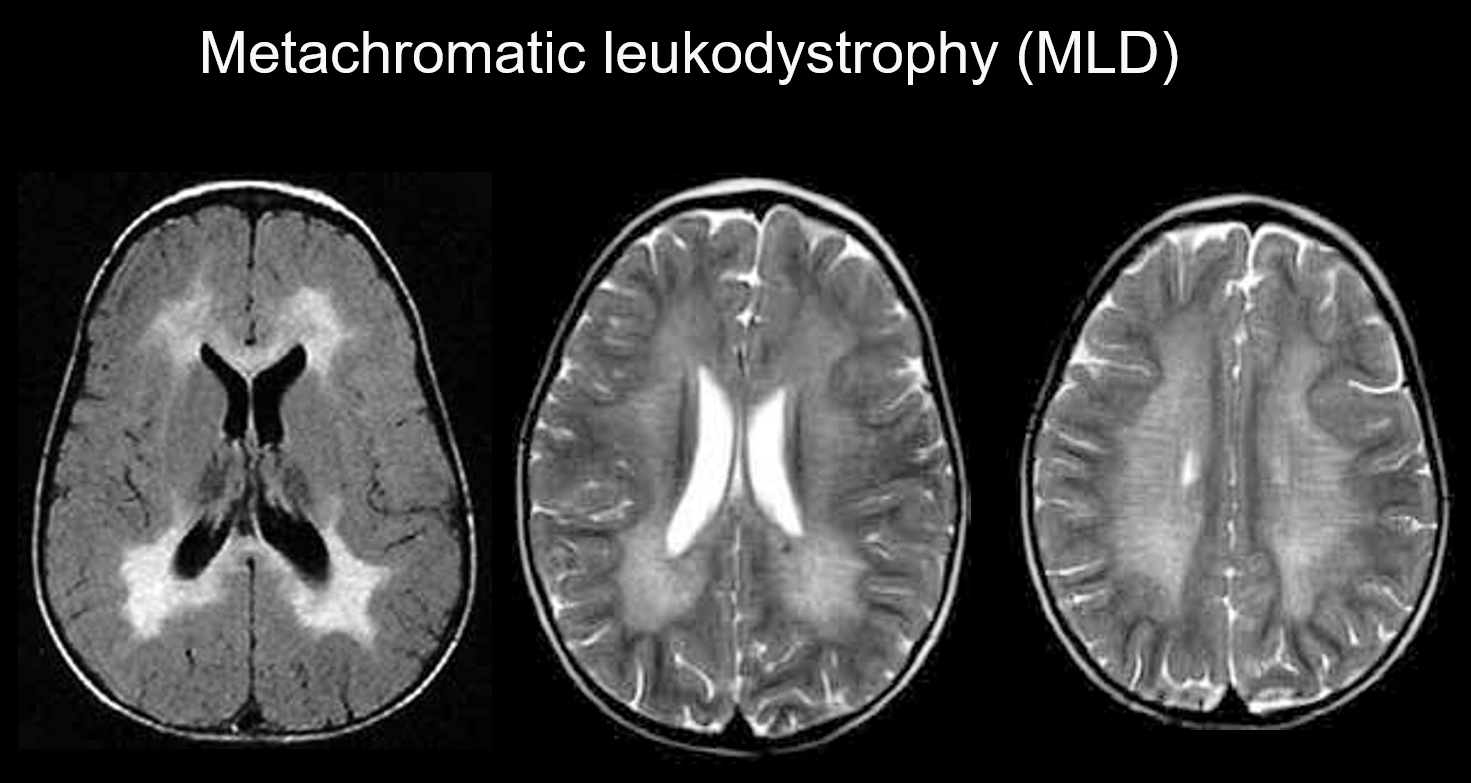
(a) Metachromatisk leukodystrofi.
Metachromatisk leukodystrofi är en autosomalt recessivt nedärvd sjukdom (lysosomal lagringssjukdom) som orsakas av arylsulfatas-A-brist (kromosom 22q13.31), där ackumulationen av mycket giftigt sulfatid leder till demyelinisering. Beroende på den ålder vid vilken den uppträder klassificeras den som medfödd, infantilt debut, juvenil debut eller vuxen debut. Symtomen omfattar kognitiv tillbakagång, spastisk pares, ofrivilliga rörelser, perifer neuropati och atrofi av synnerven. Den visar sig på T2-viktade bilder som hyperintensiviteter i den vita substansen, främst runt de laterala ventriklarna, och på T1-viktade bilder som milda hypointensiviteter. Läsionerna tenderar att vara övervägande i frontalloben. Band med normal intensitet (tiger stripes) kan vara tydliga inom de utbredda onormala signalerna i den vita substansen (figur 5). Dessa tros bero på det partiella bevarandet av myelinskidan i det perivaskulära utrymmet och på ackumulering av nedbrytningsprodukter från myelinskidan i makrofager.
5. Subkortikal dominans
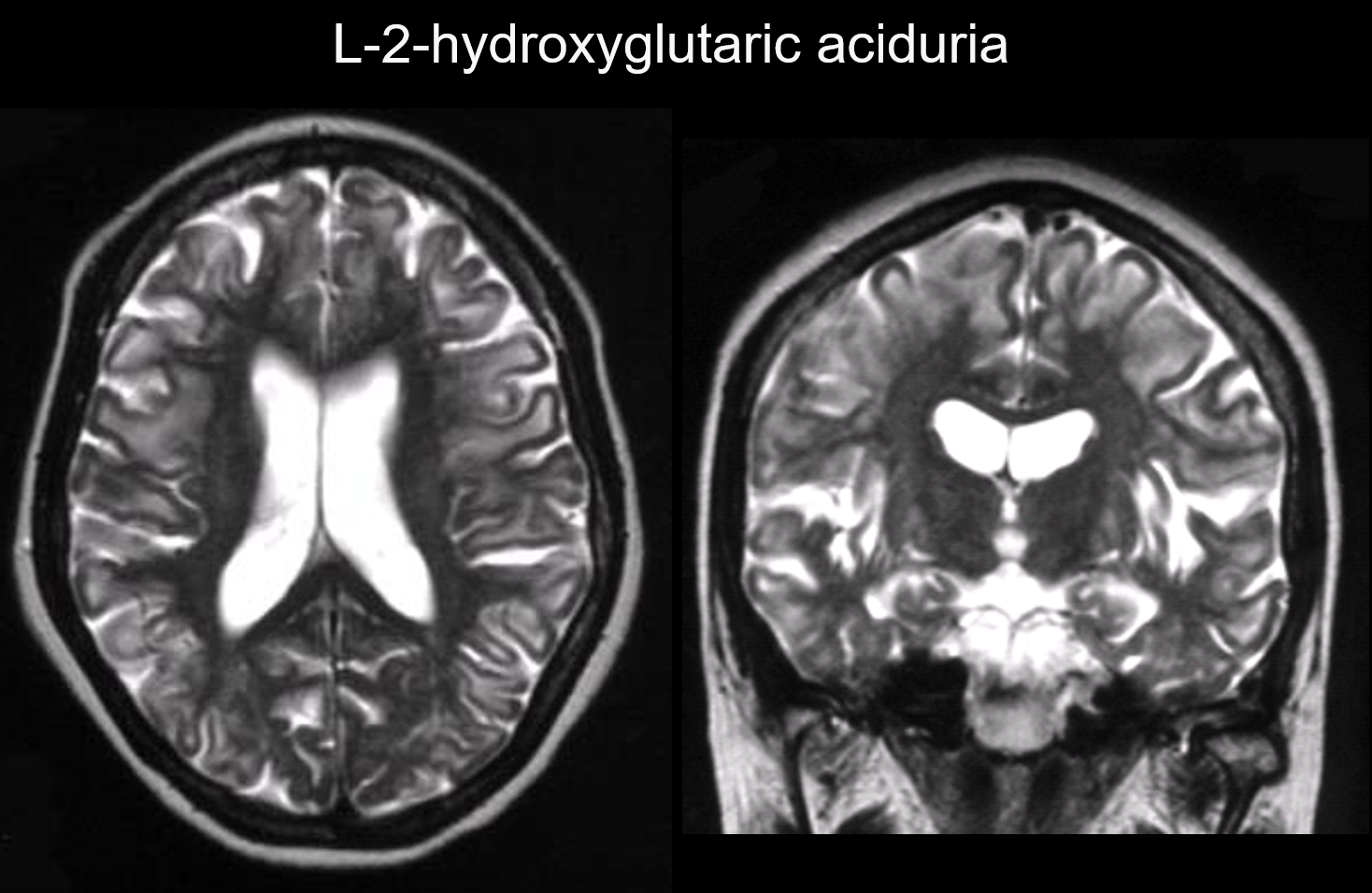
I dessa sjukdomar förekommer lesioner främst i den subkortikala vita substansen, inklusive U-fibrerna. Sjukdomar med detta mönster är bland annat L-2-hydroxyglutarsyrauria (figur 6), galaktosemi, Kearns-Sayers syndrom, propionakemi, störningar i ureacykeln och Canavans sjukdom i ett tidigt skede.
6. Diffus cerebral
I dessa sjukdomar uppträder onormala signaler i hela den vita substansen i hjärnan. De uppvisar starka T2-hyperintensiteter jämfört med de T2-signaler som produceras av icke-myeliniserad vit substans (hypomyelinisering). Förutom fall av megalencefalisk leukoencefalopati med subkortikala cystor och leukoencefalopati med försvinnande vit substans uppvisar patienter med alla typer av sjukdomar i vit substans så småningom detta mönster när sjukdomen fortskrider.
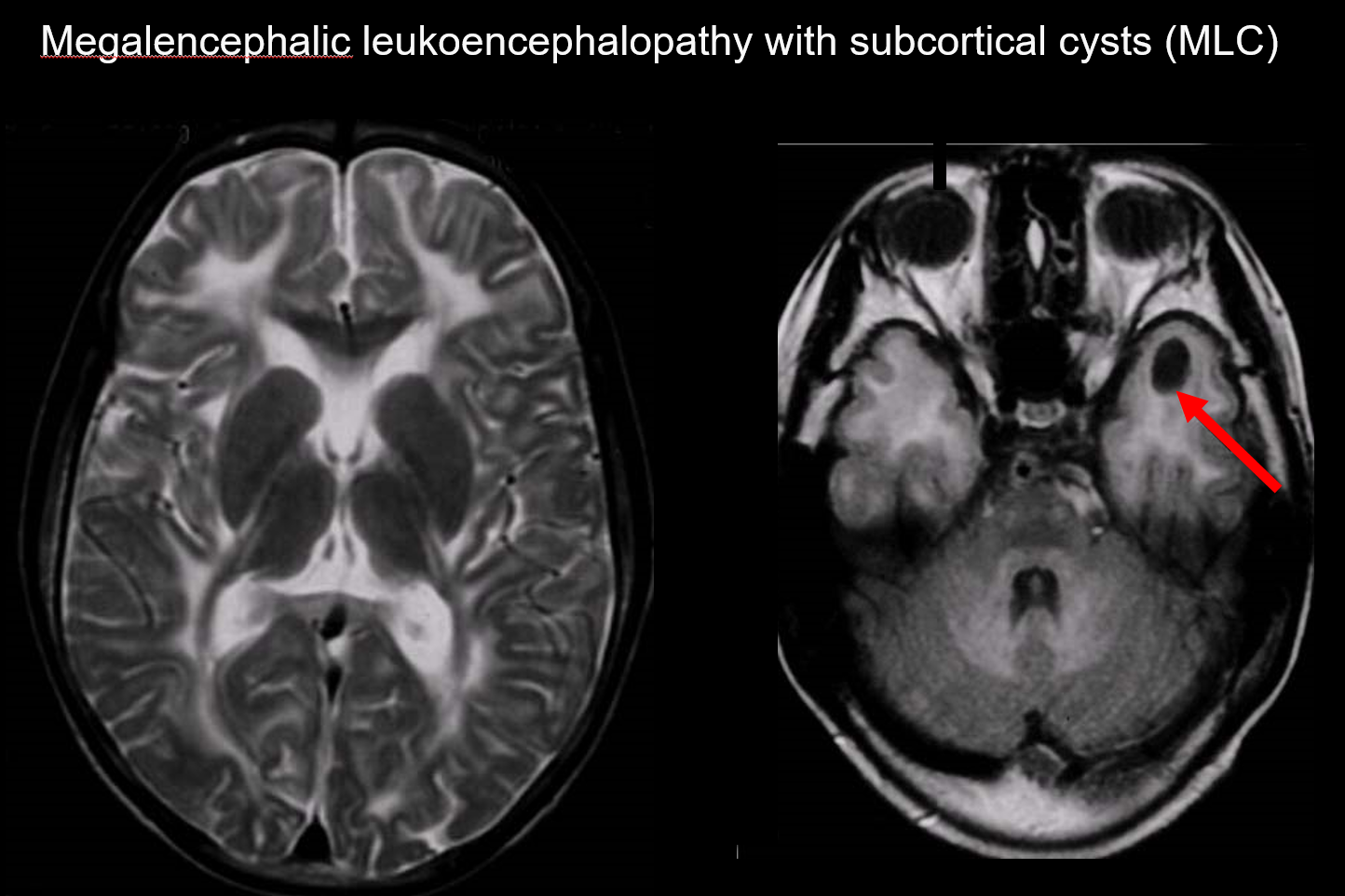
(a) Megalencefalisk leukoencefalopati med subkortikala cystor (MLC)
MLC är en autosomalt recessivt nedärvd sjukdom som orsakas av en abnormitet i MLC1-genen, och dess debut i spädbarnsåldern kännetecknas av megalocefali, långsamt fortskridande motorisk försämring, ataxi och spasticitet. MRT avslöjar karakteristiska utbredda onormala signaler i den vita substansen och mild svullnad av den vita substansen samt cystbildning i de parietala och temporala loberna (figur 7).7, 8) T1-viktad och T2-viktad avbildning avslöjar onormal vit substans, medan cystorna alla uppvisar T1-hypointensitet och T2-hyperintensitet, vilket gör dem särskilt svåra att upptäcka. FLAIR-avbildning, som visualiserar cystor (vatten) som hypointensiteter, är värdefull för dess diagnostik. Den är vanligare bland japaner än vacuolating megalencephalic leukoencephalopathy.
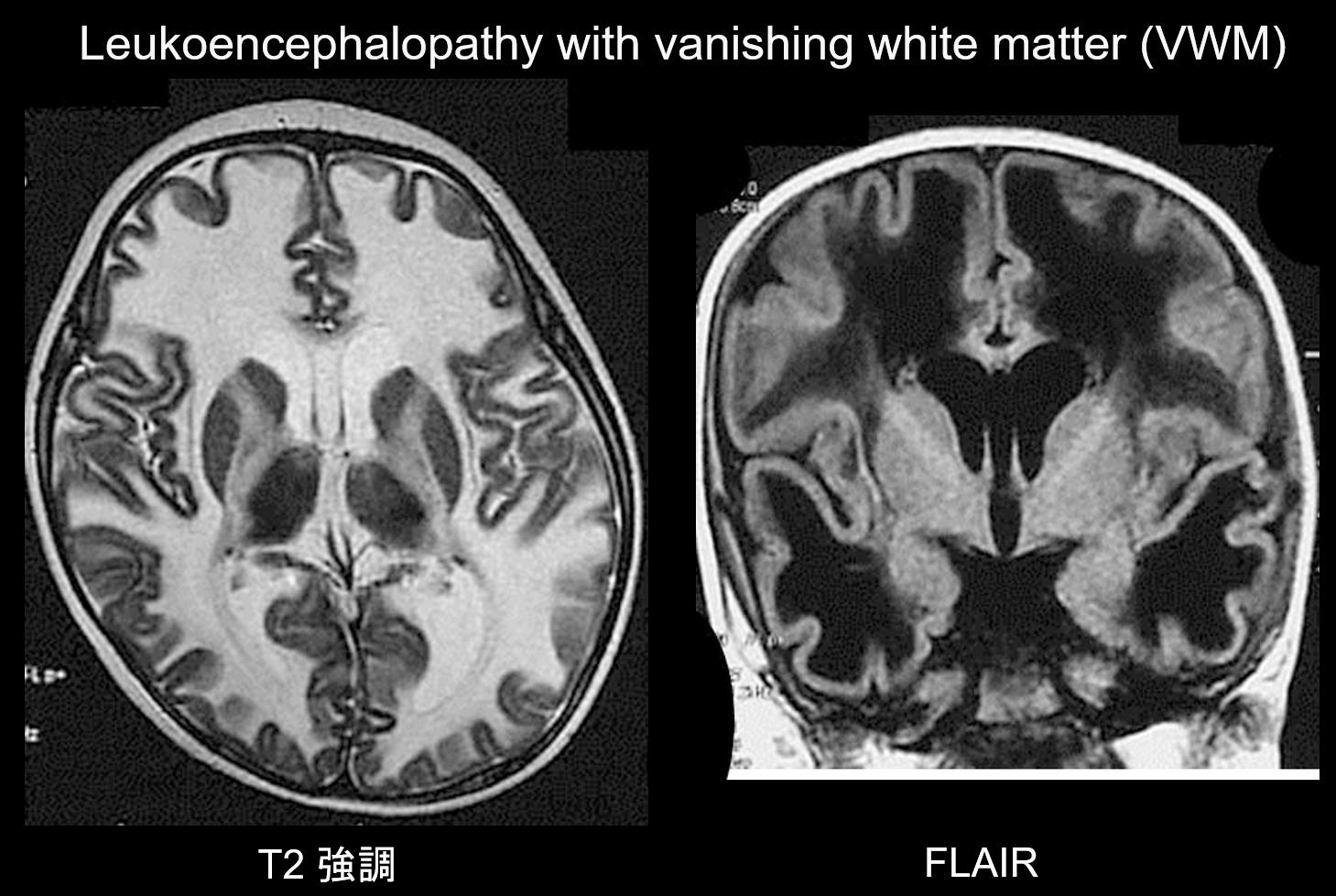
(b) Leukoencefalopati med försvinnande vit substans.
Leukoencefalopati med försvinnande vit substans (VWM) är en autosomalt recessivt nedärvd sjukdom som orsakas av en brist på eIF2B, ett protein som är associerat med eIF2, som överför initiator tRNA till ribosomer. eIF2B består av fem olika proteiner, som alla har olika genetiska loci. VWM har visat sig vara samma sjukdom som childhood cerebellar ataxia and central hypomyelination (CACH). Patienterna är normala under neonatalperioden och den tidiga spädbarnstiden, men efter insjuknandet (vanligtvis vid 2-6 års ålder) utvecklar de långsamt progressiv kognitiv regression, spasticitet och ataxi. Dessa symtom är kända för att förvärras av infektioner eller mindre trauman. Den cerebrala vita substansen uppvisar utbredd T2-hyperintensitet och T1-hypointensitet och ersätts gradvis av vätska med tiden (som namnet antyder försvinner den vita substansen) (figur 8). Den cystiska vita substansen innehåller bandstrukturer som tros representera den kvarvarande vävnaden. Onormala signaler ses också i hjärnstammen, särskilt i den centrala tegmentala trakten. FLAIR-avbildning är värdefull för diagnosen av denna sjukdom.
7. Predominans eller prominens i bakre fossa
Dessa störningar kännetecknas av lesioner främst i hjärnstammen och lillhjärnan. Läsioner i den vita substansen i lillhjärnan kan orsakas av sjukdomar som cerebrotendinös xanthomatos (CTX), peroxisomala sjukdomar, Alexanders sjukdom, leukoencefalopati med involvering av hjärnstam och ryggmärg och laktatförhöjning (LBSL), lönnsirapurinsjuka, histiocytos samt heroin- och kokaintoxicitet. Läsioner i hjärnstammen kan orsakas av sjukdomar som Alexanders sjukdom, LSBL och adult polyglucosan disease. Läsioner i mellersta lillhjärnan ses vid fragilt X-syndrom och vuxen autosomal dominant leukodystrofi relaterad till en lamin B1-duplikation.
8. Multifokala lesioner
I motsats till störningar som ger upphov till de konfluenta lesioner som beskrivs i 2-7 ovan resulterar störningarna i detta avsnitt i multifokala (utspridda) lesioner. De omfattar infektioner som TORCH-syndromet (på grund av kongenital cytomegalovirusinfektion eller annan orsak) och brucellos; inflammatoriska sjukdomar som akut disseminerad encefalomyelit (ADEM), multipel skleros (MS) och neuromyelitis optica (NMO); Vaskulopatier som cerebral autosomalt dominerande arteriopati med subkortikala infarkter och leukoencefalopati (CADASIL), ateroskleros, amyloid angiopati, COL4A1-associerad cerebral småkärlssjukdom, Fabrys sjukdom och Susacs syndrom; och ärftliga tillstånd som mitokondriell sjukdom, L-2-hydroxyglutarsyrauria, mukopolysackaridos (MPS) och kromosomavvikelser (t.ex. 6p-syndrom).
9. Lesioner med låg diffusionsförmåga
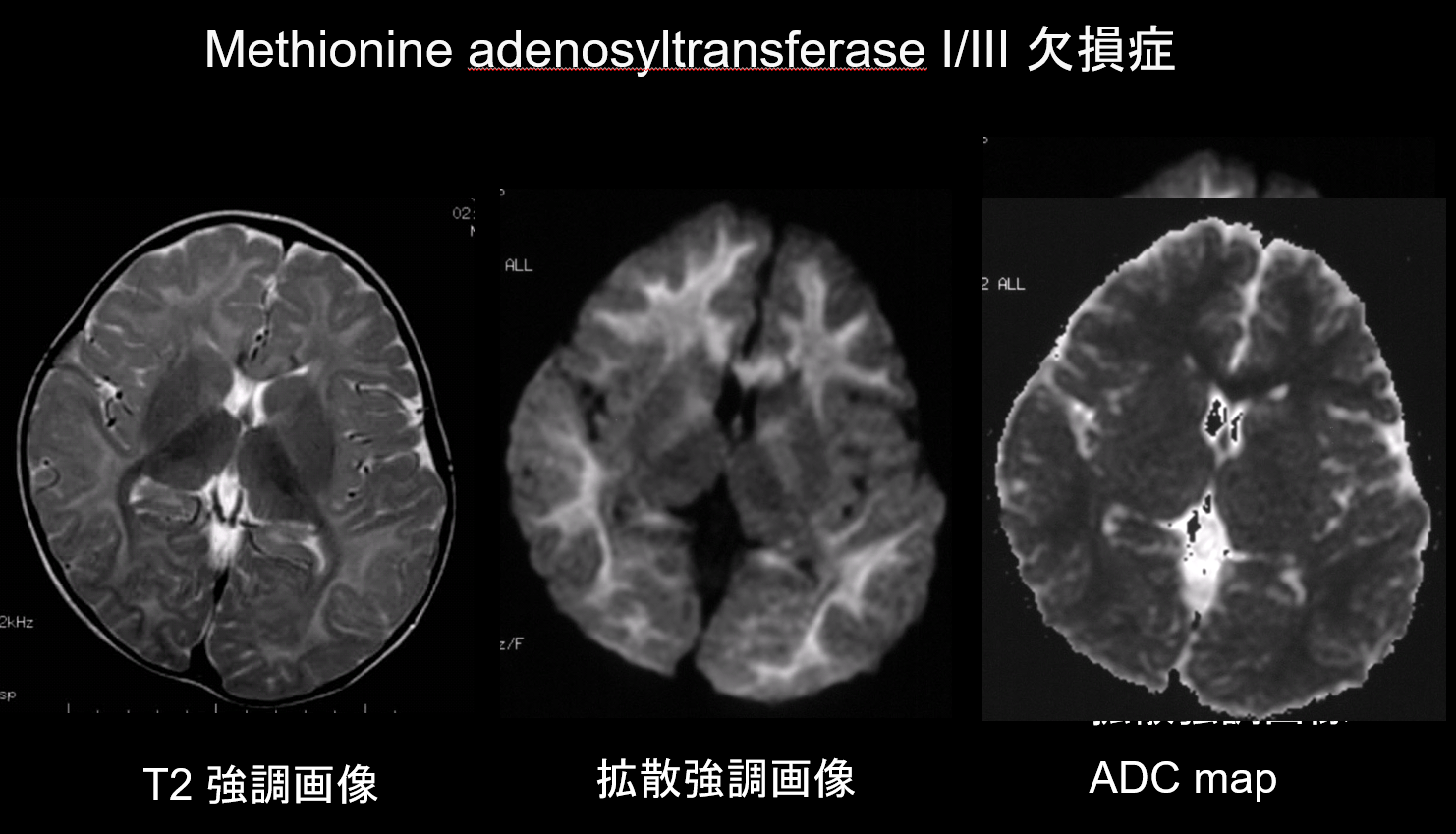
I både demyelinisering och hypomyelinisering, de viktigaste patologierna för sjukdomar i den vita substansen, minskar mängden myelin, vilket begränsar diffusionen, och motsvarande ökning av extracellulär vätska resulterar i T2-hyperintensiviteter med en hög skenbar diffusionskoefficient (ADC). Det är sällsynt att sjukdomar i den vita substansen uppvisar både T2-hyperintensiviteter och låg ADC, och denna kombination har därför ett högt diagnostiskt värde. Störningar som kännetecknas av förekomst av intramyeliniskt ödem i myelinskidan och i mellanrummen mellan skidorna uppvisar en låg ADC. De omfattar bl.a. lönnsirapurins sjukdom, brist på metioninadenosyltransferas I/III (figur 9), fenylketonuri, icke-ketotisk hyperglycinemi och Canavans sjukdom. Krabbes sjukdom och metakromatisk leukodystrofi kan också uppvisa låg ADC i vissa lesioner i den vita substansen, eftersom intramyeliniskt ödem kan uppstå under den akuta fasen av demyelinisering.
- Van der Knaap MS, Valk J. Classification of myelin disorders. I Van der Knaap MS, Valk J, eds. Magnetisk resonans av myelinisering och myelinstörningar. 3rd ed. Berlin: Springer, 2005, 20-24.
- Schiffmann R, van der Knaap MS. Ett MRT-baserat tillvägagångssätt för diagnostik av sjukdomar i den vita substansen. Neurology 2009; 72: 750-759
- Takanashi J. Diagnostic imaging of white matter disorders. Journal of the Japan Pediatric Society 2007; 111: 1243-1254.
- Van der Knaap MS, Breiter SN, Naidu S, et al. Definition och kategorisering av leukoencefalopatier av okänt ursprung: MR-avbildning. Radiology 1999; 213: 121-133.
.