Modification of Winkler’s method for determination of dissolved oxygen concentration in small sample volumes
Erstveröffentlicht am 27. August 2010
Die Methode von Winkler ist das gängigste Verfahren zur Bestimmung der Konzentration von gelöstem Sauerstoff (DO) in Wasserproben. Diese Methode erfordert jedoch ein relativ großes Probenvolumen von 200 mL für eine genaue DO-Bestimmung. Es wurden viele alternative Methoden zur Messung der DO-Konzentration in kleinen Probenvolumina vorgeschlagen, aber die meisten dieser Methoden haben entweder das Problem der geringen Genauigkeit, der hohen Kosten, der komplizierten Instrumentierung oder der langen Analysezeiten. In diesem Beitrag wird eine einfache Modifikation der Winkler-Methode zur Messung der DO-Konzentration in Proben mit einem Volumen von 1 mL vorgeschlagen. Die vorgeschlagene Methode ist genau, kostengünstig, einfach und schnell. Die DO-Konzentrationen wurden in 33 Proben sowohl mit der herkömmlichen Winkler-Methode (WM) als auch mit der vorgeschlagenen Methode (PM) gemessen. Bei 23 der 33 analysierten Proben konnte die Hypothese, dass die Mittelwerte der Messungen in der Bevölkerung gleich sind (μ1 = μ2), bei einem Konfidenzniveau von 95 Prozent nicht zurückgewiesen werden, und bei 19 Proben konnte die Hypothese, dass die Varianzen der Messungen in der Bevölkerung gleich sind (σ21 = σ22), bei einem Konfidenzintervall von 95 Prozent nicht zurückgewiesen werden. Daraus wurde gefolgert, dass die DO-Messungen mit WM und PM in den meisten Fällen sowohl in Bezug auf die Genauigkeit als auch auf die Präzision vergleichbare Ergebnisse liefern.
Einführung
Die Winkler-Methode (Methode Nr. 4500-O-C)1 hat sich allgemein als genaue und zuverlässige Methode2 für die Messung der Konzentration von gelöstem Sauerstoff (DO) in einer Vielzahl von Wasserproben durchgesetzt. Diese Methode gilt als Maßstab für die DO-Bestimmung. Der größte Nachteil dieser Methode ist jedoch, dass ein großes Probenvolumen von 200 ml erforderlich ist.3
Zahlreiche alternative Methoden wurden ebenfalls für die Messung des DO entwickelt. Diese Methoden lassen sich in drei Kategorien einteilen: (1) kolorimetrische Methoden, (2) Methoden mit Gaschromatographie und (3) Methoden mit elektrochemischen und optischen Sensoren. Die kolorimetrischen Methoden können für die Bestimmung von DO in kleinen Probenmengen verwendet werden. Sie haben jedoch Nachteile wie die Notwendigkeit teurer (z. B. Goldsol) oder giftiger (z. B. Zyanid) chemischer Reagenzien.4 Ein weiterer einschränkender Faktor für solche Methoden ist das Fehlen einer angemessenen Begründung für die Wahl der Messwellenlänge.5 Die DO-Bestimmung ist auch mit der Gaschromatographie möglich. Gaschromatografische Methoden sind zwar genau und erfordern kleine Probenmengen, sind aber zeitaufwändig und teuer. Elektrochemische Sensoren sind für die DO-Messung weit verbreitet, und ihre Vor- und Nachteile wurden an anderer Stelle besprochen.6 Elektrochemische Sensoren leiden im Allgemeinen unter irreversiblen Druckeffekten, Verunreinigung durch Schwefelwasserstoff und Querempfindlichkeit.7 Außerdem verbrauchen sie während der Messung DO und sind daher für sehr kleine Probenmengen möglicherweise ungeeignet. In jüngster Zeit liegt der Schwerpunkt auf der Entwicklung optischer Sensoren, die auf dem Prinzip der dynamischen Sauerstofflumineszenzlöschung beruhen.8 Diese optischen Sensoren sind einfach zu bedienen, haben eine schnelle Ansprechzeit und sind langlebig. Allerdings erfordern alle Sensoren, ob elektrochemisch oder optisch, eine Kalibrierung nach der Winkler-Methode, da sie temperatur- und druckempfindlich sind.9,10 Außerdem sind sie empfindlich gegenüber Bio-Fouling und Bakterienwachstum auf der Sensoroberfläche.8
Aufgrund der oben beschriebenen inhärenten Einschränkungen alternativer Methoden und ihrer Abhängigkeit von der Winkler-Methode zur Gegenkontrolle und Kalibrierung wurden auch mehrere Modifikationen der Winkler-Methode selbst für die Messung von DO-Konzentrationen in Probenvolumina von 1-10 ml vorgeschlagen.11,12,13 Solche „Mikro-Winkler“-Methoden sind jedoch aufgrund der komplexen instrumentellen Anforderungen und der aufwändigen Vorsichtsmaßnahmen, die erforderlich sind, um die Kontamination der Proben durch den Austausch mit Luftsauerstoff zu vermeiden, nicht sehr beliebt. Diese Methoden wurden an anderer Stelle kritisch geprüft.14 Kürzlich wurde eine gravimetrische Mikro-Winkler-Titrierungsmethode15 für die DO-Messung in kleinen Proben vorgeschlagen. Dieses Verfahren erfordert jedoch mehrere und genaue gravimetrische Messungen unter Verwendung einer empfindlichen Waage und scheint daher recht komplex zu sein.
Aus der Literaturübersicht geht hervor, dass fast alle für die DO-Messung in kleinen Proben entwickelten Methoden auf die eine oder andere Weise mangelhaft sind. Daher besteht ein ständiger Bedarf an der Entwicklung einer besseren, d.h. genauen, präzisen, kostengünstigen, einfachen und schnellen Methode zur DO-Messung in kleinen Probenvolumina.
Kurzbeschreibung der vorgeschlagenen Methode
Die größte Herausforderung bei der Messung der DO-Konzentration in kleinen Proben ist die Verhinderung einer Kontamination der Proben durch Wechselwirkung mit der Atmosphäre. Es wird vorgeschlagen, eine isolierende Flüssigkeitsschicht zwischen der Wasserprobe und der Atmosphäre einzubringen. Erforderliche Eigenschaften der Isolierflüssigkeit sind: Wasserunmischbarkeit, eine geringere Dichte als Wasser und eine vernachlässigbare Sauerstoffauflösungskapazität. Es wird vorgeschlagen, die Isolierflüssigkeit in ein Fläschchen zu geben und die Wasserprobe, deren DO bestimmt werden soll (1 mL Volumen), direkt unter die Isolierflüssigkeitsschicht zu bringen. Durch diesen Schritt wird die Wasserprobe wirksam von der Atmosphäre abgeschottet. Der DO-Wert in der Wasserprobe kann dann fixiert und mit denselben Reagenzien wie bei der Winkler-Methode in eine äquivalente Menge Iod umgewandelt werden. Die Jodlösung wird dann mit einer Spritze aus dem Fläschchen extrahiert und mit Na2S2O3 titriert, um die DO-Konzentration in der Probe zu bestimmen.
Nach mehreren Versuchsreihen wurde n-Hexan als Isolierflüssigkeit wie oben beschrieben ausgewählt. n-Hexan ist leichter als Wasser (spezifisches Gewicht = 0,7) und mit Wasser praktisch nicht mischbar. Die Löslichkeit von Sauerstoff in n-Hexan beträgt 0,002 Molenbruch,16 d.h. Sauerstoff ist in n-Hexan praktisch unlöslich.
Material und Methoden
Alle verwendeten Reagenzien waren von analytischer Reagenzienqualität (>99% Reinheit, Loba Chemicals, Indien). Für die Herstellung der Reagenzien und die Verdünnung der Proben wurde entionisiertes Wasser (Milli-Q, Millipore, USA) verwendet. Das verwendete n-Hexan war von HPLC-Qualität (>99% Reinheit, Merck, Indien). In dieser Studie wurden Borosilikatglasgeräte verwendet. MnSO4- und Alkali-Azid-Iodid-Lösungen wurden nach Standardmethoden (Methode Nr. 4500-O C) hergestellt.1
Das DO-Messverfahren nach der vorgeschlagenen Methode (PM) war wie folgt. Zunächst wurden 0,5 mL n-Hexan in ein 16 mL Glasfläschchen (Wheaton Science, USA) überführt. Dann wurde 1 mL n-Hexan in eine 2-mL-Pipette gegeben, und die Pipette wurde mit 1 mL der Wasserprobe gefüllt, deren DO-Konzentration bestimmt werden sollte. Durch das oben beschriebene Verfahren zur Probenentnahme wurde sichergestellt, dass die Probe ohne einen Kopfraum entnommen wurde. Dieser Schritt der Probenentnahme ist der wichtigste, da das Auftreten von Blasen oder Luftspalten an der Hexan-Wasser-Grenzfläche oder an anderer Stelle in der Pipette zu Fehlern führen kann. Die Öffnung der Pipette wurde dann unterhalb der Hexanschicht im Fläschchen platziert, so dass die Probe unterhalb der Hexanschicht eingebracht wurde, wodurch jeglicher Kontakt zwischen der Probe und der Atmosphäre vermieden wurde. Die Probenentnahme in der Pipette und das Aufbringen der Probe unterhalb der Hexanschicht im Fläschchen müssen so schnell wie möglich erfolgen, um Fehler zu minimieren. Anschließend wurden 5 μL MnSO4 mit einer 10 μL-Mikrospritze (Hamilton, USA) in die Wasserprobe unterhalb der Hexanschicht eingebracht, gefolgt von einer ähnlichen Zugabe von 5 μL Alkali-azid-Iodid-Lösung. Die Präzipitatbildung setzte unmittelbar nach den Zugaben ein und war innerhalb von 3 min abgeschlossen. Anschließend wurden 0,1 mL konz. H2SO4 mit einer Mikropipette zu dem unter der Hexanschicht gebildeten Niederschlag gegeben. Der Niederschlag wurde innerhalb von 3 min aufgelöst und es bildete sich eine gelbe Iodlösung unter der Hexanschicht. Genau 1 mL der Iodlösung wurde mit einer Mikrospritze aus der Hexanschicht extrahiert und in ein 25-mL-Becherglas überführt. Die 1 mL Iodlösung im Becherglas wurde durch Zugabe von entionisiertem Wasser auf ∼10 mL verdünnt, um die Titration zu erleichtern. Durch die Zugabe von entionisiertem Wasser wird die Iodlösung lediglich verdünnt, ohne die Iodmenge im Becherglas zu verändern. Der Inhalt des Becherglases wurde mit 0,00625 M Na2S2O3-Lösung titriert. 1 mL dieses Titriermittels entspricht 55,5 mg L-1 des DO in der ursprünglichen Probe. Das Titriermittel wurde in einer 250 μL-Mikrospritze (Hamilton, USA) aufgezogen und unter ständigem Rühren tropfenweise in das Becherglas gegeben, bis die gelbe Farbe des Iods fast verschwunden war. Dann wurden 1-2 Tropfen Stärkelösung hinzugefügt und die Titration fortgesetzt, bis die blaue Farbe der Stärke verschwunden war. Anhand des Volumens des Titriermittels, das für eine bestimmte Titration benötigt wurde, wurde die DO-Konzentration in der ursprünglichen Probe berechnet.
Die DO-Konzentration wurde in verschiedenen Proben auch mit der Winkler-Methode (WM) bestimmt. Der Reagenzienbedarf und andere Details der beiden Methoden sind in Tabelle 1 dargestellt.
| Proben-Nr. | Reagenz | Menge | Stärke | ||
|---|---|---|---|---|---|
| WM | PM | WM | PM | ||
| Probe | 200 mL | 1 mL | – | – | |
| MnSO4 | 1 mL | 5 μL | nach WM | ||
| Alkali-Azid-Jodid-Reagenz | 1 mL | 5 μL | wie pro WM | ||
| Na2S2O3 | wie erforderlich | wie erforderlich | 0.025M | 0.00625M | |
| H2SO4 | 1 mL | 0.1 mL | Nach WM | ||
| Stärke | 1-2 Tropfen | 1-2 Tropfen | Nach WM | ||
| n-Hexan | Nicht verwendet | 1.5 mL | – | – | |
Ergebnisse und Diskussion
Die DO-Konzentration wurde in 33 Wasserproben (siehe Tabelle 2) gemessen, die an verschiedenen Orten in und um die Stadt Kanpur, Indien, gewonnen wurden. Von den 33 Proben waren 8 Leitungswasserproben, 16 Flusswasserproben, 6 mit Leitungswasser verdünnte Haushaltsabwasserproben, 2 Grundwasserproben und 1 Teichwasserprobe. Die Proben wurden so ausgewählt, dass die DO-Konzentrationen in einer Vielzahl von Probenmatrices gemessen werden konnten. Für jede Probe wurden mehrere DO-Wiederholungsmessungen durchgeführt, sowohl mit dem WM als auch mit dem PM. Die berechneten Probenmittelwerte (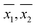 ), Probenstandardabweichungen (S1, S2) und die Anzahl der Wiederholungsmessungen (n1, n2) für WM bzw. PM sind in Tabelle 2 für jede Probe dargestellt.
), Probenstandardabweichungen (S1, S2) und die Anzahl der Wiederholungsmessungen (n1, n2) für WM bzw. PM sind in Tabelle 2 für jede Probe dargestellt.
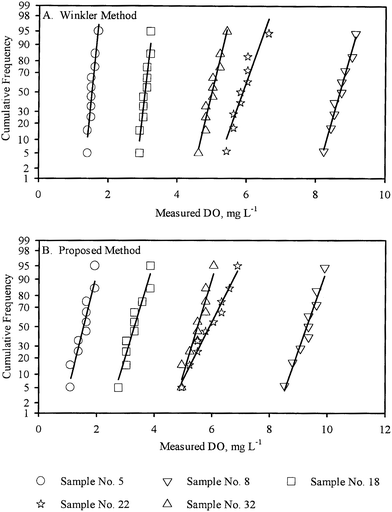
Die Normaldiagramme der Sätze von Wiederholungsmessungen mit beiden Methoden waren alle annähernd linear, was darauf hindeutet, dass die Wiederholungsmessungen normalverteilt waren und daher eine weitere statistische Analyse auf dieser Grundlage möglich war. Zur Veranschaulichung sind in Abb. 1A die Normalkurven für fünf mit dem WM durchgeführte Probenmessungen dargestellt. Die Normaldiagramme für dieselben fünf Probenmessungen, die mit dem PM durchgeführt wurden, sind in Abb. 1B dargestellt.
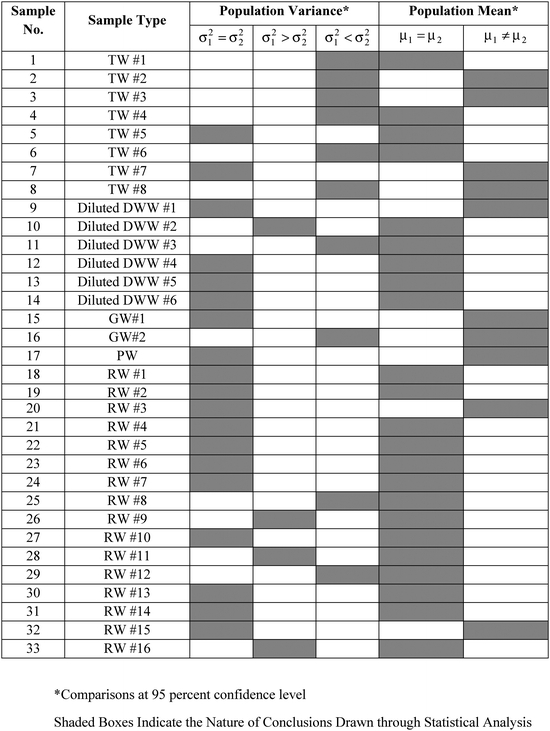
Die Varianzen (S21,S22) in den Wiederholungsmessungen einer Probe durch WM bzw. PM wurden für den paarweisen Vergleich der entsprechenden Populationsvarianzen (σ21,σ22) unter Verwendung des F-Tests verwendet. Von den 33 Proben, bei denen der DO mit den beiden Methoden (WM und PM) gemessen wurde, konnte die Hypothese, dass die Varianzen der Populationen gleich sind (σ21 = σ22), bei einem Konfidenzniveau von 95 % für 19 Proben nicht zurückgewiesen werden. Darüber hinaus konnte die Hypothese σ21 > σ22 für 4 Stichproben nicht zurückgewiesen werden, während die Hypothese σ21 < σ22 für die übrigen 10 Stichproben nicht zurückgewiesen werden konnte, alle bei einem Konfidenzniveau von 95 Prozent. Diese Ergebnisse sind in Tabelle 3 zusammengefasst.
Weiterhin wurden die Stichprobenvarianzen (S21, S22) und Stichprobenmittelwerte (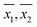 ) für jede Stichprobe, wie sie von WM bzw. PM ermittelt wurden, für den paarweisen Vergleich der entsprechenden Populationsmittelwerte (μ1, μ2) verwendet. Für Stichproben mit gleichen Varianzen (siehe Tabelle 3) wurde der paarweise Vergleich mit dem Student’s t-Test durchgeführt. Bei Proben mit ungleichen Varianzen (siehe Tabelle 3) wurde der paarweise Vergleich mit dem t-Test für ungleiche Varianzen durchgeführt.17 Bei 23 der 33 Proben, bei denen die DO-Messungen sowohl mit WM als auch mit PM durchgeführt wurden, konnte die Hypothese, dass die Populationsmittelwerte gleich sind (μ1 = μ2), bei einem 95-prozentigen Konfidenzniveau nicht zurückgewiesen werden.
) für jede Stichprobe, wie sie von WM bzw. PM ermittelt wurden, für den paarweisen Vergleich der entsprechenden Populationsmittelwerte (μ1, μ2) verwendet. Für Stichproben mit gleichen Varianzen (siehe Tabelle 3) wurde der paarweise Vergleich mit dem Student’s t-Test durchgeführt. Bei Proben mit ungleichen Varianzen (siehe Tabelle 3) wurde der paarweise Vergleich mit dem t-Test für ungleiche Varianzen durchgeführt.17 Bei 23 der 33 Proben, bei denen die DO-Messungen sowohl mit WM als auch mit PM durchgeführt wurden, konnte die Hypothese, dass die Populationsmittelwerte gleich sind (μ1 = μ2), bei einem 95-prozentigen Konfidenzniveau nicht zurückgewiesen werden.
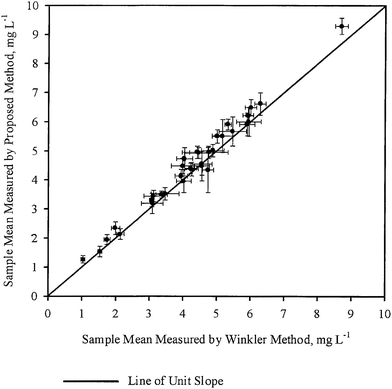
Die Probenmittelwerte (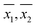 ) für jede Probe, die mit WM bzw. PM ermittelt wurden, wurden in Abb. 2 gegeneinander aufgetragen. Die in der Abbildung gezeigten Fehlerbalken entsprechen den entsprechenden 95 %-Konfidenzintervallen. Eine Linie mit einheitlicher Steigung, die durch den Ursprung verläuft, wurde ebenfalls in dieselbe Abbildung eingezeichnet. Es wurde festgestellt, dass alle Punkte sehr nahe an der Geraden mit einheitlicher Steigung liegen, was mit den allgemeinen Schlussfolgerungen in Tabelle 3 übereinstimmt, d. h. für die meisten Proben sind die mit den beiden Methoden ermittelten mittleren DO-Konzentrationen statistisch nicht unterschiedlich. Somit war in den meisten Fällen die DO-Messung durch PM genauso genau wie die DO-Messung durch WM.
) für jede Probe, die mit WM bzw. PM ermittelt wurden, wurden in Abb. 2 gegeneinander aufgetragen. Die in der Abbildung gezeigten Fehlerbalken entsprechen den entsprechenden 95 %-Konfidenzintervallen. Eine Linie mit einheitlicher Steigung, die durch den Ursprung verläuft, wurde ebenfalls in dieselbe Abbildung eingezeichnet. Es wurde festgestellt, dass alle Punkte sehr nahe an der Geraden mit einheitlicher Steigung liegen, was mit den allgemeinen Schlussfolgerungen in Tabelle 3 übereinstimmt, d. h. für die meisten Proben sind die mit den beiden Methoden ermittelten mittleren DO-Konzentrationen statistisch nicht unterschiedlich. Somit war in den meisten Fällen die DO-Messung durch PM genauso genau wie die DO-Messung durch WM.
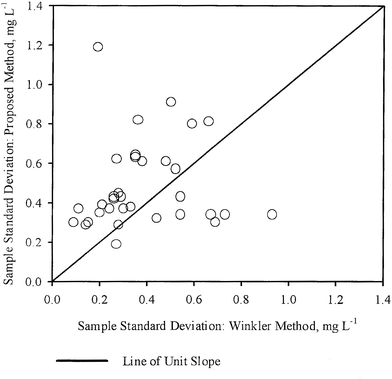
Die Standardabweichungen (S1, S2) für jede Probe, die durch WM bzw. PM ermittelt wurden, wurden in Abb. 3 gegeneinander aufgetragen. In derselben Abbildung wurde auch eine Linie mit einheitlicher Steigung eingezeichnet, die durch den Ursprung verläuft. In diesem Fall scheinen die Punkte ziemlich gleichmäßig in Bezug auf die Linie der Einheitssteigung verteilt zu sein, wobei einige Punkte nahe an der Linie liegen, während die anderen weiter entfernt sind. Diese Beobachtungen stimmen auch mit den Schlussfolgerungen aus Tabelle 3 überein, d.h. für die meisten Proben sind die Unterschiede in der DO-Konzentration, die mit den beiden Methoden gemessen wurden, statistisch nicht unterschiedlich. In den meisten Fällen war also die DO-Messung mit PM genauso genau wie die DO-Messung mit WM.
Es wurde festgestellt, dass die vorgeschlagene Methode (PM) bei sorgfältiger Probenhandhabung und Titration sowohl in Bezug auf die Genauigkeit als auch auf die Präzision mit der Winkler-Methode (WM) vergleichbare Ergebnisse liefern kann. Nichtsdestotrotz kann die Genauigkeit der DO-Bestimmung durch PM wahrscheinlich durch die Verwendung einer Mikrospritze mit einer geringeren Mindestanzahl für die abschließende Titration erhöht werden. Die in dieser Studie verwendete Mikrospritze hatte eine Mindestmenge von 5 μL, was unter den Bedingungen der vorliegenden Studie einer Unsicherheit von ∼0,25 mg L-1 DO entspricht. Diese Unsicherheit kann durch die Verwendung einer Mikrospritze mit einer geringeren Mindestanzahl verringert werden.
Schlussfolgerungen
Das Ziel dieser Studie war die Entwicklung einer genauen, kostengünstigen, einfachen und schnellen Methode zur Messung des DO in kleinen Probenmengen. Auf der Grundlage der vorgelegten Ergebnisse und Analysen kann der Schluss gezogen werden, dass die vorgeschlagene Methode die meisten der oben genannten Probleme angeht. Die wichtigsten Schlussfolgerungen der Studie waren die folgenden:
➢ Die Einführung einer isolierenden Schicht aus n-Hexan zur Verhinderung des Sauerstofftransfers zwischen der wässrigen Probe und der Atmosphäre führt zu einer konsistenten und genauen Bestimmung des DO in kleinen Probenvolumina. Dies ist die wichtigste Neuerung der vorgeschlagenen Methode.
➢ Es wurde auch gezeigt, dass die vorgeschlagene Methode (PM) durch angemessene Vorsichtsmaßnahmen im Allgemeinen Ergebnisse liefern kann, die statistisch mit den Ergebnissen der Winkler-Methode (WM) vergleichbar sind, sowohl in Bezug auf die mittlere DO-Konzentration als auch in Bezug auf die Varianz der DO-Konzentration um den Mittelwert.
➢ Die Anforderungen an Reagenzien und Glasgeräte sind bei der vorgeschlagenen Methode geringer als bei der Winkler-Methode, was in erster Linie auf das geringere Probenvolumen zurückzuführen ist. n-Hexan ist das einzige zusätzlich verwendete Reagenz, aber die geringe Menge (∼1,5 ml pro Probe) an n-Hexan, die benötigt wird, hat vernachlässigbare Auswirkungen auf die Gesamtkosten der Probenanalyse.
Die vorgeschlagene Methode (PM) kann daher für DO-Messungen unter allen Umständen verwendet werden, unter denen die Winkler-Methode derzeit eingesetzt wird. Die vorgeschlagene Methode ist besonders nützlich, wenn die Winkler-Methode aufgrund des begrenzten verfügbaren Probenvolumens nicht angewendet werden kann.