Bilaterale Ganzlungenlavage bei pulmonaler alveolärer Proteinose – Eine retrospektive Studie
Einführung
Pulmonale alveoläre Proteinose (PAP) ist eine seltene diffuse Lungenerkrankung mit drei klinischen Formen, angeboren, erworben (idiopathisch) und sekundär, gekennzeichnet durch eine Anhäufung großer Mengen eines phospholipoproteinhaltigen Materials in den Alveolen aufgrund eines Mangels an Granulozyten-Makrophagen-Kolonie-stimulierender Faktor (GM-CSF) Aktivität1-14 (Abb. 1). Dies geht mit einer abnormen Makrophagenfunktion und einer gestörten Clearance von Surfactant aus der Lunge einher. PAP hat eine Prävalenz von 3,7 Fällen pro Million, eine männliche Prävalenz (Verhältnis 4:1 Männer/Frauen) und 80 % der Fälle werden im dritten und vierten Lebensjahrzehnt gemeldet.6
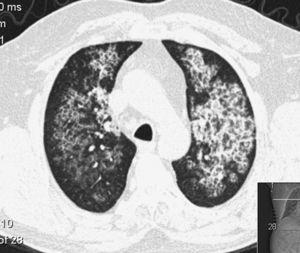
CT-Scan eines Patienten mit pulmonaler alveolärer Proteinose. Man beachte die verdickten interlobaren Septen innerhalb des getrübten Parenchyms, die ein „verrücktes Pflastermuster“ ergeben.
Die in den 1960er Jahren eingeführte Ganzlungenspülung (WLL)3,4,7,10,15 ist immer noch die Standardbehandlung.6 Die unilaterale WLL, bei der die Lavage in jeder Lunge in verschiedenen, nach Tagen/Wochen getrennten Sitzungen durchgeführt wird, ist das häufigste Verfahren. Die bilaterale sequentielle WLL in derselben Behandlungssitzung ist jedoch eine attraktive Alternative, da sie deutlich weniger Zeit in Anspruch nimmt, weniger Beschwerden für den Patienten mit sich bringt und kostengünstiger ist.
Ihre Wirksamkeit wird nicht nur auf die Entfernung von lipoproteinhaltigem Material aus den Alveolarräumen zurückgeführt, sondern auch auf die Entfernung von Anti-GM-CSF-Antikörpern, alveolären Makrophagen und Epithelzellen vom Typ II. Dieses therapeutische Verfahren wird in Betracht gezogen, wenn der Patient eine erhebliche Einschränkung der täglichen Aktivitäten angibt und/oder eine Hypoxämie mit einem pO2
60mmHg, einem P(A-a) O2 ≥40mmHg und einer Shuntfraktion ≥10% festgestellt wird.12
In unserem Krankenhaus haben wir 2010 die erste WWL durchgeführt und sind nach fünf unilateralen WLL zu einem sequentiellen bilateralen WWL-Programm übergegangen.
Ziel dieses Berichts ist es, die bilaterale WLL-Technik zu beschreiben und ihre Sicherheit und Wirksamkeit zu erörtern.
Methoden
In dieser retrospektiven Studie haben wir demografische und klinische Daten aus den medizinischen Berichten von drei erwachsenen Patienten gesammelt. Die angewandte Standardtechnik war eine modifizierte Version des Protokolls des Royal Brompton Hospital (London).6,10
Während des gesamten Verfahrens wurden Elektrokardiographie, Pulsoximetrie (SatO2), invasiver Blutdruck, zentraler Venendruck (CVP), Urinausscheidung, Kapnographie, Tidalvolumina, Bispectral Index (BIS) und zentrale Temperatur kontinuierlich überwacht, und die arteriellen Blutgase (ABGs) wurden stündlich durchgeführt. Es wurde eine totale intravenöse Anästhesie (TIVA) durchgeführt, um die Tiefe der Anästhesie unabhängig von den mit dem Verfahren verbundenen Beatmungsschwankungen zu steuern. Die Narkose wurde während des gesamten Eingriffs aufrechterhalten. Es wurde ein linker Doppellumentubus (DLT) eingeführt, wobei die größtmögliche Größe gewählt wurde, um die Isolierung der Lunge zu gewährleisten und die Beatmung sowie die Wirksamkeit der WLL zu fördern. Seine korrekte Position wurde durch fiberoptische Bronchoskopie bestätigt und der Insufflationsdruck der Manschette gemessen, um ein Auslaufen der Lavageflüssigkeit kontralateral zu verhindern.11
Eine Vor-Oxygenierung mit einem FiO2 von 100 % wurde während 5 Minuten durchgeführt, um eine korrekte alveoläre Denitrogenierung und das Auftreten von Luftblasen zu gewährleisten, die die Entfernung des lipoproteinhaltigen Materials aus den Alveolen beeinträchtigen könnten. Es wurde mit der Ein-Lungen-Beatmung begonnen und die Lungenisolierung überprüft. Die Patienten wurden druckkontrolliert beatmet, wobei der Druck unter 30 cmH2O lag. Das Volumen der zu instillierenden Kochsalzlösung wurde anhand der präoperativen Messungen der funktionellen Residualkapazität (FRC) berechnet. Das Volumen der rechten Lunge wurde mit 3/5 der FRC und das der linken Lunge mit 2/5 der FRC berechnet (im ersten Zyklus wurde ein kleineres Volumen instilliert). Die Kochsalzlösung sollte unter dem Einfluss der Schwerkraft aus einer Höhe von nicht mehr als 40 cm über der mittleren Axillarlinie instilliert werden, um ein Barotrauma und ein Auslaufen in die belüftete Lunge zu verhindern.10 Obwohl in einigen Berichten eine 30°-Lateraldekubitus-Lagerung beschrieben wird, um das Verhältnis von Ventilation/Perfusion der abhängigen, beatmeten Lunge zu erhalten, erhöht dies die Wahrscheinlichkeit einer kontralateralen Lungenüberflutung, so dass wir eine Dorsaldekubitus-Lagerung mit einer umgekehrten Trendelenburg-Lagerung sowie eine Trendelenburg-Lagerung bevorzugten, um die gravitative Instillation und Entfernung der warmen Kochsalzlösung aus der Lunge zu erleichtern.6,11 Diese Position wurde gewählt, wenn eine bilaterale WLL durchgeführt wurde (Abb. 2).
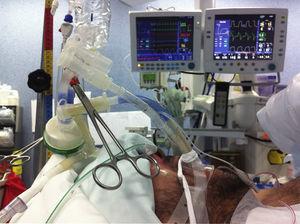
Technische Darstellung einer WLL.
Wenn der zunächst milchige Ausfluss weniger dicht wurde, wurde die Drainage bei der Hälfte des Volumens unterbrochen, und mehrere Zyklen manueller Beatmung mit einem CPAP-Ventil mit 5-10 mmHg Druckbegrenzung (die „Bingisser-Modifikation“) ermöglichten eine manuelle Perkussion der Alveolen. Dieses Manöver steigert die Lipoprotein-Clearance erheblich.12,14 Der Lavage-Zyklus wurde so lange wiederholt, bis der Lavage-Abfluss klar wurde (Abb. 3). Da während des Eingriffs ein hohes Flüssigkeitsvolumen gespült wird, besteht ein hohes Risiko der Hypothermie. Die Aufrechterhaltung der Körpertemperatur ist von entscheidender Bedeutung und sollte mit einer auf 37°C erwärmten Lavageflüssigkeit und einer Wärmedecke erfolgen.

Entwicklung der milchigen Flüssigkeit während des Verfahrens.
Nachdem die erste Lunge erfolgreich gewaschen worden war, wurde sie vorsichtig abgesaugt und ihre Reexpansion durchgeführt, zunächst durch bilaterale Beatmung, dann durch unilaterale Beatmung. Nach 1 Stunde Beatmung wurden die Lungencompliance und die Daten der Blutgasanalyse überprüft. Wenn die gewaschene Lunge den Gasaustauschbedarf des Patienten sicherstellen konnte, wurde die kontralaterale WLL eingeleitet, wobei die oben beschriebenen Verfahren wiederholt wurden.8
Am Ende des Verfahrens wurde die restliche Kochsalzlösung über die faseroptische Bronchoskopie abgesaugt und die bilaterale Beatmung wieder aufgenommen. Der doppellumige Tubus wurde dann durch einen Endotrachealtubus ersetzt und der Patient zur Überwachung über Nacht auf eine Aufwachstation verlegt.
Ergebnisse
Bilaterale WWL wurde bei drei erwachsenen Patienten durchgeführt, 2 Männern und 1 Frau, Durchschnittsalter 43,6 (Bereich 39 – 47 Jahre) (Tabelle 1), alle mit einer Hypoxie in Ruhe unter 60mmHg.
Salzlösungsmenge, die in die bilaterale WWL instilliert und dort zurückgehalten wurde.
| Lavagen | Volumen (L) rechte Lunge | Volumen (L) linke Lunge | ||
| Instilliertes Volumen (L) | Positiver Saldo (mL) | Instilliertes Volumen (L) | Positiver Saldo (mL) | |
| 1. | 9.2 | 470 | 11.8 | 510 |
| 2. | 15.3 | 530 | 10.7 | 450 |
| 3. | 14.0 | 600 | 10.8 | 550 |
| 4. | 13.5 | 500 | 10.6 | 350 |
| 5. | 15.5 | 930 | 11.1 | 480 |
| 6. | 15.5 | 820 | 15.3 | 900 |
Der erste Patient war männlich, 39 Jahre alt, Raucher, Bäcker, bei dem einen Monat vor der ersten WLL aufgrund klinischer, radiologischer und BAL-Merkmale sowie des Vorhandenseins von GM-CSF-Antikörpern im Serum PAP diagnostiziert wurde. Bei der Vorstellung der Krankheit hatte er eine respiratorische Insuffizienz in Verbindung mit einer ausgedehnten bilateralen Lungenbeteiligung, die im HRCT-Scan zu sehen war, und es wurde eine bilaterale WLL durchgeführt, bei der 9,2 und 11,8 l Kochsalzlösung in die rechte bzw. linke Lunge instilliert wurden. Nach einer kurzen Zeit der klinischen, funktionellen und radiologischen Besserung verschlechterte sich der Zustand des Patienten mit der Ausbreitung der radiologischen Lungentrübungen und der Ateminsuffizienz. Diese klinische Verschlechterung fiel mit der Rückkehr des Patienten an seinen Arbeitsplatz zusammen. Bäckereimehl war als möglicher Auslöser beschrieben worden.16 Drei Monate später wurde eine zweite beidseitige WLL durchgeführt, bei der 15,3 und 10,7 l Kochsalzlösung instilliert wurden. Nach diesem Eingriff und der Beendigung seines früheren Arbeitsumfelds blieb der Patient klinisch stabil.
Der zweite Patient, bei dem eine WLL durchgeführt wurde, war weiblich, 47 Jahre alt, Landwirtin, Nichtraucherin, ohne Komorbiditäten, mit der Diagnose PAP einen Monat vor der ersten WLL aufgrund klinischer, radiologischer und BAL-Merkmale und dem Vorhandensein von GM-CSF-Antikörpern im Serum. Das klinische Bild war dem des ersten Patienten sehr ähnlich, mit Dyspnoe bei Anstrengung und trockenem Husten in Verbindung mit respiratorischer Insuffizienz und breiten bilateralen Crazy-Paving-Muster-Opazitäten im HRCT-Scan. Nach der Diagnose wurde eine WLL mit Instillation von 14 bzw. 10,8 l Kochsalzlösung in die rechte bzw. linke Lunge durchgeführt. Nach einer kurzen anfänglichen klinischen Besserung wurde sie 1,5 Monate später einer weiteren WLL unterzogen, da sie zunehmend symptomatisch wurde und einen paO2
60mmHg aufwies. Bei diesem Verfahren wurden insgesamt 13,5 und 10,6 l in die rechte bzw. linke Lunge instilliert. Vier Monate später wurde aufgrund einer klinischen Verschlechterung eine dritte WLL durchgeführt, und diesmal wurden 15,5 l in die rechte und 11,1 l in die linke Lunge instilliert (Abb. 4). Nach diesem Eingriff erreichte der Patient klinische, funktionelle und radiologische Stabilität.

Sequentielle Proben von bilateralen WLLs.
Der dritte eingeschlossene Patient war männlich, 45 Jahre alt, Ex-Raucher, Reifenfabrikarbeiter, mit der Diagnose PAP während einer Untersuchung und Behandlung eines nocardia-induzierten zerebralen Abszesses. Wie bei den beiden anderen Patienten wurde die Diagnose anhand der typischen radiologischen und BAL-Merkmale in Verbindung mit GM-CSF-Antikörpern im Serum gestellt. Allerdings hatte er zwei Jahre zuvor eine Thorax-HRCT-Aufnahme mit beidseitigem Crazy-Paving-Muster erhalten. Ein Jahr nach der Diagnose traten bei ihm vermehrt Symptome wie Dyspnoe bei Anstrengung und respiratorische Insuffizienz (paO2-57mmHg) auf, weshalb er sich einer WLL unterzog, bei der 15,5 bzw. 15,3 ml Kochsalzlösung in die rechte bzw. linke Lunge instilliert wurden. Nach diesem Eingriff kam es zu einer deutlichen klinischen, funktionellen und radiologischen Verbesserung.
Alle sechs WLL-Verfahren wurden nach dem festgelegten Protokoll und ohne größere Komplikationen durchgeführt.
Die stündliche gasometrische Überwachung konzentrierte sich auf die Sicherstellung einer korrekten Oxygenierung und Ventilation. Die gasometrischen Werte der Patienten konnten während des gesamten Eingriffs problemlos aufrechterhalten werden, wobei der pCO2-Wert unter 55 mmHg und der SpO2-Wert dauerhaft über den Werten der Patienten lag, obwohl diese sich in Rückenlage befanden (Tabelle 2) (Abb. 5). In der Tat beobachteten wir bei allen bilateralen WWL-Patienten während des Verfahrens eine fortschreitende Entwicklung der metabolischen Azidose. Diese metabolische Azidose wurde in den ersten Stunden postoperativ rückgängig gemacht, und danach wurden keine Komorbiditäten mehr festgestellt.
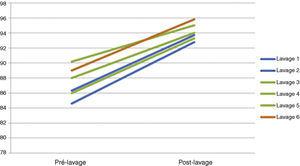
Entwicklung der SatO2-Messung während der Ganzlungen-Lavagen.
Beim Bingisser-Manöver beobachteten wir eine vorübergehende Schwierigkeit bei der Rückgewinnung des Lavagevolumens (was zu einer positiven Flüssigkeitsbilanz beitrug), aber eine deutliche Zunahme der Lavagedichte.
In jedem Fall beobachteten wir eine Episode kontralateraler Lavageparavasation. Bei allen Eingriffen wurde die Körpertemperatur zwischen 36 und 37°C gehalten. Die mittlere Eingriffszeit betrug 8 Stunden (Bereich 7h32-9h41).
Die Zeit bis zur Extubation variierte je nach der Entwicklung der klinischen und Blutgasanalyse, und alle Patienten wurden nach 18 Stunden erfolgreich extubiert.
Nach diesen Eingriffen waren die Funktionsfähigkeit und die täglichen Aktivitäten aller Patienten deutlich verbessert, was durch klinische Anzeichen/Symptome sowie die Atemfunktionstests und die gasometrischen Daten dokumentiert wurde.
Diskussion
In dieser kurzen Mitteilung haben wir sechs bilaterale sequenzielle WLL-Eingriffe beschrieben, die bei drei Patienten mit PAP durchgeführt wurden, und ihre klinische Wirksamkeit und Sicherheit bestätigt.
Trotz ihrer erheblichen Invasivität bleibt die WLL die empfohlene Behandlung bei PAP und ist bisher die einzige Therapie mit nachgewiesener Wirksamkeit. Wenn ein PAP-Patient mit Ateminsuffizienz und ausgedehnten bildgebenden Trübungen im HRCT-Scan vorstellig wird, ist dieses Verfahren sogar obligatorisch. Die WLL ist ein teures und zeitaufwändiges Verfahren, das die Expertise eines multidisziplinären Ansatzes erfordert, was zusammen mit der Seltenheit von PAP erklärt, warum dieses Verfahren nur in wenigen Zentren durchgeführt wird. Die Entscheidung für eine bilaterale WLL bedeutet einen besseren Patientenkomfort, eine Verringerung der Kosten und des Zeitaufwands sowie die Aufrechterhaltung der klinischen Wirksamkeit.
Die drei eingeschlossenen Patienten können als typische PAP-Fälle angesehen werden, obwohl es einige Unterschiede gab. Bei zwei von ihnen trat die Krankheit akut auf, so dass eine WLL nach der Diagnose erforderlich war, während der andere Patient im Verlauf der Krankheit diesem Verfahren unterzogen wurde. Während dieser dritte Patient nur einer WLL unterzogen werden musste, waren bei den beiden anderen mehrere WLL erforderlich, genauer gesagt zwei und drei Verfahren.
Der entscheidende Faktor für die Durchführung der zweiten Lungenspülung ist, ob die Kapazität der ersten Lungenspülung ausreicht, um die Bedürfnisse des Patienten zu erfüllen. Aus diesem Grund wählen wir, wenn keine laterale Dominanz vorliegt, die größere Lunge, die rechte Lunge, für die erste Spülung aus. Um ein Barotrauma zu vermeiden, wurde der maximale Inspirationsdruck auf 30 cmH2O begrenzt. Bei allen Verfahren waren nach einer Stunde Beatmung die pulmonale Compliance und die gasometrischen Werte bei der Ein-Lungen-Belüftung der gewaschenen Lunge mit dem Beginn der Lavage der zweiten Lunge kompatibel.
Die Wahl der druckgesteuerten Beatmung ermöglichte es uns, die Veränderungen der Lungencompliance während der Lavage kontinuierlich zu überwachen, und verhinderte eine mögliche Schlauchdislokation oder andere Störungen. Außerdem konnte so die Erholung der gewaschenen Lungencompliance beobachtet werden.
Die Rückenlage des Patienten behinderte die Oxygenierung nicht, so dass wir bei der Beatmung der abhängigen Lunge nicht auf die seitliche Dekubitusposition zurückgreifen mussten, eine Position, die weniger stabil ist und bei einem langwierigen Verfahren (durchschnittlich 8 Stunden) größere Risiken birgt.
Wir haben uns für das Perkussionsmanöver nach Bingisser entschieden, weil der Druck, der auf die Atemwege ausgeübt wird, gemessen wird, im Gegensatz zu den kinesiotherapeutischen Manövern, bei denen diese Quantifizierung nicht möglich ist, wodurch das Risiko eines übermäßigen Perkussionsdrucks verringert und eine mögliche kontralaterale Überschwemmung vermieden wird.8
In einem Versuch, die während der Eingriffe beobachtete metabolische Azidose umzukehren, wurde das in der perioperativen Periode verwendete Erhaltungsserum – Natriumchlorid 0,9 % – beim dritten bilateralen Eingriff und danach durch Ringerlactat ersetzt, was nur zu bescheidenen Verbesserungen führte. In der Literatur findet sich kein Hinweis auf die Verwendung dieses Lösungsmittels als Lavageflüssigkeit für die Lunge, so dass Natriumchlorid weiterhin verwendet wird.
Zusammenfassend lässt sich sagen, dass die klinische Wirksamkeit der bilateralen WLL, ihre Vorteile in Bezug auf Zeit- und Kostenersparnis und die Verringerung der Unannehmlichkeiten für den Patienten diese Technik zu einer geeigneten ersten Wahl für die therapeutische Lavage bei PAP-Patienten machen.
Ethische AngabenSchutz der menschlichen und tierischen Versuchspersonen
Die Autoren erklären, dass die angewandten Verfahren mit den Vorschriften der zuständigen Ethikkommission für klinische Forschung und mit dem Ethikkodex des Weltärztebundes (Deklaration von Helsinki) übereinstimmen.
Vertraulichkeit der Daten
Die Autoren erklären, dass sie die Protokolle ihrer Arbeitsstelle über die Veröffentlichung von Patientendaten befolgt haben.
Recht auf Privatsphäre und informierte Zustimmung
Die Autoren erklären, dass in diesem Artikel keine Patientendaten erscheinen.
Interessenkonflikte
Die Autoren haben keine Interessenkonflikte zu erklären.