Modification of Winkler’s method for determination of dissolved oxygen concentration in small sample volumes
Poprvé publikováno 27. srpna 2010
Winklerova metoda je nejoblíbenějším postupem pro stanovení koncentrace rozpuštěného kyslíku (DO) ve vzorcích vody. Tato metoda však vyžaduje poměrně velký objem vzorku 200 ml pro přesné stanovení DO. Bylo navrženo mnoho alternativních metod pro měření koncentrace DO v malých objemech vzorků, ale většina těchto metod má problémy buď s nízkou přesností, vysokou cenou, komplikovaným přístrojovým vybavením nebo dlouhou dobou analýzy. V tomto článku je navržena jednoduchá modifikace Winklerovy metody pro měření koncentrací DO ve vzorcích o objemu 1 ml. Navrhovaná metoda je přesná, levná, jednoduchá a rychlá. Koncentrace DO byly měřeny ve 33 vzorcích jak konvenční Winklerovou metodou (WM), tak navrhovanou metodou (PM). U 23 z 33 analyzovaných vzorků nebylo možné na 95 % hladině spolehlivosti zamítnout hypotézu, že populační průměry měření jsou stejné (μ1 = μ2), a u 19 vzorků nebylo možné na 95 % hladině spolehlivosti zamítnout hypotézu, že populační rozptyly měření jsou stejné (σ21 = σ22). Byl tedy učiněn závěr, že ve většině případů poskytují měření DO metodami WM a PM srovnatelné výsledky jak z hlediska přesnosti, tak i preciznosti.
Úvod
Winklerova metoda (metoda č. 4500-O-C)1 byla všeobecně přijata jako přesná a spolehlivá metoda2 pro měření koncentrace rozpuštěného kyslíku (DO) v různých vzorcích vody. Tato metoda je považována za etalon pro stanovení DO. Hlavní nevýhodou této metody je však požadavek na velký objem vzorku 200 ml.3
Pro měření DO byla vyvinuta také řada alternativních metod. Tyto metody spadají do tří různých kategorií: (1) kolorimetrické metody, (2) metody využívající plynovou chromatografii a (3) metody využívající elektrochemické a optické senzory. Kolorimetrické metody lze použít pro stanovení DO v malých objemech vzorků. Trpí však nevýhodami, jako je požadavek na drahá (např. zlatý sol) nebo toxická (např. kyanid) chemická činidla.4 Dalším limitujícím faktorem těchto metod je nedostatečné zdůvodnění výběru vlnové délky měření.5 Stanovení DO je možné také pomocí plynové chromatografie. Metody plynové chromatografie jsou sice přesné a vyžadují malé objemy vzorků, nicméně jsou časově náročné a drahé. Elektrochemické senzory jsou pro měření DO široce používány a jejich výhody a nevýhody byly přezkoumány jinde.6 Elektrochemické senzory obecně trpí nevratnými tlakovými efekty, kontaminací sirovodíkem a křížovou citlivostí.7 Během měření také spotřebovávají DO, a proto mohou být nevhodné pro velmi malé objemy vzorků. V poslední době se pozornost zaměřuje na vývoj optických senzorů založených na principu dynamického zhášení luminiscence kyslíku.8 Tyto optické senzory se snadno používají, mají rychlou odezvu a jsou odolné. Všechny senzory, ať už elektrochemické nebo optické, však vyžadují kalibraci podle Winklerovy metody kvůli citlivosti senzorů na teplotu a tlak.9,10 Jsou také citlivé na biologické znečištění a růst bakterií na povrchu senzoru.8
Vzhledem k přirozeným omezením alternativních metod popsaným výše a jejich závislosti na Winklerově metodě pro křížovou kontrolu a kalibraci bylo navrženo také několik modifikací samotné Winklerovy metody pro měření koncentrací DO v objemech vzorků 1-10 ml.11,12,13 Tyto „mikro-Winklerovy“ metody však nejsou příliš populární kvůli složitým přístrojovým požadavkům a propracovaným bezpečnostním opatřením nutným k zamezení kontaminace vzorků výměnou s atmosférickým kyslíkem. Tyto metody byly kriticky přezkoumány jinde.14 Nedávno byla navržena gravimetrická titrační metoda Micro-Winkler15 pro měření DO v malých vzorcích. Tento postup však vyžaduje několikanásobné a přesné gravimetrické měření pomocí citlivých vah, a proto se zdá být poměrně složitý.
Na základě přehledu literatury se zdá, že téměř všechny metody vyvinuté pro měření DO v malých vzorcích mají nějaké nedostatky. Proto je stále zapotřebí vyvinout lepší, tj. přesnou, precizní, levnou, jednoduchou a rychlou metodu pro měření DO v malých objemech vzorků.
Představení navrhované metody
Hlavním problémem při měření koncentrací DO v malých vzorcích je zabránit kontaminaci vzorků interakcí s atmosférou. Navrhuje se, aby mezi vzorek vody a atmosféru byla zavedena izolační vrstva kapaliny. Požadované vlastnosti izolační kapaliny jsou: nemísitelnost s vodou, hustota menší než voda a zanedbatelná schopnost rozpouštět kyslík. Navrhuje se, aby se izolační kapalina odebrala do lahvičky a vzorek vody, jehož DO se má stanovit (objem 1 ml), se zavedl přímo pod vrstvu izolační kapaliny. Tímto krokem se vzorek vody účinně uzavře před atmosférou. DO ve vzorku vody lze poté stanovit a převést na ekvivalentní množství jódu pomocí stejných činidel, jaká se používají ve Winklerově metodě. Roztok jódu se poté extrahuje z lahvičky pomocí injekční stříkačky a titruje se pomocí Na2S2O3 pro stanovení koncentrace DO ve vzorku.
Po několika kolech zkoušek byl jako izolační kapalina zvolen n-hexan, jak je popsáno výše. n-hexan je lehčí než voda (specifická hmotnost = 0,7) a je prakticky nemísitelný s vodou. Rozpustnost kyslíku v n-hexanu je 0,002 molárního zlomku,16tj. kyslík je v n-hexanu prakticky nerozpustný.
Materiál a metody
Všechna použitá činidla byla analytické reagenční třídy (>99% čistoty, Loba Chemicals, Indie). Pro přípravu činidel a ředění vzorků byla použita deionizovaná voda (Milli-Q, Millipore, USA). Použitý n-hexan byl kvality HPLC (>99% čistoty, Merck, Indie). V této studii bylo použito borosilikátové sklo. Roztoky MnSO4 a alkalických jodidů byly připraveny podle standardních metod (metoda č. 4500-O C).1
Postup měření DO podle navržené metody (PM) byl následující. Nejprve bylo 0,5 ml n-hexanu přeneseno do 16ml skleněné lahvičky (Wheaton Science, USA). Poté byl do 2ml pipety odebrán 1 ml n-hexanu a pipeta byla dále naplněna 1 ml vzorku vody, jehož koncentrace DO měla být stanovena. Výše uvedený postup odběru vzorku zajistil, že vzorek byl odebrán bez hlavového prostoru. Tento krok odběru vzorku je nejdůležitější, protože výskyt jakýchkoli bublin nebo vzduchové mezery na rozhraní hexanu a vody nebo jinde v pipetě může vést k chybám. Ústí pipety se pak umístilo pod vrstvu hexanu v lahvičce, a vzorek se tak dostal pod vrstvu hexanu, čímž se zabránilo jakémukoli kontaktu vzorku s atmosférou. Odběr vzorku do pipety a nanesení vzorku pod vrstvu hexanu v lahvičce musí být provedeno co nejrychleji, aby se minimalizovaly chyby. Poté bylo do vzorku vody pod hexanovou vrstvou vneseno 5 μl MnSO4 pomocí 10 μl mikroinjekční stříkačky (Hamilton, USA) a následně bylo obdobným způsobem přidáno 5 μl roztoku alkalicko-azido-jodidového roztoku. Tvorba sraženiny začala ihned po přídavcích a byla dokončena do 3 min. Poté bylo k sraženině vytvořené pod vrstvou hexanu přidáno pomocí mikropipety 0,1 ml konc. H2SO4. Sraženina byla rozpuštěna během 3 min a pod hexanovou vrstvou se vytvořil žlutý roztok jódu. Přesně 1 ml roztoku jódu byl extrahován zpod hexanové vrstvy pomocí mikrostříkačky a převeden do 25 ml kádinky. 1 ml roztoku jódu v kádince byl zředěn na ∼10 ml přidáním deionizované vody pro snadnější titraci. Přídavek deionizované vody pouze zředí roztok jódu, aniž by ovlivnil množství jódu v kádince. Obsah kádinky byl titrován 0,00625 M roztokem Na2S2O3. 1 ml tohoto titrantu odpovídá 55,5 mg L-1 DO v původním vzorku. Titrant se nabral do 250 μl mikroinjekční stříkačky (Hamilton, USA) a za stálého míchání se po kapkách přidával do kádinky, dokud se žluté zbarvení jódu téměř nevytratilo. Poté byly přidány 1-2 kapky roztoku škrobu a titrace pokračovala, dokud se modré zbarvení způsobené škrobem nevytratilo. Na základě objemu titrantu potřebného při konkrétní titraci byla vypočtena koncentrace DO v původním vzorku.
Koncentrace DO byla rovněž stanovena v různých vzorcích pomocí Winklerovy metody (WM). Požadavky na činidla a další podrobnosti obou metod jsou uvedeny v tabulce 1.
| Vzorky č. 1 a č. 2. | Reagent | Kvantita | Síla | ||
|---|---|---|---|---|---|
| WM | PM | WM | PM | ||
| Vzorek | 200 ml | 1 ml | – | – | |
| MnSO4 | 1 ml | 5 μL | Podle WM | ||
| Alkali-azido-jodidové činidlo | 1 ml | 5 μl | Jako na WM | ||
| Na2S2O3 | Podle potřeby | Podle potřeby | 0.025M | 0,00625M | |
| H2SO4 | 1 ml | 0.1 ml | Podle WM | ||
| Škrob | 1-2 kapky | 1-2 kapky | Podle WM | ||
| n-?Hexan | Nepoužívá se | 1.5 ml | – | – | |
Výsledky a diskuse
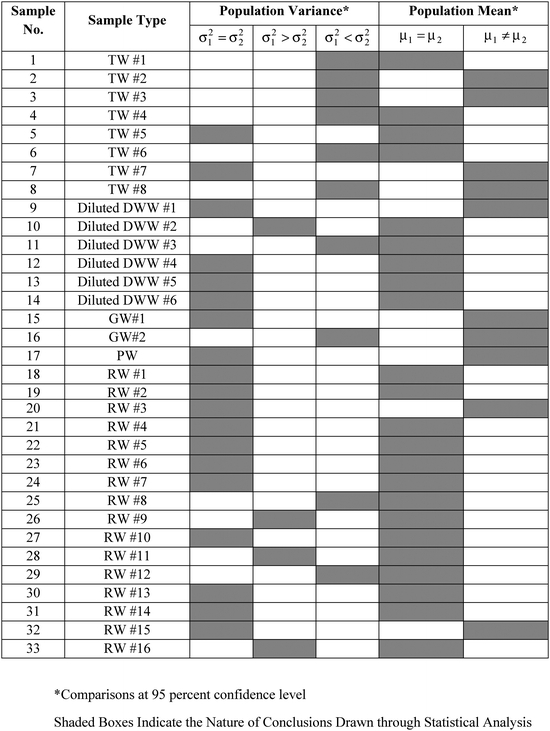
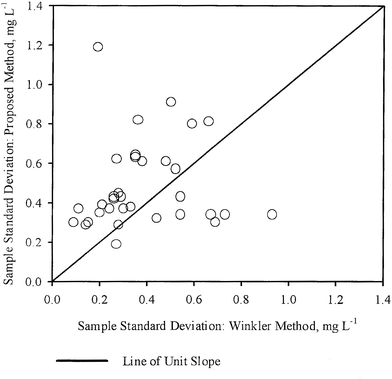
Koncentrace DO byla měřena ve 33 vzorcích vody (viz tabulka 2) získaných z různých míst v okolí města Kanpur v Indii. Z 33 vzorků bylo 8 vzorků vody z vodovodu, 16 vzorků říční vody, 6 vzorků domácích odpadních vod ředěných vodou z vodovodu, 2 vzorky podzemní vody a 1 vzorek vody z rybníka. Vzorky byly vybrány tak, aby bylo možné měřit koncentrace DO v různých matricích vzorků. U každého vzorku bylo provedeno několik opakovaných měření DO, a to jak WM, tak PM. Vypočtené střední hodnoty vzorků (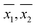 ), směrodatné odchylky vzorků (S1, S2) a počet opakovaných měření (n1, n2) pro WM a PM jsou uvedeny v tabulce 2 pro každý vzorek.
), směrodatné odchylky vzorků (S1, S2) a počet opakovaných měření (n1, n2) pro WM a PM jsou uvedeny v tabulce 2 pro každý vzorek.
Normální grafy souborů opakovaných měření oběma metodami byly všechny přibližně lineární, což naznačuje, že opakovaná měření jsou normálně rozdělena, a tudíž je lze na tomto základě dále statisticky analyzovat. Pro ilustraci jsou na obr. 1A uvedeny normální grafy pro pět měření vzorků provedených metodou WM. Normální grafy pro stejných pět měření vzorků provedených PM jsou uvedeny na obr. 1B.
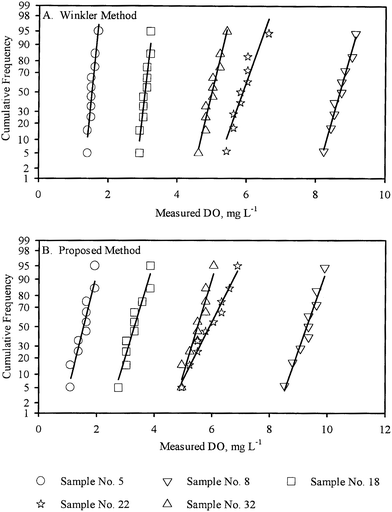
Rozptyly (S21,S22) v opakovaných měřeních vzorku pomocí WM, resp. pomocí PM byly použity pro párové porovnání odpovídajících populačních rozptylů (σ21,σ22) pomocí F-testu. Z 33 vzorků, u nichž byla DO měřena oběma metodami (WM a PM), nebylo možné hypotézu, že populační rozptyly jsou stejné (σ21 = σ22), zamítnout na 95 % hladině spolehlivosti u 19 vzorků. Dále nebylo možné zamítnout hypotézu σ21 > σ22 u 4 vzorků, zatímco hypotézu σ21 < σ22 nebylo možné zamítnout u zbývajících 10 vzorků, všechny na 95 % hladině spolehlivosti. Tyto výsledky byly shrnuty v tabulce 3.
Dále byly pro párové porovnání odpovídajících populačních průměrů (μ1, μ2) použity výběrové rozptyly (S21,S22) a výběrové průměry (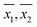 ) pro každý vzorek, jak byly získány pomocí WM, respektive PM. U vzorků se stejnými rozptyly (viz tabulka 3) bylo párové srovnání provedeno pomocí Studentova t-testu. U vzorků s nerovnoměrnými rozptyly (viz tabulka 3) bylo párové srovnání provedeno pomocí t-testu nerovnoměrných rozptylů.17 U 23 z 33 vzorků, u nichž bylo měření DO provedeno jak pomocí WM, tak pomocí PM, nebylo možné na 95 % hladině spolehlivosti zamítnout hypotézu, že populační průměry jsou stejné (μ1 = μ2).
) pro každý vzorek, jak byly získány pomocí WM, respektive PM. U vzorků se stejnými rozptyly (viz tabulka 3) bylo párové srovnání provedeno pomocí Studentova t-testu. U vzorků s nerovnoměrnými rozptyly (viz tabulka 3) bylo párové srovnání provedeno pomocí t-testu nerovnoměrných rozptylů.17 U 23 z 33 vzorků, u nichž bylo měření DO provedeno jak pomocí WM, tak pomocí PM, nebylo možné na 95 % hladině spolehlivosti zamítnout hypotézu, že populační průměry jsou stejné (μ1 = μ2).
Vzorové průměry (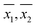 ) pro každý vzorek, jak byly získány pomocí WM, respektive PM, byly vzájemně vyneseny do grafu na obr. 2. Chybové úsečky uvedené na obrázku odpovídají příslušným 95procentním intervalům spolehlivosti. Na stejném obrázku byla také nakreslena přímka s jednotkovým sklonem procházející počátkem. Bylo zjištěno, že všechny body leží velmi blízko přímky jednotkového sklonu, což je v souladu s obecnými závěry uvedenými v tabulce 3, tj. u většiny vzorků se průměrné koncentrace DO získané oběma metodami statisticky neliší. Ve většině případů bylo tedy měření DO pomocí PM stejně přesné jako měření DO pomocí WM.
) pro každý vzorek, jak byly získány pomocí WM, respektive PM, byly vzájemně vyneseny do grafu na obr. 2. Chybové úsečky uvedené na obrázku odpovídají příslušným 95procentním intervalům spolehlivosti. Na stejném obrázku byla také nakreslena přímka s jednotkovým sklonem procházející počátkem. Bylo zjištěno, že všechny body leží velmi blízko přímky jednotkového sklonu, což je v souladu s obecnými závěry uvedenými v tabulce 3, tj. u většiny vzorků se průměrné koncentrace DO získané oběma metodami statisticky neliší. Ve většině případů bylo tedy měření DO pomocí PM stejně přesné jako měření DO pomocí WM.
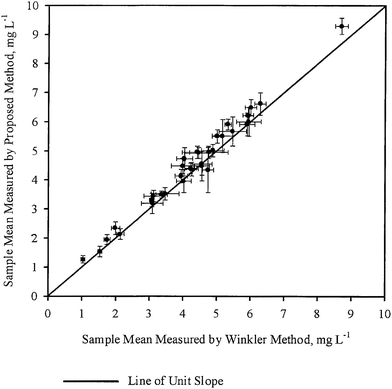
Na obr. 3 byly proti sobě vyneseny směrodatné odchylky vzorků (S1,S2) pro jednotlivé vzorky získané pomocí WM, resp. pomocí PM. Na stejném obrázku byla také nakreslena přímka s jednotkovým sklonem procházející počátkem. V tomto případě se zdá, že body jsou vzhledem k přímce jednotkového sklonu rozptýleny poměrně rovnoměrně, přičemž některé body jsou blízko přímky, zatímco jiné jsou od ní vzdálenější. Tato pozorování jsou také v obecném souladu se závěry vyvozenými z tabulky 3, tj. u většiny vzorků se odchylky v koncentraci DO naměřené oběma metodami statisticky neliší. Ve většině případů bylo tedy měření DO metodou PM stejně přesné jako měření DO metodou WM.
Dospělo se k závěru, že při pečlivé manipulaci se vzorky a titraci může navrhovaná metoda (PM) poskytovat výsledky srovnatelné s Winklerovou metodou (WM), a to jak z hlediska přesnosti, tak i správnosti. Nicméně přesnost stanovení DO metodou PM lze pravděpodobně zvýšit použitím mikrostříkačky s nižším nejmenším počtem pro závěrečnou titraci. Mikrostříkačka použitá v této studii měla nejmenší počet 5 μl, což odpovídá nejistotě ∼0,25 mg L-1 DO v podmínkách této studie. Tuto nejistotu lze snížit použitím mikrostříkačky s nižším nejmenším počtem.
Závěry
Cílem této studie bylo vyvinout přesnou, levnou, jednoduchou a rychlou metodu měření DO v malých objemech vzorků. Na základě předložených výsledků a analýzy lze konstatovat, že navržená metoda řeší většinu výše uvedených problémů. Hlavní závěry studie byly následující:
➢ Zavedení izolační vrstvy n-hexanu pro zabránění přenosu kyslíku mezi vodným vzorkem a atmosférou vede ke konzistentnímu a přesnému stanovení DO v malých objemech vzorku. To je hlavní inovace obsažená v navrhované metodě.
➢ Bylo také prokázáno, že při přijetí vhodných opatření může navrhovaná metoda (PM) obecně poskytovat výsledky, které jsou statisticky srovnatelné s výsledky získanými Winklerovou metodou (WM), a to jak s ohledem na průměrnou koncentraci DO, tak i s ohledem na rozptyl koncentrace DO kolem průměru.
➢ Požadavky na činidla a skleněné nádobí jsou u navrhované metody menší než u Winklerovy metody, a to především díky menšímu objemu použitého vzorku. n-hexan je jediným dodatečně použitým činidlem, ale malé množství (∼1,5 ml na vzorek) potřebného n-hexanu má zanedbatelný dopad na celkové náklady na analýzu vzorku.
Pro měření DO lze tedy navrhovanou metodu (PM) použít za všech okolností, kdy se v současnosti používá Winklerova metoda. Navrhovaná metoda je zvláště užitečná za okolností, kdy Winklerovu metodu nelze použít z důvodu omezení dostupného objemu vzorku.
.