9.4: De ce nu putem vedea moleculele?
Cel mai simplu mod de a determina structurile moleculelor ar fi să „vedem” cum sunt aranjate nucleele și cum sunt distribuiți electronii. Acest lucru nu este posibil cu lumina vizibilă, deoarece lungimile de undă ale luminii vizibile sunt foarte mult mai mari decât dimensiunile moleculare obișnuite. Un fascicul de electroni poate avea lungimile de undă scurte necesare, dar moleculele organice mici sunt distruse rapid prin iradierea cu electroni cu lungimi de undă corespunzătoare. Cu toate acestea, microscopia electronică este o tehnică valoroasă pentru studiul moleculelor mari, cum ar fi ADN-ul, care pot fi colorate cu atomi de metale grele înainte de vizualizare, sau care sunt ele însele rezonabil de stabile la un fascicul de electroni (figurile 9-4 și 9-5).

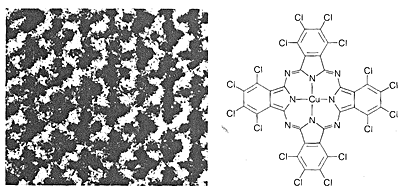
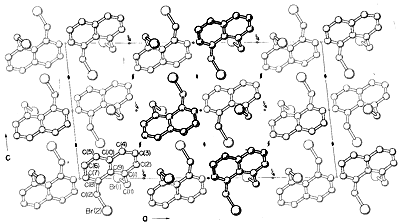
Practic toate părțile spectrului de radiații electromagnetice, de la razele X până la undele radio, au o aplicație practică pentru studiul moleculelor organice. Utilizarea difracției de raze X pentru determinarea structurilor moleculelor din cristale este deosebit de valoroasă, iar în ultimii zece ani această tehnică a devenit aproape o rutină. Figura 9-6 prezintă aranjamentul detaliat al carbonilor, al hidrogenilor și al bromurilor din 1,8-bis(bromometil)naftalină, \(1\), așa cum a fost determinat prin difracție de raze X. Aparatura și tehnicile utilizate sunt extrem de complexe și nu sunt încă disponibile pentru foarte multe laboratoare organice.\(^3\)
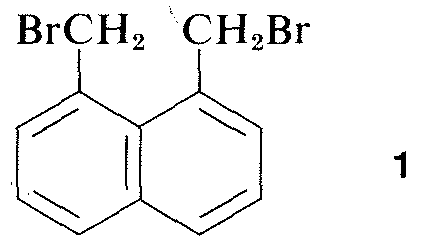
Alte metode de difracție includ difracția electronică, care poate fi utilizată pentru a „determina structurile gazelor sau ale substanțelor lichide volatile care nu pot fi obținute sub formă de cristale adecvate pentru difracția de raze X, și difracția neutronică, care are o aplicație specială pentru cristalele în care se dorește localizarea exactă a hidrogenilor. Hidrogenul nu are suficientă putere de împrăștiere a razelor X pentru a fi localizat cu precizie prin difracție de raze X.
Metodele de difracție pot fi folosite pentru a determina structurile complete ale moleculelor organice, dar nu sunt suficient de obișnuite pentru a fi utilizate în general în lucrările practice de laborator de organică. Din acest motiv, în restul acestui capitol vom pune accentul pe acele forme de spectroscopie care sunt în general disponibile pentru utilizarea de rutină în laborator. După cum se va vedea, aceste metode sunt utilizate de către chimiștii organici în moduri mai mult sau mai puțin empirice. În general, metodele spectroscopice depind de o anumită formă de excitare a moleculelor prin absorbția de radiații electromagnetice și, după cum am spus, practic toate părțile spectrului electromagnetic au utilitate în acest sens. Întinderea frecvent utilizată a spectrului electromagnetic este prezentată în figura 9-7, împreună cu o comparație a diferitelor unități care sunt folosite pentru a exprima energia sau lungimea de undă.
Principalele tipuri de spectroscopie utilizate pentru analiza structurală a compușilor organici sunt enumerate în tabelul 9-1. Este prezentată gama de frecvențe ale radiației absorbite, precum și efectul produs de radiație și tipul specific de informații care sunt utilizate în analiza structurală. După o scurtă prezentare a principiilor spectroscopiei, vom descrie metodele care sunt de cea mai mare utilitate pentru lucrările practice de laborator. Cu toate acestea, este foarte important să cunoaștem și alte metode, mai puțin obișnuite, care pot fi folosite pentru rezolvarea unor probleme speciale, iar unele dintre acestea sunt discutate în acest capitol și în capitolele 19 și 27.
S-ar putea să aveți probleme cu relațiile dintre varietatea de unități de lungime de undă și frecvență folosite în mod obișnuit în spectroscopie. Relația dintre lungimea de undă, frecvență și viteză ar trebui să vă devină clară dacă vă considerați stând pe un dig și privind valurile oceanului care trec. Presupunând că valurile sunt uniform distanțate, va exista o distanță uniformă între creste, care este \(\lambda\), lungimea de undă. Crestele valurilor vor trece cu un anumit număr pe minut, care este \(\nu\), frecvența. Viteza, \(c\), cu care trec crestele pe lângă tine este legată de \(\lambda\) și \(\nu\) prin relația \(c = \lambda \nu\).
Acest lucru nu este cu adevărat foarte complicat și se aplică la fel de bine la undele apei sau la radiația electromagnetică. Ceea ce este aproape inutil de complicat este varietatea de unități utilizate în mod obișnuit pentru a exprima \(\lambda\) și \(\nu\) pentru radiația electromagnetică. O problemă este reprezentată de tradiție, iar cealaltă de dorința de a evita numerele foarte mari sau foarte mici. Astfel, după cum arată figura 9-7, putem fi interesați de lungimi de undă electromagnetice care diferă cu un factor de \(10^{16}\). Deoarece viteza radiației electromagnetice în vid este constantă la \(3 \ ori 10^8 \: \text{m sec}^{-1}\), frecvențele vor diferi cu același factor.
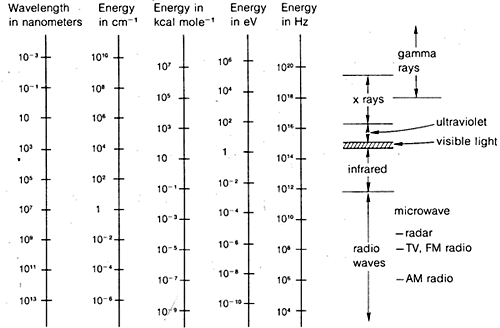
Unitățile utilizate în mod obișnuit pentru lungimea de undă sunt metri (\(\text{m}\)), centimetri (\(\text{cm}\)), nanometri (\(\text{nm}\)) și microni (\(\mu}\)). În trecut, angstromii (\(Å\)) și milimicronii (\(\text{m} \mu m\)) erau, de asemenea, utilizați pe scară largă.
\
\
\
\
Unitățile de frecvență sunt în cicluri pe secundă (cps) sau hertzi (\(\text{Hz}\)), care sunt echivalente (radianții pe secundă sunt folosiți pe scară largă de fizicieni).
Tabelul 9-1: Principalele tehnici spectroscopice utilizate în prezent pentru analiza structurii moleculare

\
\
\
\(^3\)O descriere utilă a modului în care structurile moleculare pot fi determinate prin „viziune cu raze X” este dată în capitolul XI din Organic Molecules in Action de M. Goodman și F. Morehouse, Gordon and Breach, New York, 1973.
- John D. Robert și Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, ediția a doua. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. Acest conținut este protejat prin drepturi de autor în următoarele condiții: „Vi se acordă permisiunea pentru reproducerea, distribuirea, afișarea și interpretarea individuală, educațională, de cercetare și necomercială a acestei lucrări în orice format.”