Modificação do método Winkler para determinação da concentração de oxigênio dissolvido em pequenos volumes de amostra
Primeiro publicado em 27 de Agosto de 2010
Método de Winkler é o procedimento mais popular para determinação da concentração de oxigénio dissolvido (DO) em amostras de água. No entanto, este método requer um volume de amostra relativamente grande de 200 mL para uma determinação precisa da DO. Muitos métodos alternativos têm sido propostos para medir concentrações de DO em pequenos volumes de amostras, mas a maioria desses métodos tem problemas de baixa precisão, alto custo, instrumentação complicada ou tempos de análise longos. Neste artigo, uma simples modificação ao método Winkler é proposta para a medição de concentrações de DO em amostras de 1 mL de volume. O método proposto é preciso, de baixo custo, simples e rápido. As concentrações de DO foram medidas em 33 amostras tanto pelo método Winkler convencional (WM) como pelo método proposto (PM). Para 23 das 33 amostras analisadas, a hipótese de que as médias populacionais das medidas são iguais (μ1 = μ2) não poderia ser rejeitada com um nível de confiança de 95% e para 19 amostras, a hipótese de que as variâncias populacionais das medidas são iguais (σ21 = σ22) não poderia ser rejeitada com um intervalo de confiança de 95%. Assim, concluiu-se que na maioria dos casos, as medições de DO por WM e PM dão resultados comparáveis tanto em termos de precisão como de precisão.
Introdução
Método Winkler (Método No. 4500-O-C)1 foi universalmente aceite como um método preciso e fiável2 para a medição da concentração de oxigénio dissolvido (DO) numa variedade de amostras de água. Este método é considerado como a referência para a determinação da DO. Contudo, a principal desvantagem deste método é a exigência de um grande volume de amostra de 200 mL.3
Números métodos alternativos também foram desenvolvidos para a medição de DO. Estes métodos enquadram-se em três categorias distintas, (1) métodos colorimétricos, (2) métodos que utilizam cromatografia gasosa e (3) métodos que utilizam sensores eletroquímicos e ópticos. Os métodos colorimétricos podem ser usados para a determinação de DO em pequenos volumes de amostra. Entretanto, eles sofrem de inconvenientes como a exigência de reagentes químicos caros (por exemplo, sol de ouro) ou tóxicos (por exemplo, cianeto).4 A falta de justificativa adequada na seleção do comprimento de onda de medição é outro fator limitante para tais métodos.5 A determinação da DO também é possível usando a cromatografia gasosa. No entanto, os métodos cromatográficos a gás, embora precisos e que requerem pequenos volumes de amostras, são, no entanto, demorados e caros. Os sensores eletroquímicos têm sido amplamente utilizados para a medição de DO e suas vantagens e desvantagens têm sido revistas em outros lugares.6 Os sensores eletroquímicos geralmente sofrem efeitos de pressão irreversíveis, contaminação por sulfeto de hidrogênio e sensibilidade cruzada.7 Eles também consomem DO durante a medição e, portanto, podem ser inadequados para volumes muito pequenos de amostras. O foco recente é o desenvolvimento de sensores ópticos baseados no princípio da luminescência dinâmica de oxigênio.8 Estes sensores ópticos são fáceis de usar, têm tempo de resposta rápido e são duráveis. Entretanto, todos os sensores, sejam eletroquímicos ou ópticos, requerem calibração contra o método Winkler devido à sensibilidade dos sensores à temperatura e à pressão.9,10 Eles também são sensíveis ao crescimento de bioincrustantes e bactérias na superfície do sensor.8
Devido às limitações inerentes aos métodos alternativos descritos acima e sua dependência do método Winkler para verificação cruzada e calibração, várias modificações ao próprio método Winkler também foram propostas para medição de concentrações de DO em volumes de amostra de 1-10 mL.11,12,13 Entretanto, tais métodos de ‘Micro-Winkler’ não são muito populares devido às complexas exigências instrumentais e às elaboradas precauções necessárias para evitar a contaminação das amostras através de trocas com oxigênio atmosférico. Estes métodos têm sido revistos criticamente em outros lugares.14 Um método gravimétrico de titulação de Micro-Winkler foi recentemente proposto15 para medição de DO em amostras pequenas. Entretanto, este procedimento requer medições gravimétricas múltiplas e precisas usando um equilíbrio sensível e, portanto, parece ser bastante complexo.
Baseado na revisão da literatura, parece que quase todos os métodos desenvolvidos para medições de DO em amostras pequenas são deficientes de alguma forma ou de outra. Portanto, há uma necessidade contínua de desenvolvimento de um método melhor, ou seja, preciso, preciso, de baixo custo, simples e rápido para medição de DO em pequenos volumes de amostras.
Linha do método proposto
O principal desafio na medição de concentrações de DO em pequenas amostras é a prevenção da contaminação das amostras através da interação com a atmosfera. É proposta a introdução de uma camada líquida isolante entre a amostra de água e a atmosfera. As propriedades necessárias do líquido isolante são: imiscibilidade da água, densidade menor que a água e capacidade de dissolução de oxigênio insignificante. Propõe-se que o líquido isolante seja tomado em um frasco e a amostra de água cuja DO deve ser determinada (1 mL de volume) seja introduzida diretamente abaixo da camada do líquido isolante. A amostra de água é efectivamente selada a partir da atmosfera através desta etapa. A DO na amostra de água pode então ser fixada e convertida em quantidade equivalente de iodo usando os mesmos reagentes usados no método Winkler. A solução de iodo é então extraída do frasco utilizando uma seringa e titulada com Na2S2O3 para determinação da concentração de DO na amostra.
Após várias séries de ensaios, o n-hexano foi escolhido como líquido isolante, como descrito acima. n-Hexano é mais leve que a água (gravidade específica = 0,7) e é virtualmente imiscível em água. A solubilidade do oxigênio no n-hexano é 0,002 fração molar,16i.e., o oxigênio é praticamente insolúvel no n-hexano.
Material e métodos
Todos os reagentes utilizados foram de grau de reagente analítico (>99% de pureza, Loba Chemicals, Índia). Água desionizada (Milli-Q, Millipore, EUA) foi utilizada na preparação de reagentes e diluição de amostras. O n-hexano utilizado foi de grau HPLC (>99% de pureza, Merck, Índia). Os vidros de borosilicato foram utilizados neste estudo. Soluções de MnSO4 e de iodeto alcalinoazídico foram preparadas de acordo com métodos padrão (Método No. 4500-O C).1
O procedimento de medida DO pelo método proposto (PM) foi o seguinte. Inicialmente, 0,5 mL de n-hexano foi transferido para um frasco de vidro de 16 mL (Wheaton Science, EUA). Em seguida, 1 mL de n-hexano foi tomado em uma pipeta de 2 mL, e a pipeta foi ainda preenchida com 1 mL da amostra de água cuja concentração de DO deveria ser determinada. O procedimento de coleta da amostra acima garantiu que a amostra fosse coletada sem headspace. Esta etapa de recolha de amostras é a mais crucial, uma vez que o aparecimento de qualquer bolha ou caixa de ar na interface hexano-água ou em qualquer outro lugar na pipeta pode levar a erros. A boca da pipeta foi então colocada abaixo da camada de hexano no frasco e assim a amostra foi introduzida abaixo da camada de hexano, evitando qualquer contacto entre a amostra e a atmosfera. A coleta da amostra na pipeta e a aplicação da amostra abaixo da camada de hexano no frasco deve ser feita o mais rápido possível, de forma a minimizar erros. Em seguida, 5 μL MnSO4 foi introduzido na amostra de água abaixo da camada de hexano utilizando uma micro seringa 10 μL (Hamilton, EUA), seguida de uma adição semelhante de 5 μL solução de iodetos alcalinoazídicos. A formação de precipitados começou imediatamente após as adições e foi concluída em 3 minutos. Posteriormente, 0,1 mL de H2SO4 conc. foi adicionado usando uma micropipeta ao precipitado formado abaixo da camada de hexano. O precipitado foi dissolvido dentro de 3 min e a solução de iodo amarelo foi formada abaixo da camada de hexano. Exatamente 1 mL da solução de iodo foi extraído de abaixo da camada de hexano usando micro seringa e transferido para um copo de 25 mL. A solução de iodo de 1 mL no béquer foi diluída para ∼10 mL adicionando água de-ionizada para facilitar a titulação. A adição de água desionizada apenas dilui a solução de iodo, sem afetar a quantidade de iodo no copo. O conteúdo do copo foi titulado com solução 0,00625 M Na2S2O3. 1 mL deste titulante corresponde a 55,5 mg L-1 de DO na amostra original. O titulante foi tomado em uma micro seringa de 250 μL (Hamilton, EUA) e adicionado ao copo com agitação constante até que a cor amarela do iodo estivesse quase descarregada. Em seguida, foram adicionadas 1-2 gotas de solução de amido e a titulação continuou até que a cor azul devido ao amido fosse descarregada. Com base no volume de titulação necessário numa determinada titulação, foi calculada a concentração de DO na amostra original.
DO também foi determinada em várias amostras usando o método Winkler’s (WM). Os requisitos de reagente e outros detalhes de ambos os métodos são apresentados na Tabela 1.
| Número de Amostra. | Reagente | Quantidade | Força | |||
|---|---|---|---|---|---|---|
| WM | PM | WM | PM | |||
| Amostra | 200 mL | 1 mL | – | – | ||
| MnSO4 | 1 mL | 5 μL | As por WM | |||
| Alkali-reagente de iodetos azidos | 1 mL | 5 μL | As por WM | |||
| Na2S2O3 | As necessário | As necessário | As necessário | 0.025M | 0.00625M | |
| H2SO4 | 1 mL | 0.1 mL | As por WM | |||
| Amido | 1-2 gotas | 1-2 gotas | As por WM | |||
| n-Hexano | Não usado | 1.5 mL | – | – | ||
Resultados e discussão
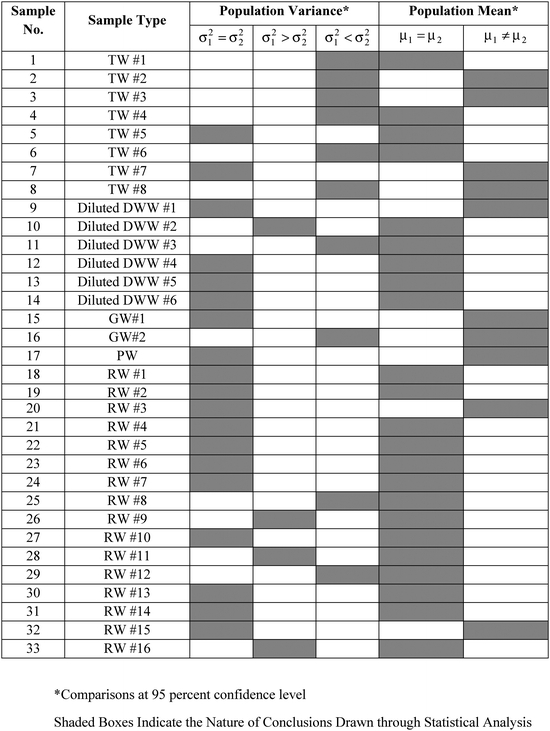
A concentração de DO foi medida em 33 amostras de água (ver Tabela 2) obtidas em vários lugares dentro e ao redor da cidade de Kanpur, Índia. Das 33 amostras, 8 eram amostras de água da torneira, 16 eram amostras de água de rio, 6 eram amostras de águas residuais domésticas diluídas com água da torneira, 2 eram amostras de água subterrânea e 1 era uma amostra de água de tanque. As amostras foram escolhidas de forma a que as concentrações de DO pudessem ser medidas numa grande variedade de matrizes de amostras. Para cada amostra, foram feitas várias medições de DO replicadas, tanto pela WM como pela PM. As médias das amostras calculadas (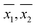 ), os desvios padrão das amostras (S1, S2) e o número de medidas replicadas (n1, n2) para WM e PM respectivamente são apresentados na Tabela 2 para cada amostra.
), os desvios padrão das amostras (S1, S2) e o número de medidas replicadas (n1, n2) para WM e PM respectivamente são apresentados na Tabela 2 para cada amostra.
Pistas normais dos conjuntos de medidas replicadas por ambos os métodos foram todas aproximadamente lineares, indicando que as medidas replicadas foram normalmente distribuídas e, portanto, foram passíveis de análise estatística adicional com base nisso. Para fins ilustrativos, os gráficos normais para cinco medições de amostra realizadas pelo WM são apresentados na Fig. 1A. Os gráficos normais para as mesmas cinco medidas de amostras realizadas pelo WM são apresentados na Fig. 1B.
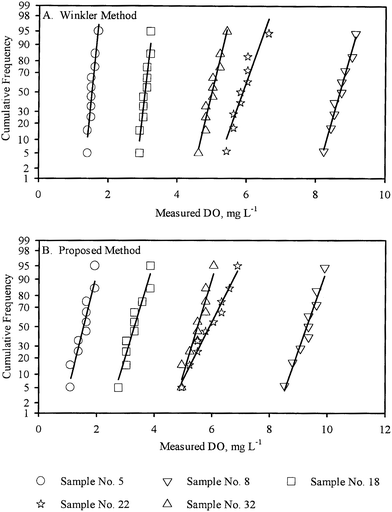
As variâncias (S21,S22) nas medições de réplicas de uma amostra por WM e PM respectivamente foram utilizadas para comparação em pares das variâncias populacionais correspondentes (σ21,σ22) utilizando o teste F. Das 33 amostras para as quais a DO foi medida pelos dois métodos (WM e PM), a hipótese de que as variâncias populacionais eram iguais (σ21 = σ22) não pôde ser rejeitada ao nível de 95% de confiança para 19 amostras. Além disso, a hipótese, σ21 > σ22 não poderia ser rejeitada para 4 amostras, enquanto a hipótese, σ21 < σ22 não poderia ser rejeitada para as 10 amostras restantes, todas ao nível de 95% de confiança. Estes resultados foram resumidos na Tabela 3.
Outras, as variâncias amostrais (S21,S22) e as médias amostrais (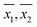 ) para cada amostra, como obtidas por WM e PM respectivamente, foram utilizadas para a comparação das médias populacionais correspondentes (μ1, μ2). Para amostras com variâncias iguais (ver Tabela 3), a comparação em pares foi feita usando o teste t de Student. Para amostras com variâncias desiguais (ver Tabela 3), a comparação em pares foi feita usando o teste t de variância desigual.17 Em 23 das 33 amostras onde as medidas de DO foram feitas tanto pelo WM como pelo PM, a hipótese de que as médias populacionais eram iguais (μ1 = μ2) não pôde ser rejeitada ao nível de 95% de confiança.
) para cada amostra, como obtidas por WM e PM respectivamente, foram utilizadas para a comparação das médias populacionais correspondentes (μ1, μ2). Para amostras com variâncias iguais (ver Tabela 3), a comparação em pares foi feita usando o teste t de Student. Para amostras com variâncias desiguais (ver Tabela 3), a comparação em pares foi feita usando o teste t de variância desigual.17 Em 23 das 33 amostras onde as medidas de DO foram feitas tanto pelo WM como pelo PM, a hipótese de que as médias populacionais eram iguais (μ1 = μ2) não pôde ser rejeitada ao nível de 95% de confiança.
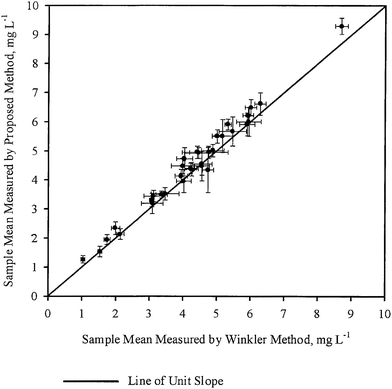
As médias amostrais (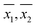 ) para cada amostra, como obtidas pelo WM e PM respectivamente, foram plotadas uma contra a outra na Fig. 2. As barras de erro apresentadas na figura correspondem a intervalos de confiança correspondentes a 95 por cento. Uma linha de inclinação da unidade passando pela origem também foi traçada na mesma figura. Todos os pontos foram observados muito próximos da linha de inclinação da unidade, o que está de acordo com as conclusões gerais da Tabela 3, ou seja, para a maioria das amostras, a concentração média de DO obtida pelos dois métodos não é estatisticamente diferente. Assim, na maioria dos casos, a DO medida por PM foi tão precisa quanto a DO medida por WM.
) para cada amostra, como obtidas pelo WM e PM respectivamente, foram plotadas uma contra a outra na Fig. 2. As barras de erro apresentadas na figura correspondem a intervalos de confiança correspondentes a 95 por cento. Uma linha de inclinação da unidade passando pela origem também foi traçada na mesma figura. Todos os pontos foram observados muito próximos da linha de inclinação da unidade, o que está de acordo com as conclusões gerais da Tabela 3, ou seja, para a maioria das amostras, a concentração média de DO obtida pelos dois métodos não é estatisticamente diferente. Assim, na maioria dos casos, a DO medida por PM foi tão precisa quanto a DO medida por WM.
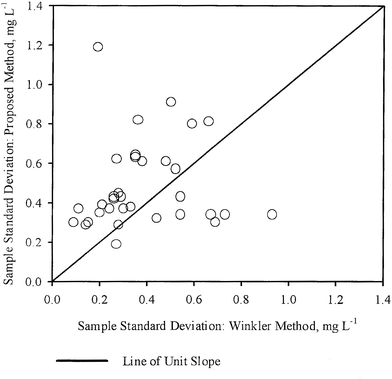
Os desvios padrão da amostra (S1,S2) para cada amostra, como obtidos por WM e PM respectivamente foram plotados um contra o outro na Fig. 3. Uma linha de inclinação da unidade passando pela origem também foi traçada na mesma figura. Neste caso, os pontos parecem estar dispersos de forma bastante uniforme em relação à linha de declive unitário, com alguns pontos próximos da linha, enquanto os outros estão mais afastados. Estas observações também estão em geral de acordo com as conclusões da Tabela 3, ou seja, para a maioria das amostras, a variação na concentração de DO medida pelos dois métodos não é estatisticamente diferente. Assim, na maioria dos casos, a medição de DO por PM foi tão precisa quanto a medição de DO por WM.
Concluiu-se que com um manuseamento e titulação cuidadosos da amostra, o método proposto (PM) pode produzir resultados comparáveis ao método Winkler (WM), tanto em termos de precisão como de precisão. No entanto, a precisão da determinação da DO por PM pode provavelmente ser aumentada usando uma micro-seringa com uma contagem menor para a titulação final. A micro-seringa utilizada neste estudo teve uma contagem mínima de 5 μL, o que corresponde a uma incerteza de ∼0.25 mg L-1 DO sob as condições do presente estudo. Esta incerteza pode ser reduzida usando uma micro seringa com menor contagem.
Conclusões
O objetivo deste estudo foi desenvolver um método preciso, de baixo custo, simples e rápido para a medição da DO em pequenos volumes de amostra. Com base nos resultados e análises apresentadas, pode-se concluir que o método proposto aborda a maioria das questões acima. As principais conclusões do estudo foram as seguintes:
➢ Introdução de uma camada isolante de n-hexano para prevenção de transferência de oxigênio entre a amostra aquosa e a atmosfera resulta na determinação consistente e precisa da DO em pequenos volumes de amostra. Esta é a principal inovação incorporada no método proposto.
➢ Também foi demonstrado que, tomando as precauções adequadas, o método proposto (PM) pode geralmente produzir resultados que são estatisticamente comparáveis com os resultados obtidos pelo método de Winkler (WM), tanto no que diz respeito à concentração média de DO como também no que diz respeito à variância na concentração de DO sobre a média.
➢ As necessidades de reagente e material de vidro para o método proposto são inferiores às do método de Winkler, principalmente devido ao menor volume de amostra utilizado. n-Hexano é o único reagente adicional utilizado, mas a pequena quantidade (∼1.5 mL por amostra) de n-hexano necessária tem um impacto insignificante no custo total da análise da amostra.
Hence o método proposto (PM) pode ser utilizado para medições de DO em todas as circunstâncias em que o método de Winkler é actualmente utilizado. O método proposto é particularmente útil nas circunstâncias em que o método Winkler não pode ser usado devido a limitações no volume de amostras disponíveis.