Modification of Winkler’s method for determination of dissolved oxygen concentration in small sample volumes
Voor het eerst gepubliceerd op 27 augustus 2010
De methode van Winkler is de meest populaire procedure voor de bepaling van de concentratie opgeloste zuurstof (DO) in watermonsters. Deze methode vereist echter een relatief groot monstervolume van 200 ml voor een nauwkeurige DO-bepaling. Er zijn veel alternatieve methoden voorgesteld voor het meten van DO-concentraties in kleine monstervolumes, maar de meeste van die methoden hebben problemen zoals een geringe nauwkeurigheid, hoge kosten, gecompliceerde instrumentatie of lange analysetijden. In dit artikel wordt een eenvoudige wijziging van de Winkler-methode voorgesteld voor het meten van DO-concentraties in monsters met een volume van 1 mL. De voorgestelde methode is nauwkeurig, goedkoop, eenvoudig en snel. De DO-concentraties werden gemeten in 33 monsters met zowel de conventionele Winkler-methode (WM) als de voorgestelde methode (PM). Voor 23 van de 33 geanalyseerde monsters kon de hypothese dat de populatiegemiddelden van de metingen gelijk zijn (μ1 = μ2) niet worden verworpen bij een betrouwbaarheidsinterval van 95 % en voor 19 monsters kon de hypothese dat de populatievarianties van de metingen gelijk zijn (σ21 = σ22) niet worden verworpen bij een betrouwbaarheidsinterval van 95 %. Er werd dus geconcludeerd dat in de meeste gevallen DO-metingen met WM en PM vergelijkbare resultaten opleveren, zowel wat nauwkeurigheid als wat precisie betreft.
Inleiding
De methode van Winkler (Methode nr. 4500-O-C)1 is universeel aanvaard als een nauwkeurige en betrouwbare methode2 voor het meten van de concentratie opgeloste zuurstof (DO) in een verscheidenheid van watermonsters. Deze methode wordt beschouwd als de benchmark voor de bepaling van DO. Het belangrijkste nadeel van deze methode is echter dat een groot monstervolume van 200 ml nodig is.3
Er zijn ook talrijke alternatieve methoden ontwikkeld voor de meting van DO. Deze methoden kunnen in drie categorieën worden onderverdeeld: (1) colorimetrische methoden, (2) methoden waarbij gebruik wordt gemaakt van gaschromatografie en (3) methoden waarbij gebruik wordt gemaakt van elektrochemische en optische sensoren. De colorimetrische methoden kunnen worden gebruikt voor de bepaling van DO in kleine monstervolumes. Zij hebben echter nadelen, zoals het gebruik van dure (b.v. goudoplosbare oplossing) of toxische (b.v. cyanide) chemische reagentia.4 Het ontbreken van een goede motivering bij de keuze van de meetgolflengte is een andere beperkende factor voor dergelijke methoden.5 DO-bepaling is ook mogelijk met behulp van gaschromatografie. Gaschromatografische methoden zijn weliswaar nauwkeurig en vereisen kleine monstervolumes, maar zijn niettemin tijdrovend en duur. Elektrochemische sensoren zijn op grote schaal gebruikt voor DO-meting en de voor- en nadelen ervan zijn elders besproken.6 Elektrochemische sensoren hebben in het algemeen te lijden van onomkeerbare drukeffecten, verontreiniging door waterstofsulfide en kruisgevoeligheid.7 Zij verbruiken ook DO tijdens de meting en zijn daarom wellicht ongeschikt voor zeer kleine monstervolumes. De laatste tijd ligt de nadruk op de ontwikkeling van optische sensoren op basis van het principe van dynamische zuurstofluminiscentie-quenching.8 Deze optische sensoren zijn gemakkelijk in het gebruik, hebben een snelle responstijd en zijn duurzaam. Alle sensoren, zowel elektrochemische als optische, moeten echter worden gekalibreerd volgens de methode van Winkler wegens de gevoeligheid van de sensoren voor temperatuur en druk.9,10 Zij zijn ook gevoelig voor biofouling en bacteriegroei op het sensoroppervlak.8
Vanwege de inherente beperkingen van alternatieve methoden zoals hierboven beschreven en hun afhankelijkheid van de Winkler-methode voor kruiscontrole en ijking, zijn ook verscheidene modificaties van de Winkler-methode zelf voorgesteld voor het meten van DO-concentraties in monstervolumes van 1-10 ml.11,12,13 Dergelijke “Micro-Winkler”-methoden zijn echter niet erg populair vanwege de complexe instrumentele vereisten en de uitgebreide voorzorgsmaatregelen die nodig zijn om besmetting van de monsters door uitwisseling met atmosferische zuurstof te voorkomen. Deze methoden zijn elders kritisch besproken.14 Onlangs is een gravimetrische Micro-Winkler titratiemethode voorgesteld15 voor de meting van DO in kleine monsters. Deze procedure vereist echter meervoudige en nauwkeurige gravimetrische metingen met behulp van een gevoelige balans en blijkt dus vrij complex te zijn.
Uit het literatuuroverzicht blijkt dat bijna alle methoden die zijn ontwikkeld voor DO-metingen in kleine monsters, op de een of andere manier tekortschieten. Vandaar dat er een voortdurende behoefte is aan de ontwikkeling van een betere, d.w.z. nauwkeurige, precieze, goedkope, eenvoudige en snelle methode voor DO-meting in kleine monstervolumes.
Opzet van de voorgestelde methode
De voornaamste uitdaging bij het meten van DO-concentraties in kleine monsters is het voorkomen van verontreiniging van de monsters door interactie met de atmosfeer. Voorgesteld wordt een isolerende vloeistoflaag aan te brengen tussen het watermonster en de atmosfeer. Vereiste eigenschappen van de isolerende vloeistof zijn: onvermengbaar met water, dichtheid kleiner dan die van water en verwaarloosbaar zuurstofoplossend vermogen. Voorgesteld wordt de isolerende vloeistof in een flesje te doen en het watermonster waarvan de DO moet worden bepaald (volume 1 mL) direct onder de isolerende vloeistoflaag in te brengen. Het watermonster wordt door deze stap doeltreffend van de atmosfeer afgesloten. Het DO in het watermonster kan vervolgens worden gefixeerd en omgezet in een equivalente hoeveelheid jood met behulp van dezelfde reagentia als gebruikt bij de Winkler-methode. De joodoplossing wordt vervolgens met een injectiespuit uit het flesje geëxtraheerd en getitreerd met Na2S2O3 voor de bepaling van de DO-concentratie in het monster.
Na verschillende ronden van proeven werd n-hexaan gekozen als de isolerende vloeistof zoals hierboven beschreven. n-Hexaan is lichter dan water (soortelijk gewicht = 0,7) en is vrijwel niet mengbaar met water. De oplosbaarheid van zuurstof in n-hexaan is 0,002 mol fractie,16 d.w.z. dat zuurstof praktisch onoplosbaar is in n-hexaan.
Materiaal en methoden
Alle gebruikte reagentia waren van analytische reagenskwaliteit (>99% zuiverheid, Loba Chemicals, India). Gedeïoniseerd water (Milli-Q, Millipore, USA) werd gebruikt voor de bereiding van reagentia en de verdunning van monsters. Het gebruikte n-hexaan was van HPLC-kwaliteit (zuiverheid >99%, Merck, India). In dit onderzoek werd borosilicaatglaswerk gebruikt. MnSO4- en alkali-azide-jodide-oplossingen werden bereid volgens standaardmethoden (Methode nr. 4500-O C).1
De DO-meetprocedure volgens de voorgestelde methode (PM) was als volgt. Aanvankelijk werd 0,5 mL n-hexaan overgebracht in een glazen flesje van 16 mL (Wheaton Science, USA). Vervolgens werd 1 mL n-hexaan in een pipet van 2 mL gebracht en de pipet werd verder gevuld met 1 mL van het watermonster waarvan de DO-concentratie moest worden bepaald. De bovenstaande procedure voor de monsterafname zorgde ervoor dat het monster werd verzameld zonder headspace. Deze bemonsteringsstap is de meest cruciale, aangezien het ontstaan van luchtbellen of luchtspleet in het hexaan-water-interface of elders in de pipet tot fouten kan leiden. De mond van de pipet werd vervolgens onder de hexaanlaag in het flesje geplaatst en zo werd het monster onder de hexaanlaag ingebracht, waardoor elk contact tussen het monster en de atmosfeer werd vermeden. Het verzamelen van het monster in de pipet en het aanbrengen van het monster onder de hexaanlaag in het flesje moet zo snel mogelijk gebeuren om fouten te minimaliseren. Vervolgens werd 5 μl MnSO4 in het watermonster onder de hexaanlaag gebracht met een 10 μl microspuit (Hamilton, USA), gevolgd door een gelijkaardige toevoeging van 5 μl alkali-azide-jodide-oplossing. De neerslagvorming begon onmiddellijk na de toevoegingen en was binnen 3 min voltooid. Daarna werd 0,1 mL conc. H2SO4 toegevoegd met een micropipet aan het neerslag gevormd onder hexaan laag. Het neerslag werd binnen 3 min opgelost en onder de hexaanlaag werd een gele joodoplossing gevormd. Precies 1 mL van de joodoplossing werd met een microspuit van onder de hexaanlaag afgezogen en overgebracht in een bekerglas van 25 mL. De 1 mL joodoplossing in het bekerglas werd verdund tot ∼10 mL door toevoeging van gedeïoniseerd water om de titratie te vergemakkelijken. Door de toevoeging van gedeïoniseerd water wordt de jodiumoplossing alleen verdund, zonder dat dit van invloed is op de hoeveelheid jodium in het bekerglas. De inhoud van het bekerglas werd getitreerd met 0,00625 M Na2S2O3 oplossing. 1 mL van deze titrant komt overeen met 55,5 mg L-1 DO in het oorspronkelijke monster. De titrant werd in een microspuit van 250 μL (Hamilton, USA) gebracht en onder voortdurend roeren druppelsgewijs aan het bekerglas toegevoegd tot de gele kleur van jodium bijna verdwenen was. Vervolgens werden 1-2 druppels zetmeeloplossing toegevoegd en werd de titratie voortgezet totdat de blauwe kleur als gevolg van zetmeel was verdwenen. Aan de hand van het volume titrant dat bij een bepaalde titratie nodig was, werd de DO-concentratie in het oorspronkelijke monster berekend.
De DO-concentratie werd ook in verschillende monsters bepaald met behulp van de Winkler’s methode (WM). De benodigde reagentia en andere bijzonderheden van beide methoden zijn vermeld in tabel 1.
| MonsterNr. | Reagens | Hoeveelheid | Sterkte | ||
|---|---|---|---|---|---|
| WM | PM | WM | PM | ||
| Sample | 200 mL | 1 mL | – | – | |
| MnSO4 | 1 mL | 5 μL | Zoals per WM | ||
| Alkali-azide-jodide reagens | 1 mL | 5 μL | Zoals per WM | ||
| Na2S2O3 | Zoals vereist | 0.025M | 0.00625M | ||
| H2SO4 | 1 mL | 0.1 mL | Zoals per WM | ||
| Stijfsel | 1-2 druppels | 1-2 druppels | Zoals per WM | ||
| n-Hexaan | Niet gebruikt | 1.5 mL | – | – | |
Resultaten en discussie
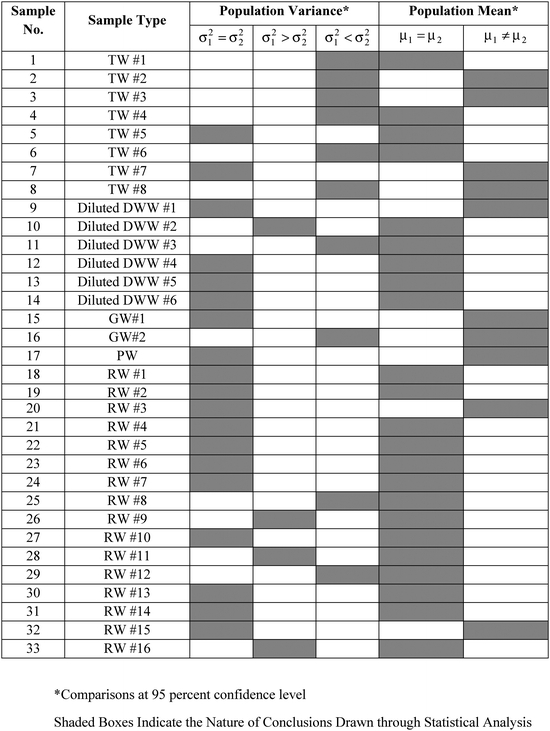
De DO-concentratie werd gemeten in 33 watermonsters (zie tabel 2) die afkomstig waren van verschillende plaatsen in en rond de stad Kanpur, India. Van de 33 monsters waren er 8 leidingwatermonsters, 16 rivierwatermonsters, 6 met leidingwater verdunde monsters van huishoudelijk afvalwater, 2 grondwatermonsters en 1 vijverwatermonster. De monsters werden zo gekozen dat de DO-concentratie kon worden gemeten in een grote verscheidenheid van monstermatrices. Voor elk monster werden verschillende replicaat DO-metingen verricht, zowel door WM als door de PM. De berekende monstergemiddelden (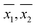 ), de standaardafwijkingen van de monsters (S1, S2) en het aantal herhalingsmetingen (n1, n2) voor respectievelijk WM en PM zijn voor elk monster weergegeven in tabel 2.
), de standaardafwijkingen van de monsters (S1, S2) en het aantal herhalingsmetingen (n1, n2) voor respectievelijk WM en PM zijn voor elk monster weergegeven in tabel 2.
Normale plots van de reeksen herhalingsmetingen met beide methoden waren alle bij benadering lineair, wat erop wijst dat de herhalingsmetingen normaal verdeeld waren en derhalve op die basis voor verdere statistische analyse in aanmerking kwamen. Ter illustratie zijn in fig. 1A de normaalgrafieken voor vijf met de WM uitgevoerde monstermetingen weergegeven. De normale grafieken voor dezelfde vijf monsters, uitgevoerd door de PM, staan in Fig. 1B.
De varianties (S21,S22) in de herhalingsmetingen van een monster door respectievelijk WM en PM werden gebruikt voor een paarsgewijze vergelijking van de overeenkomstige populatievarianties (σ21,σ22) met behulp van de F-toets. Van de 33 monsters waarvoor de DO met de twee methoden (WM en PM) werd gemeten, kon de hypothese dat de populatievarianties gelijk waren (σ21 = σ22) voor 19 monsters niet worden verworpen bij een betrouwbaarheidsniveau van 95 %. Voorts kon de hypothese σ21 > σ22 voor 4 steekproeven niet worden verworpen, terwijl de hypothese σ21 < σ22 voor de overige 10 steekproeven niet kon worden verworpen, en dit alles bij een betrouwbaarheidsniveau van 95 %. Deze resultaten zijn samengevat in tabel 3.
Verder werden de steekproefvarianties (S21,S22) en steekproefgemiddelden (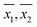 ) voor elk monster, zoals verkregen door respectievelijk WM en PM, gebruikt voor de paarsgewijze vergelijking van de overeenkomstige populatiegemiddelden (μ1, μ2). Voor steekproeven met gelijke varianties (zie tabel 3) werd de vergelijking per paar uitgevoerd met behulp van de Student’s t-toets. Voor monsters met ongelijke varianties (zie tabel 3) is de vergelijking per monster uitgevoerd met behulp van de t-toets voor ongelijke variantie.17 In 23 van de 33 monsters waarbij de DO-metingen zowel door WM als door PM werden uitgevoerd, kon de hypothese dat de populatiegemiddelden gelijk waren (μ1 = μ2) niet worden verworpen bij een betrouwbaarheidsniveau van 95 %.
) voor elk monster, zoals verkregen door respectievelijk WM en PM, gebruikt voor de paarsgewijze vergelijking van de overeenkomstige populatiegemiddelden (μ1, μ2). Voor steekproeven met gelijke varianties (zie tabel 3) werd de vergelijking per paar uitgevoerd met behulp van de Student’s t-toets. Voor monsters met ongelijke varianties (zie tabel 3) is de vergelijking per monster uitgevoerd met behulp van de t-toets voor ongelijke variantie.17 In 23 van de 33 monsters waarbij de DO-metingen zowel door WM als door PM werden uitgevoerd, kon de hypothese dat de populatiegemiddelden gelijk waren (μ1 = μ2) niet worden verworpen bij een betrouwbaarheidsniveau van 95 %.
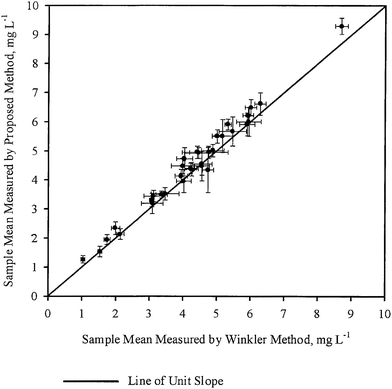
De steekproefgemiddelden (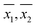 ) voor elk monster, zoals verkregen door respectievelijk WM en PM, zijn tegen elkaar uitgezet in fig. 2. De foutbalkjes in de figuur corresponderen met de bijbehorende 95 % betrouwbaarheidsintervallen. In dezelfde figuur is ook een lijn met een helling per eenheid door de oorsprong getrokken. Alle punten bleken zeer dicht bij de eenheidshelling te liggen, hetgeen in overeenstemming is met de algemene conclusies van tabel 3, namelijk dat voor de meeste monsters de gemiddelde DO-concentratie die met de twee methoden wordt verkregen, statistisch niet verschilt. In de meeste gevallen was de DO-meting met behulp van PM dus even nauwkeurig als de DO-meting met behulp van WM.
) voor elk monster, zoals verkregen door respectievelijk WM en PM, zijn tegen elkaar uitgezet in fig. 2. De foutbalkjes in de figuur corresponderen met de bijbehorende 95 % betrouwbaarheidsintervallen. In dezelfde figuur is ook een lijn met een helling per eenheid door de oorsprong getrokken. Alle punten bleken zeer dicht bij de eenheidshelling te liggen, hetgeen in overeenstemming is met de algemene conclusies van tabel 3, namelijk dat voor de meeste monsters de gemiddelde DO-concentratie die met de twee methoden wordt verkregen, statistisch niet verschilt. In de meeste gevallen was de DO-meting met behulp van PM dus even nauwkeurig als de DO-meting met behulp van WM.
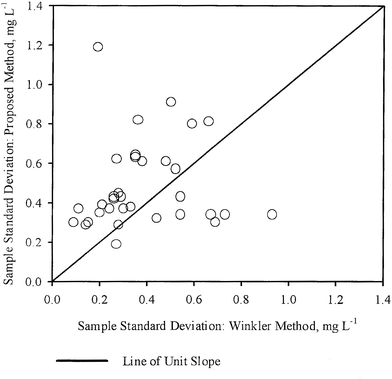
De standaardafwijkingen van de monsters (S1,S2) voor elk monster, zoals verkregen met respectievelijk WM en PM, zijn tegen elkaar uitgezet in Fig. 3. In dezelfde figuur is ook een lijn met een helling per eenheid door de oorsprong getrokken. In dit geval blijken de punten tamelijk gelijkmatig verdeeld te zijn ten opzichte van de eenheidshelling, waarbij sommige punten dicht bij de lijn liggen, terwijl de andere verder weg liggen. Deze waarnemingen komen ook in grote lijnen overeen met de conclusies van tabel 3, d.w.z. dat voor de meeste monsters de variatie in de DO-concentratie die met de twee methoden wordt gemeten, statistisch niet verschillend is. In de meeste gevallen was de DO-meting met PM dus even nauwkeurig als de DO-meting met WM.
Geconcludeerd werd dat met zorgvuldige monsterbehandeling en titratie de voorgestelde methode (PM) resultaten kan opleveren die vergelijkbaar zijn met de methode van Winkler (WM), zowel wat nauwkeurigheid als wat precisie betreft. Niettemin kan de nauwkeurigheid van de DO-bepaling met PM waarschijnlijk worden vergroot door voor de eindtitratie een micro-injectiespuit te gebruiken met een lager kleinste aantal. De in deze studie gebruikte micro-injectiespuit had een kleinste aantal van 5 μL, wat overeenkomt met een onzekerheid van ∼0,25 mg L-1 DO onder de omstandigheden van de huidige studie. Deze onzekerheid kan worden verminderd door gebruik te maken van een micro-injectiespuit met een lager kleinste aantal.
Conclusies
Het doel van deze studie was de ontwikkeling van een nauwkeurige, goedkope, eenvoudige en snelle methode voor de meting van DO in kleine monstervolumes. Op basis van de gepresenteerde resultaten en analyse kan worden geconcludeerd dat met de voorgestelde methode de meeste van de bovengenoemde problemen worden aangepakt. De belangrijkste conclusies van de studie waren de volgende:
➢ De invoering van een isolerende laag n-hexaan ter voorkoming van zuurstofoverdracht tussen het waterige monster en de atmosfeer resulteert in een consistente en nauwkeurige bepaling van DO in kleine monstervolumes. Dit is de belangrijkste vernieuwing die in de voorgestelde methode is verwerkt.
➢ Ook is aangetoond dat de voorgestelde methode (PM) met de juiste voorzorgsmaatregelen over het algemeen resultaten kan opleveren die statistisch vergelijkbaar zijn met de resultaten die met de methode van Winkler (WM) worden verkregen, zowel wat betreft de gemiddelde DO-concentratie als wat betreft de variantie in DO-concentratie ten opzichte van het gemiddelde.
➢ De reagentia en het glaswerk die voor de voorgestelde methode nodig zijn, zijn geringer dan die van de methode van Winkler, voornamelijk door het kleinere monstervolume dat wordt gebruikt. n-Hexaan is het enige extra reagens dat wordt gebruikt, maar de geringe hoeveelheid (∼1,5 ml per monster) n-hexaan die nodig is, heeft een verwaarloosbaar effect op de totale kosten van de monsteranalyse.
Hieruit volgt dat de voorgestelde methode (PM) kan worden gebruikt voor DO-metingen onder alle omstandigheden waarin de methode van Winkler momenteel wordt gebruikt. De voorgestelde methode is bijzonder nuttig in omstandigheden waarin de Winkler-methode niet kan worden gebruikt wegens beperkingen van het beschikbare monstervolume.