Lavado pulmonar completo bilateral en la proteinosis alveolar pulmonar – Un estudio retrospectivo
Introducción
La proteinosis alveolar pulmonar (PAP) es una rara enfermedad pulmonar difusa con tres formas clínicas, congénita, adquirida (idiopática) y secundaria, caracterizada por la acumulación de grandes cantidades de un material fosfolipoproteínico en los alvéolos debido a una deficiencia en la actividad del factor estimulante de colonias de granulocitos-macrófagos (GM-CSF)1-14 (Fig. 1). Esto se asocia a una función anormal de los macrófagos y a una deficiente eliminación del surfactante de los pulmones. La PAP tiene una prevalencia de 3,7 casos por millón, una preponderancia masculina (relación 4:1 hombre/mujer) y el 80% de los casos se registran durante la tercera y cuarta década de la vida.6
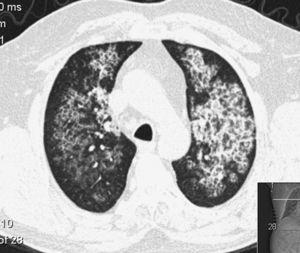
TAC de un paciente con Proteinosis Alveolar Pulmonar. Obsérvese el engrosamiento de los septos interlobulares dentro del parénquima opacificado que produce un patrón de «pavimento loco».
El Lavado Pulmonar Integral (LAP), introducido en la década de 1960,3,4,7,10,15 sigue siendo el tratamiento de referencia.6 El WLL unilateral, con el lavado realizado en cada pulmón en diferentes sesiones separadas por días/semanas, es el procedimiento más frecuente. Sin embargo, el WLL secuencial bilateral en la misma sesión de tratamiento es una alternativa atractiva, ya que consume mucho menos tiempo, con una cantidad reducida de molestias para el paciente y es más rentable.
Su eficacia se ha atribuido no sólo a la eliminación del material lipoproteínico de los espacios alveolares, sino también a la eliminación de los anticuerpos anti GM-CSF, los macrófagos alveolares y las células epiteliales de tipo II. Este procedimiento terapéutico se plantea cuando el paciente refiere una limitación importante en sus actividades diarias y/o se detecta una hipoxemia con una pO2
60mmHg, una P(A-a) O2 ≥40mmHg y una fracción de derivación ≥10%.12
En nuestro Hospital, realizamos la primera LEBM en 2010 y, tras cinco LEBM unilaterales, pasamos a un programa de LEBM bilateral secuencial.
El objetivo de este informe es describir la técnica de LEBM bilateral y discutir su seguridad y eficacia.
Métodos
En este estudio retrospectivo, recogimos datos demográficos y clínicos de los informes médicos de tres pacientes adultos. La técnica estándar aplicada fue una versión modificada del protocolo de la técnica del Royal Brompton Hospital (Londres).6,10
Durante todo el procedimiento se monitorizaron continuamente la electrocardiografía, la oximetría de pulso (SatO2), la presión arterial invasiva, la presión venosa central (PVC), la diuresis, la capnografía, los volúmenes tidales, el índice biespectral (BIS) y la temperatura central, y los gases sanguíneos arteriales (GSA) se realizaron cada hora. Se realizó una anestesia intravenosa total (TIVA) para poder gestionar la profundidad de la anestesia, independientemente de las variaciones ventilatorias inherentes al procedimiento. Se mantuvo la curarización durante todo el procedimiento. Se introdujo un tubo de doble luz (DLT) izquierdo, seleccionando el mayor tamaño posible, para asegurar el aislamiento pulmonar y favorecer la ventilación y la eficacia de la WLL. Se confirmó su correcta posición mediante broncoscopia de fibra óptica y se midió la presión de insuflación del manguito para evitar la fuga contralateral del líquido de lavado.11
Se realizó una preoxigenación con una FiO2 del 100% durante 5min para asegurar una correcta desnitrogenación alveolar y la aparición de burbujas de aire, que podrían perjudicar la eliminación del material lipoproteico de los alvéolos. Se inició la ventilación monopulmonar y se verificó el aislamiento pulmonar. Los pacientes fueron ventilados mediante ventilación controlada por presión, con un valor de presión inferior a 30cmH2O. El volumen de suero salino a instilar se calculó mediante las mediciones preoperatorias de la capacidad residual funcional (CRF). El volumen del pulmón derecho se calculó en 3/5 de la CRF y el del izquierdo en 2/5 de la CRF (en el primer ciclo se instiló un volumen menor). El suero salino debe instilarse bajo efecto gravitacional desde una altura no superior a los 40 cm por encima de la línea axilar media, para evitar el barotrauma y las fugas al pulmón ventilado.10 Aunque algunos informes describen una posición de decúbito lateral de 30° para preservar la relación ventilación/perfusión del pulmón ventilado dependiente, esto aumenta la probabilidad de inundación del pulmón contralateral, por lo que preferimos una posición de decúbito dorsal, con un trendelenburg inverso, así como una posición de trendelenburg para facilitar la instilación gravitacional y la retirada del suero salino caliente de los pulmones.6,11 Esta posición se adoptó cuando se realizó una WLL bilateral (Fig. 2).
Representación técnica de un WLL.
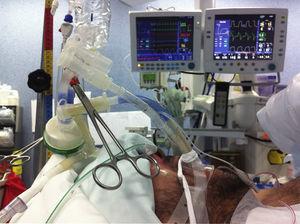
Cuando el flujo de salida, inicialmente lechoso, se hizo menos denso, se interrumpió el drenaje a la mitad del volumen, y varios ciclos de ventilación manual utilizando una válvula de CPAP con 5-10mmHg de límite de presión (la «modificación Bingisser») permitieron una percusión manual de los alvéolos. Esta maniobra mejora en gran medida el aclaramiento lipoproteico.12,14 El ciclo de lavado se repitió hasta que el flujo de salida del lavado se volvió límpido (Fig. 3). Dado que el volumen de lavado de líquidos es elevado durante el procedimiento, existe un alto riesgo de hipotermia. La conservación de la temperatura corporal es crucial y debe mantenerse utilizando líquido de lavado calentado a 37°C y una manta de calentamiento.

Evolución del líquido lechoso a lo largo del procedimiento.
Después de que el primer pulmón fuera lavado con éxito, se succionó cuidadosamente y se realizó su reexpansión, inicialmente mediante ventilación bilateral seguida de ventilación unilateral. Tras 1h de ventilación, se verificaron los datos de distensibilidad pulmonar y de análisis de gases en sangre. Si el pulmón lavado podía asegurar las necesidades de intercambio gaseoso del paciente, entonces se iniciaba la WLL contralateral, repitiendo los procedimientos descritos anteriormente.8
Al final del procedimiento se aspiraba la solución salina residual a través de broncoscopia de fibra óptica y se reanudaba la ventilación bilateral. A continuación se sustituyó el tubo de doble lumen por un tubo endotraqueal y se trasladó al paciente a una unidad de recuperación para su monitorización durante la noche.
Resultados
Se realizó WWL bilateral en tres pacientes adultos, 2 varones y 1 mujer, con una edad media de 43,6 (rango 39 – 47 años) (Tabla 1) todos ellos con hipoxia en reposo inferior a 60mmHg.
Cantidad de solución salina instilada y retenida en WWL bilateral.
| Lavajes | Volumen (L) pulmón derecho | Volumen (L) pulmón izquierdo | ||
| Volumen instilado volumen (L) | Balance positivo (mL) | Volumen destilado (L) | Balance positivo (mL) | |
| 1ª | 9.2 | 470 | 11,8 | 510 |
| 2° | 15,3 | 530 | 10,7 | 450 |
| 3° | 14.0 | 600 | 10,8 | 550 |
| 4ª | 13,5 | 500 | 10,6 | 350 |
| 5ª | 15.5 | 930 | 11,1 | 480 |
| 6ª | 15,5 | 820 | 15.3 | 900 |
El primer paciente era varón, de 39 años, fumador, panadero, diagnosticado de PAP un mes antes de la primera WLL, en base a las características clínicas, radiológicas y del BAL y a la presencia de anticuerpos séricos del GM-CSF. En el momento de la presentación de la enfermedad, presentaba una insuficiencia respiratoria asociada a una amplia afectación pulmonar bilateral observada en la TCAR, y se realizó una LEB bilateral con 9,2 y 11,8 l de solución salina instilada en el pulmón derecho e izquierdo respectivamente. Tras un breve periodo de mejora clínica, funcional y radiológica, el estado del paciente empeoró con la extensión de las opacidades pulmonares radiológicas y la insuficiencia respiratoria. Este deterioro clínico coincidió con su vuelta al trabajo. De hecho, la harina de panadería se había descrito como un posible factor desencadenante.16 Tres meses más tarde se realizó una segunda WLL bilateral y se instilaron 15,3 y 10,7 L de solución salina. Tras este procedimiento y el cese de su entorno laboral previo, el paciente mantuvo la estabilidad clínica.
El segundo paciente sometido a WLL era una mujer de 47 años, agricultora, no fumadora, sin comorbilidades, con el diagnóstico de PAP un mes antes de la primera WLL en base a las características clínicas, radiológicas y de BAL y la presencia de anticuerpos séricos de GM-CSF. La presentación clínica fue muy similar a la del primer paciente, con disnea de esfuerzo y tos seca asociada a insuficiencia respiratoria y amplias opacidades bilaterales en patrón de pavimento loco en la TCAR. Tras el diagnóstico, se realizó un WLL con instilación de 14 y 10,8L de suero salino en el pulmón derecho e izquierdo respectivamente. Tras una breve mejoría clínica inicial, fue sometida a otra WLL 1,5 meses después, ya que se había vuelto más sintomática y con paO2
60mmHg. Con este procedimiento, se instilaron un total de 13,5 y 10,6L en el pulmón derecho e izquierdo respectivamente. Cuatro meses más tarde se realizó un tercer WLL debido al deterioro clínico y en esta ocasión se instilaron 15,5 y 11,1L en el pulmón derecho e izquierdo respectivamente (Fig. 4). Después de este procedimiento, el paciente alcanzó la estabilidad clínica, funcional y radiológica.

Muestras secuenciales de WLL bilaterales.
El tercer paciente incluido fue un varón de 45 años, exfumador, trabajador de una fábrica de neumáticos, con el diagnóstico de PAP durante la evaluación y tratamiento de un absceso cerebral inducido por nocardia. Al igual que en los otros dos pacientes, el diagnóstico se estableció por los rasgos radiológicos y de BAL típicos asociados a los anticuerpos séricos del GM-CSF. Sin embargo, dos años antes se le había practicado una TCAR torácica con patrón de pavimento loco bilateral. Un año después del diagnóstico, se volvió más sintomático, con disnea de esfuerzo e insuficiencia respiratoria (paO2-57mmHg), por lo que fue sometido a un WLL con instilación de 15,5 y 15,3 de solución salina en el pulmón derecho e izquierdo respectivamente. Después de este procedimiento, consiguió una mejora clínica, funcional y radiológica significativa.
Los seis procedimientos de WLL se llevaron a cabo según el protocolo establecido y sin ninguna complicación importante.
La monitorización gasométrica horaria se centró en asegurar una correcta oxigenación y ventilación. Los valores gasométricos del paciente se mantuvieron sin problemas durante todo el procedimiento, con una pCO2 por debajo de 55mmHg y una SpO2 sostenida por encima de los valores propios del paciente actual aunque estuviera en posición supina (Tabla 2) (Fig. 5). En efecto, en todos los pacientes sometidos a WWL bilateral observamos una instalación progresiva de la acidosis metabólica durante el procedimiento. Esta acidosis metabólica se revirtió en las primeras horas del postoperatorio y después no se identificaron comorbilidades.
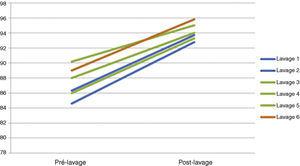
Evolución de la medición de SatO2 durante los lavados pulmonares completos.
Con la maniobra de Bingisser observamos una dificultad transitoria para recuperar el volumen de lavado (contribuyendo a un balance de fluidos positivo) pero un evidente aumento de la densidad del lavado.
En cualquier caso observamos un episodio de extravasación del lavado contralateral. En todos los procedimientos la temperatura corporal se mantuvo entre 36 y 37°C. El tiempo medio del procedimiento fue de 8h (rango 7h32-9h41).
El tiempo hasta la extubación varió en función de la evolución clínica y de los análisis de gases en sangre y todos los pacientes fueron extubados con éxito después de 18h.
Después de estos procedimientos la capacidad funcional y las actividades diarias de todos los pacientes mejoraron significativamente, documentadas por los signos/síntomas clínicos así como por las pruebas de función respiratoria y los datos gasométricos.
Discusión
En esta breve comunicación describimos seis procedimientos secuenciales bilaterales de WLL, realizados en tres pacientes con PAP, corroborando su eficacia clínica y seguridad.
A pesar de su importante invasividad, la WLL sigue siendo el tratamiento recomendado en la PAP, y ha sido hasta ahora la única terapéutica con eficacia establecida. De hecho, cuando un paciente con PAP presenta insuficiencia respiratoria y opacidades extensas en la TCAR, este procedimiento es obligatorio. La WLL es una técnica costosa y que requiere mucho tiempo, exige la experiencia de un enfoque multidisciplinar y esto, junto con la rareza de la PAP, explica por qué este procedimiento sólo se realiza en un pequeño número de centros. La elección de un WLL bilateral supone una mayor comodidad para el paciente, una reducción del coste y del tiempo y el mantenimiento de la eficacia clínica.
Los tres pacientes incluidos podrían considerarse casos típicos de PAP, aunque había algunas diferencias. Dos de ellos tuvieron una presentación aguda de la enfermedad, necesitando WLL después del diagnóstico mientras que el otro fue sometido a este procedimiento durante el curso de la enfermedad. Mientras que este tercer paciente tuvo que ser sometido a un solo WLL, los otros dos tuvieron que someterse a múltiples WLL, concretamente a dos y tres procedimientos.
El factor crucial para poder proceder al segundo lavado pulmonar es si el primer lavado pulmonar ha recuperado la capacidad suficiente para asegurar las necesidades del paciente. Por esta razón, si no hay predominio lateral, elegimos el pulmón más grande, el derecho, para ser lavado en primer lugar. Para evitar el barotrauma, la presión inspiratoria máxima se limitó a 30cmH2O. En todos los procedimientos, tras 1h de ventilación, la distensibilidad pulmonar y los valores gasométricos en ventilación unipulmonar del pulmón lavado fueron compatibles con el inicio del lavado del segundo pulmón.
La elección de la ventilación controlada por presión nos permitió monitorizar continuamente los cambios en la distensibilidad pulmonar durante el lavado y evitó la posible dislocación del tubo o cualquier otra interferencia. Además, del mismo modo, permitió observar la recuperación de la distensibilidad pulmonar del lavado.
La posición supina del paciente no dificultó la oxigenación, por lo que no tuvimos que recurrir a la posición de decúbito lateral con ventilación del pulmón dependiente, posicionamiento que es menos estable y conlleva mayores riesgos en un procedimiento prolongado (media de 8h).
Elegimos la maniobra de percusión de Bingisser debido a que se mide la presión ejercida sobre las vías aéreas, a diferencia de lo que ocurre en las maniobras de kinesioterapia, donde esa cuantificación es imposible, reduciendo así el riesgo de una presión excesiva de percusión, evitando y previniendo una posible inundación contralateral.8
En un intento de revertir la acidosis metabólica observada durante los procedimientos, el suero de mantenimiento utilizado en el periodo perioperatorio -cloruro sódico al 0,9%- fue sustituido por lactato de ringer en el tercer procedimiento bilateral y en los posteriores, con sólo modestas mejoras. En la literatura no hay ninguna referencia al uso de este soluto como líquido de lavado pulmonar, por lo que el cloruro sódico sigue utilizándose.
En conclusión, teniendo en cuenta la eficacia clínica del WLL bilateral, sus ventajas en el ahorro de tiempo y costes y la reducción de las molestias del paciente hacen de esta técnica una primera opción adecuada en el lavado terapéutico en pacientes con PAP.
Declaraciones éticasProtección de los sujetos humanos y animales
Los autores declaran que los procedimientos seguidos se ajustaron a las normas del comité de ética de investigación clínica correspondiente y a las del Código de Ética de la Asociación Médica Mundial (Declaración de Helsinki).
Confidencialidad de los datos
Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la intimidad y consentimiento informado
Los autores declaran que en este artículo no aparecen datos de pacientes.
Conflictos de intereses
Los autores no tienen conflictos de intereses que declarar.